Al2O3 অম্ল ও ক্ষার উভয়ের সাথে বিক্রিয়া করে লবণ উৎপন্ন করে।
অম্লরূপে: Al2O3(s) + 2NaOH(aq) → 2NaAl(OH)4(aq)
ক্ষাররূপে: Al2O3(s) + 6HCl(aq) → 2AlCl3(aq) + 3H2O(l)
এজন্য, Al2O3 একটি উভধর্মী পদার্থ।
Al₂O₃ (অ্যালুমিনিয়াম অক্সাইড) কে উভধর্মী অক্সাইড বলা হয় কারণ এটি উভয় ধরনের পদার্থের সাথে বিক্রিয়া করতে পারে — অর্থাৎ, অম্ল (acid) এবং ক্ষার (base) — উভয়ের সাথেই বিক্রিয়া করে।
🔬 উভধর্মী পদার্থ কী?
যে যৌগ অম্লের সাথেও এবং ক্ষারের সাথেও বিক্রিয়া করে, তাকে উভধর্মী (amphoteric) পদার্থ বলে।
⚗️ Al₂O₃ এর উভধর্মীতা প্রমাণ:
✅ ১. অম্লের সাথে বিক্রিয়া (অ্যাসিডিক আচরণ):
Al₂O₃ একটি ক্ষারীয় অক্সাইড হিসেবে আচরণ করে এবং অম্লের সাথে লবণ ও পানি তৈরি করে।
উদাহরণ:
Al2O3+6HCl→2AlCl3+3H2O
👉 এখানে HCl একটি অম্ল, এবং Al₂O₃ এর সাথে বিক্রিয়া করে লবণ (AlCl₃) ও পানি উৎপন্ন করে।
✅ ২. ক্ষারের সাথে বিক্রিয়া (অ্যাসিডিক আচরণ):
Al₂O₃ আবার অম্লীয় অক্সাইড এর মতো আচরণ করে এবং ক্ষারের সাথে বিক্রিয়া করে।
উদাহরণ:
Al2O3+2NaOH+3H2O→2Na[Al(OH)4]
👉 এখানে NaOH একটি ক্ষার, এবং Al₂O₃ এর সাথে বিক্রিয়া করে একটি জটিল লবণ তৈরি হয় – সোডিয়াম টেট্রাহাইড্রোক্সোঅ্যালুমিনেট।
📌 উপসংহার:
Al₂O₃ হলো একটি উভধর্মী অক্সাইড, কারণ এটি:
অম্লের সাথে বিক্রিয়া করে লবণ ও পানি তৈরি করে,
আবার ক্ষারের সাথেও বিক্রিয়া করে জটিল লবণ গঠন করে।
এই দ্বৈত আচরণই একে উভধর্মী করে তোলে।
এ পৃথিবীর বয়স প্রায় 4.54 বিলিয়ন বছর। আজকে পৃথিবীকে যেমন দেখছো, অনেক অনেক বছর আগে পৃথিবীর রূপ কিন্তু এমন ছিল না। আজ থেকে 500 বা 600 মিলিয়ন বছর আগে এই পৃথিবী ছিল ঘন বনজঙ্গল, নিচু জলাভূমি আর সাগর-মহাসাগরে পরিপূর্ণ। প্রাকৃতিক বিপর্যয়ে ধ্বংসপ্রাপ্ত মৃত প্রাণী, উদ্ভিদ, শৈবাল-ছত্রাক নিচু এলাকাগুলোতে জমা হয়েছিল। তার উপর পড়তে থাকল পলির আস্তরণ। এভাবে মিলিয়ন মিলিয়ন বছর ধরে এ সকল উদ্ভিদ আর প্রাণীর দেহাবশেষের উপর হাজার হাজার ফুট মাটি, বিভিন্ন শিলার আস্তরণ হয়ে গেল। উচ্চচাপ, উচ্চ তাপমাত্রা, মিলিয়ন মিলিয়ন বছর ধরে বিভিন্ন ভৌত আর রাসায়নিক পরিবর্তন ঘটে কয়লা, পেট্রোলিয়াম আর প্রকৃতিক গ্যাস সৃষ্টি হলো৷ এদেরকে বলে জীবাশ্ম জ্বালানি। কয়লার মূল উপাদান কার্বন। আর পেট্রোলিয়ামের মূল উপাদান শুধু কার্বন ও হাইড্রোজেনের দ্বারা সৃষ্ট যৌগ হাইড্রোকার্বন। হাইড্রোকার্বন হলো জৈব যৌগ। অ্যালকোহল, অ্যালডিহাইড, কিটোন, কার্বক্সিলিক এসিডসহ আরও যে সকল জৈব যৌগ আছে তারা মূলত হাইড্রোকার্বন থেকেই সৃষ্ট। এগুলো নিয়েই এ অধ্যায়ে আলোচনা করা হবে।
এ অধ্যায় পাঠ শেষে আমরা
- জীবাশ্ম জ্বালানির ধারণা ব্যাখ্যা করতে পারব।
- পেট্রোলিয়ামকে জৈব যৌগের মিশ্রণ হিসেবে ব্যাখ্যা করতে পারব।
- পেট্রোলিয়ামের ব্যবহার ব্যাখ্যা করতে পারব।
- হাইড্রোকার্বনের ধরন ও শ্রেণিবিভাগ ব্যাখ্যা করতে পারব।
- সম্পৃক্ত ও অসম্পূৰ্ণ হাইড্রোকার্বনের প্রস্তুতির বিক্রিয়া ও ধর্ম ব্যাখ্যা এবং এদের মধ্যে পার্থক্য করতে পারব।
- প্লাস্টিক দ্রব্য ও ভন্ড্রু তৈরির রাসায়নিক বিক্রিয়া এবং এর ব্যবহার বর্ণনা করতে পারব।
- পরিবেশের ওপর প্লাস্টিক দ্রব্য অপব্যবহারের কুফল উল্লেখ করতে পারব।
- প্রাকৃতিক গ্যাস, পেট্রোলিয়াম এবং কয়লা ব্যবহারের সুবিধা, অসুবিধা ও ব্যবহারের কৌশল ব্যাখ্যা করতে পারব।
- হাইড্রোকার্বন থেকে অ্যালকোহল অ্যালডিহাইড ও জৈব এসিডের প্রস্তুতির কৌশল ব্যাখ্যা করতে পারব।
- অ্যালকোহল, অ্যালডিহাইড ও জৈব এসিডের ব্যবহার করতে পারব।
- পরিবেশের উপর প্লাস্টিক দ্রব্যের প্রভাব সম্পর্কিত অনুসন্ধানমূলক কাজ করতে পারব।
- পরীক্ষার মাধ্যমে জৈব ও অজৈব যৌগের মধ্যে পার্থক্য করে দেখাতে পারব।
- জীবাশ্ম জ্বালানির সঠিক ব্যবহার সম্পর্কে সচেতনতা প্রদর্শন করতে পারব।
Related Question
View Allপেট্রোলিয়ামের প্রধান উপাদান হলো হাইড্রোকার্বন।
অ্যালকেনসমূহ কার্বন-কার্বন ও কার্বন-হাইড্রোজেন শক্তিশালী একক সমযোজী বন্ধনের মাধ্যমে গঠিত হয়। এরা রাসায়নিকভাবে আসক্তিহীন বা প্যারাফিন নামে পরিচিত। এ কারণে অ্যালকেনসমূহ সাধারণত রাসায়নিক বিক্রিয়ায় অংশগ্রহণ করে না অর্থাৎ কম সক্রিয় জৈব যৌগ। পক্ষান্তরে অ্যালকিনসমূহের অণুতে কার্বন-কার্বন দ্বি-বন্ধন বিদ্যমান থাকে। কার্বন-কার্বন দ্বি-বন্ধনের প্রথমটি সিগমা বন্ধন হওয়ায় প্রথম বন্ধনটি শক্তিশালী হলেও দ্বিতীয় বন্ধটি পাই (গ) বন্ধন হওয়ায়, তুলনামূলকভাবে দ্বিতীয় বন্ধনটি প্রথম বন্ধন অপেক্ষা দুর্বল হয়। তাই পাই (গ) বন্ধনটির সহজে ভাঙ্গন ঘটে। ফলে এরা সংযোজন, পলিমারকরণ, দহন বিক্রিয়ায় অংশগ্রহণ করে। তাই অ্যালকিন রাসায়নিকভাবে অ্যালকেন অপেক্ষা সক্রিয় হয়।
আলুতে প্রচুর পরিমাণে স্টার্চ আছে। উদ্দীপকে বিদ্যমান বিক্রিয়ার মাধ্যমে স্টার্চ থেকে গ্লুকোজ ও গ্লুকোজকে জাইমেজ এনজাইমের উপস্থিতিতে ইথানলে রূপান্তরিত করা হয়। প্রাপ্ত ইথানলকে এসিডযুক্ত পটাসিয়াম ডাইক্রোমেট অথবা পটাসিয়াম পারম্যাঙ্গানেট দ্বারা জারিত করলে প্রথমে ইথান্যাল (অ্যাসিট্যালডিহাইড) ও পরে ইথানয়িক এসিড উৎপন্ন হয়।
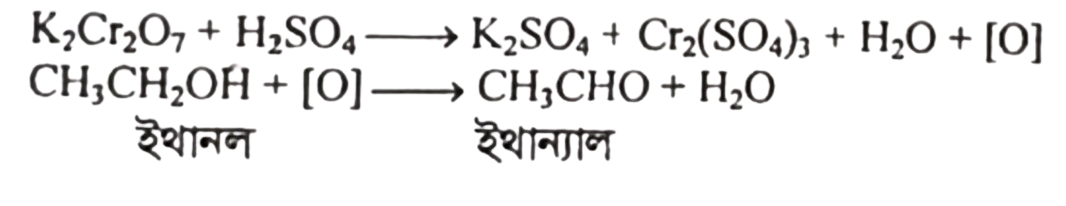
CH3CHO + [O] CH3COOH ইথানয়িক এসিড
এভাবে উৎপন্ন ইথানয়িক এসিডকে NaOH এর সাথে মিশ্রিত করলে সোডিয়াম ইথানয়েট উৎপন্ন হয়।
CH3COOH + NaOH → CH3COONa + H2O সোডিয়াম ইথানয়েট
এখানে প্রাপ্ত সোডিয়াম ইথানয়েটকে (CH3COONa) সোডালাইম (NaOH + CaO এর মিশ্রণ) সহ উত্তপ্ত করলে মিথেন (CH4) পাওয়া যায়।
বিক্রিয়া: CH3COONa CH4 + Na2CO3
এভাবে আমরা আলু থেকে মিথেন (CH4) প্রস্তুত করতে পারি।
আলুতে প্রচুর পরিমাণ স্টার্চ থাকে। অতিরিক্ত আলুতে বিদ্যমান স্টার্চ থেকে আমরা নিম্নলিখিত উপায়ে ইথানল প্রস্তুত করতে পারি যা বিকল্প জ্বালানি হিসেবে ব্যবহার করা যায়।
আলুকে প্রথমে সিদ্ধ করে কাই (Paste) এ পরিণত করা হয়। একে ম্যাস (mash) বলে। এ ম্যাসের সাথে মল্ট মিশ্রিত করে মিশ্রণটি প্রায় 45°C তাপমাত্রায় এক ঘন্টা রেখে দিলে মল্ট থেকে নিঃসৃত "ডায়াস্টেজ” নামক এক প্রকার এনজাইম দ্বারা স্টার্চ আর্দ্র বিশ্লেষিত হয়ে মল্টোজে পরিণত হয়।
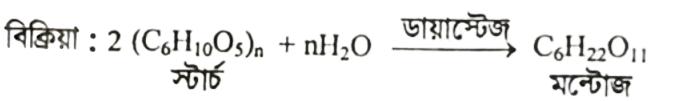
মল্টোজকে 20°C তাপমাত্রায় শীতল করে পানিযোগে লঘু (10%) করে ইস্ট যোগ করলে, ইস্ট থেকে নিঃসৃত ম্যালটেজ এনজাইম মল্টোজকে গ্লুকোজে এবং পরবর্তীতে জাইমেজ নামক এনজাইম গ্লুকোজকে ফারমেন্টেশন করে ইথানলে পরিণত করে।
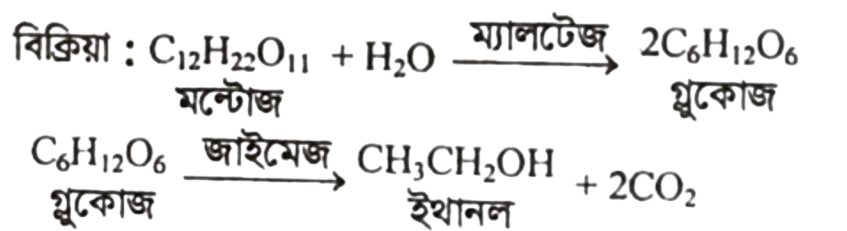
আলু থেকে এভাবে প্রাপ্ত ইথানল পৃথিবীর বিভিন্ন দেশে জীবাশ্ম জ্বালানির পরিবর্তে মটর ইঞ্জিন, বিমান, বাস, ট্রাক, কলকারখানায় বিকল্প জ্বালানিরূপে ব্যবহার করা হচ্ছে। পেট্রোলের সাথে (10-20%) ইথানল মিশ্রিত করে গ্যাসহোল (Gasohol) নামক জ্বালানি তৈরী করা হয়েছে, যা বিভিন্ন দেশে জ্বালানিরূপে ব্যবহৃত হয়ে আসছে।
CH3CH2OH + O2 → 2CO2 + 6H2O + তাপশক্তি
যেহেতু অ্যালকোহল থেকে আমরা প্রচুর পরিমাণ তাপশক্তি পাই, তাই অতিরিক্ত আলু থেকে ইথানল উৎপন্ন করে জীবাশ্ম জ্বালানির বিকল্প হিসেবে ব্যবহার সম্ভব।
হাইড্রোজেন ও কার্বন দ্বারা গঠিত দ্বি-মৌল যৌগসমূহকে হাইড্রোকার্বন বলা হয়।
অ্যারোমেটিক যৌগগুলোতে সাধারণত 5, 6 কিংবা 7 সদস্যের সমতলীয় যৌগ এবং এগুলোতে একান্তর দ্বিবন্ধন থাকে। বেনজিন ছয় সদস্যের সমতলীয় চাক্রিক যৌগ। এতে একান্তর দ্বিবন্ধন বিদ্যমান। অর্থাৎ পর্যায়ক্রমে কার্বন-কার্বন একটি একক বন্ধন এবং একটি দ্বিবন্ধন থাকে। তাই
বেনজিন  একটি অ্যারোমেটিক হাইড্রোকার্বন।
একটি অ্যারোমেটিক হাইড্রোকার্বন।
১ ক্লিকে প্রশ্ন, শীট, সাজেশন ও
অনলাইন পরীক্ষা তৈরির সফটওয়্যার!
শুধু প্রশ্ন সিলেক্ট করুন — প্রশ্নপত্র অটোমেটিক তৈরি!



