পদার্থ (Matter)
যার ভর আছে, যা কোনো স্থান দখল করে অবস্থান করে, তাকে পদার্থ বলা হয়।
বৈশিষ্ট্য | পদার্থ | শক্তি |
| ভর | ভর আছে | ভর নাই |
| স্থান দখল | করে | করে না |
| উদাহরণ | বাতাস, পানি | তাপ, আলোক, বিদ্যুৎ |
# বহুনির্বাচনী প্রশ্ন
শিকাগো আর্ট মিউজিয়াম
প্যারিস মিউজিয়াম
ব্রিটিশ মিউজিয়াম
কায়রো মিউজিয়াম
পদার্থ ও শক্তি (Matter and Energy) প্রকৃতিতে দুটি ভিন্ন বিষয়ের অস্তিত্ব আমরা বুঝতে পারি একটি জড় বা পদার্থ (matter) এবং অন্যটি হল শক্তি (energy) ।
পদার্থ (Matter) : যা ইন্দ্রিয় গ্রাহ্য, যা কিছুটা স্থান দখল করে, যার ওজন আছে এবং বলপ্রয়োগের সাহায্যে যার স্থির বা গতিশীল অবস্থার পরিবর্তন করা যায়, তাকেই পদার্থ বলে । যেমন চেয়ার, টেবিল, ইট, বালি, খাতা, পেন্সিল ইত্যাদি । পদার্থের নির্দিষ্ট পরিমাণকে বস্তু বলে । যেমন প্লাস্টিক দিয়ে জলের বালতি, মগ তৈরি করা হয় সুতরাং জলের বালতি, মগ হল বস্তু কিন্তু এগুলির উপাদান প্লাস্টিক হল পদার্থ অর্থাৎ বস্তু যে উপাদানে তৈরি হয় তাকে জড় বা পদার্থ বলে । পৃথিবীতে জড়বস্তু এবং সজীব বস্তু এই দুই ধরনের বস্তু আমরা দেখতে পাই ।
ভর এবং ভার বা ওজন : বস্তুর ভার বা ওজন নির্ণয় : ভরের নিত্যতা সূত্র বা পদার্থের অবিনাশিতা সূত্র : শক্তির বিভিন্ন রূপ : শক্তির নিত্যতা সূত্র : শক্তির রূপান্তর : সূর্যই পৃথিবীর শক্তির প্রধান উৎস
# বহুনির্বাচনী প্রশ্ন
পদার্থের অবস্থাভেদ
States of Matter
পদার্থ সাধারণত ৩টি অবস্থায় থাকতে পারে। যথা: কঠিন, তরল এবং বায়বীয়
| কঠিন পদার্থ | কঠিন পদার্থের নির্দিষ্ট আয়তন ও নির্দিষ্ট আকার এবং দৃঢ়তা আছে। এর অণুসমূহ পরস্পরের অতি সন্নিকটে অবস্থান করে। যেমন: বালু, পাথর, লবণ ইত্যাদি। |
| তরল পদার্থ | তরল পদার্থের নির্দিষ্ট আয়তন আছে কিন্তু নির্দিষ্ট আকার নেই। তরল পদার্থের অণুসমূহ পরস্পরের সন্নিকটে থাকে, তবে তাদের মধ্যকার আকর্ষণ কঠিন পদার্থের মত প্রবল নয়। উদাহরণ: পানি, পেট্রোল, কেরোসিন, ভোজ্য তেল প্রভৃতি। |
| গ্যাসীয় পদার্থ | গ্যাসীয় পদার্থের নির্দিষ্ট আয়তন ও নির্দিষ্ট আকার নেই। গ্যাসীয় পদার্থের অণুসমূহের দূরত্ব অনেক বেশি, তাই আকর্ষণ শক্তি অনেক কম। ফলে তারা প্রায় সম্পূর্ণ মুক্তভাবে চলাচল করে। উদাহরণ: নাইট্রোজেন, অক্সিজেন, মিথেন ইত্যাদি। |
তাপ পদার্থের তিন অবস্থায় রূপান্তরের প্রধান কারণ। পানি একমাত্র পদার্থ যা প্রকৃতিতে কঠিন (বরফ), তরল (পানি) এবং বায়বীয় (জলীয় বাষ্প) তিন অবস্থাতেই পাওয়া যায়।
কঠিন | তরল | বায়বীয় |
| মেরু অঞ্চল বা পর্বত শীর্ষের বরফ | নদী, সমুদ্রের পানি | বায়ুর জলীয় বাষ্প |
# বহুনির্বাচনী প্রশ্ন
গলনাংক (Melting point)
যে তাপমাত্রায় কঠিন হতে তরল পদার্থের সৃষ্টি হয়, তাকে সে পদার্থের গলনাংক বলে। পানির গলনাংক ০° সেন্টিগ্রেড।
# বহুনির্বাচনী প্রশ্ন
০ ডিগ্রি
৯৯-৯৮ ডিগ্রি
৪ ডিগ্রি
১০০ ডিগ্রি
স্ফুটনাংক (Boiling Point)
যে তাপমাত্রায় কোন তরল পদার্থ ফুটতে থাকে, তাকে সে পদার্থের স্ফুটনাংক বলে। পানির স্ফুটনাংক ১০০ ডিগ্রী সেন্টিগ্রেড।
# বহুনির্বাচনী প্রশ্ন
ঊর্ধ্বপাতন (Sublimation)
কোনো কোনো ক্ষেত্রে কঠিন পদার্থকে উত্তপ্ত করলে তা তরলে রূপান্তরিত না হয়ে সরাসরি বাষ্পে রূপান্তরিত হয়, তাকে ঊর্ধ্বপাতন বলা হয়। যেমন: কপূর, গন্ধক, আয়োডিন, ন্যাপথালিন, অ্যামোনিয়াম ক্লোরাইড, কার্বন ডাই অক্সাইড, আর্সেনিক, বেনজোয়িক এসিড ইত্যাদি।
# বহুনির্বাচনী প্রশ্ন
পদার্থের শ্রেণিবিভাগ:
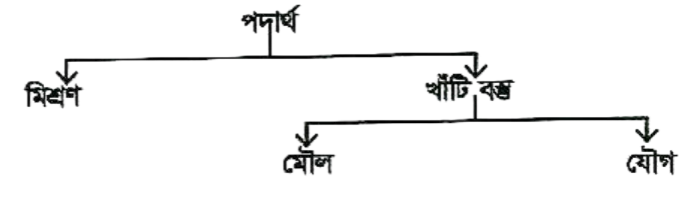
মিশ্রণ (Mixture)
দুই বা ততোধিক পদার্থকে যে কোন অনুপাতে একত্রে মিশালে যদি তারা নিজ নিজ ধর্ম বজায় রেখে পাশাপাশি অবস্থান করে, তবে উক্ত সমাবেশকে মিশ্রণ বলা হয়। বায়ু একটি মিশ্র পদার্থ কারণ বায়ুতে উপাদান মৌলসমূহ যেমন: নাইট্রোজেন, অক্সিজেন, কার্বন-ডাই-অক্সাইড ইত্যাদি নিজ নিজ ধর্ম বজায় রেখে পাশাপাশি অবস্থান করে।
খাঁটি বস্তু (Pure substance)
মৌল বা মৌলিক পদার্থ (Elements)
| সবচেয়ে হালকা মৌল | হাইড্রোজেন (H) |
| সবচেয়ে হালকা মৌলিক গ্যাস | হাইড্রোজেন (H) |
| সবচেয়ে ভারী মৌলিক গ্যাস | রেডন (Rn) |
যে বস্তুকে রাসায়নিকভাবে বিশ্লেষণ করে অন্য কোন সহজ বস্তুতে রূপান্তরিত করা যায় না, তাকে মৌল বা মৌলিক পদার্থ বলা হয়। যেমন: হাইড্রোজেন, নাইট্রোজেন, অক্সিজেন, সোনা, তামা, লোহা ইত্যাদি। পৃথিবীতে বর্তমানে মৌলিক পদার্থের সংখ্যা ১১৮। এদের মধ্যে ৯৮টি মৌল প্রকৃতিতে পাওয়া যায়। কৃত্রিম উপায়ে প্রাপ্ত মৌলিক পদার্থের সংখ্যা ২০।
যৌগ বা যৌগিক পদার্থ (Compound)
যে বস্তুকে রাসায়নিকভাবে বিশ্লেষণ করলে দুই বা ততোধিক মৌলিক পদার্থ পাওয়া যায়, তাকে যৌগ বা যৌগিক পদার্থ বলা হয়। যেমন: হাইড্রোজেন ও অক্সিজেন এ দুইটি মৌল নির্দিষ্ট ভর অনুপাতে পরস্পর যুক্ত হয়ে পানি উৎপন্ন করে। অতএব পানি একটি যৌগিক পদার্থ।
# বহুনির্বাচনী প্রশ্ন
গ্লিসারিন
ফিটকিরি
ক্যালসিয়াম কার্বনেট
সোডিয়াম ক্লোরাইড
পদার্থের পরিবর্তন (Changes in matter)
পদার্থের পরিবর্তন দুই ধরনের। যথা: ভৌত বা অবস্থানগত পরিবর্তন এবং রাসায়নিক পরিবর্তন।
ভৌত বা অবস্থানগত পরিবর্তন (Physical Change)
যে পরিবর্তনের ফলে পদার্থের শুধু বাহ্যিক আকার বা অবস্থার পরিবর্তন হয় কিন্তু নতুন কোনো পদার্থে পরিণত হয় না, তাকে ভৌত বা অবস্থানগত পরিবর্তন বলে।
ভৌত পরিবর্তনের উদাহরণ :
➺ পানিকে ঠাণ্ডা করে বরফে এবং তাপ দিয়ে জলীয় বাষ্পে পরিণত করা।
➺ একটি লোহার টুকরাকে চুম্বক দ্বারা ঘর্ষণ করে চুম্বকে পরিণত করা।
➺ তাপ দিয়ে মোম গলানো।
রাসায়নিক পরিবর্তন : যে পরিবর্তনের ফলে এক বা একাধিক বস্তু প্রত্যেকে তার নিজস্ব সত্তা হারিয়ে সম্পূর্ণ নতুন ধর্ম বিশিষ্ট এক বা একাধিক নতুন বস্তুতে পরিণত হয়, তাকে রাসায়নিক পরিবর্তন বলে।
রাসায়নিক পরিবর্তনের উদাহরণ :
➺ লোহায় মরিচা ধরা। মরিচা (Rust) হলো আর্দ্র ফেরিক অক্সাইড (Fe2O3. nH2O)। লোহায় মরিচা ধরার জন্য পানি এবং অক্সিজেন প্রয়োজন।
➺ দুধকে ছানায় পরিণত করা
➺ চাল সিদ্ধ করলে ভাতে পরিণত হয়।
➺ দিয়াশলাইয়ের কাঠি জ্বালানো
# বহুনির্বাচনী প্রশ্ন
দহন তাপ
বিক্রিয়া তাপ
সংঘটন তাপ
দ্রবণ তাপ
Read more







