উদ্দীপকে বিদ্যমান প্রথম বিক্রিয়ক গ্যাসটি মিথেন (CH4)। মিথেনের ব্যবহারসমূহ নিম্নে আলোচনা করা হলো-
i. মিথেনে (CH4) বিদ্যমান কার্বন ও হাইড্রোজেন উভয়ই দাহ্য পদার্থ। মিথেনকে বায়ুর উপস্থিতিতে দহন করলে CO2, H2O ও প্রচুর পরিমাণ তাপশক্তি উৎপন্ন হয়, যা জ্বালানি হিসাবে ব্যবহার করা হয়।
CH4 + 2O2 = CO2(s) + 2H2O(g) + তাপশক্তি
ii. মিথেন (CH4) মৃদু সূর্যালোকের (UV) উপস্থিতিতে বিক্রিয়া করে মিথাইল ক্লোরাইড CH2Cl2, ডাইক্লোরোমিথেন CH2Cl2, ক্লোরোফরম CHCI3 ও কার্বন টেট্টা ক্লোরাইড CCI4 উৎপন্ন করে।
উৎপন্ন মিথাইল ক্লোরাইড (CH3CI) শিল্পক্ষেত্রে অ্যালকোহল, অ্যালডিহাইড, জৈব এসিড প্রস্তুতিতে ব্যবহার করা হয়। ডাইক্লোরোমিথেন (CH2Cl2) ইমালশন রং শিল্পে দ্রাবক হিসাবে, ক্লোরোফরম (CHCl3) কে চেতনানাশক হিসেবে এবং কার্বন টেট্রাক্লোরাইড (CCl4) কে ড্রাইওয়াশের দ্রাবক হিসাবে ও অগ্নিনির্বাপক পদার্থ হিসাবে ব্যবহার করা হয়।
iii. মিথেনকে (CH4) উচ্চ চাপে ও 900°C তাপমাত্রায় নিকেল প্রভাবকের উপর দিয়ে চালনা করলে সংশ্লেষ গ্যাস উৎপন্ন হয়। বিক্রিয়া: CH4

iv. সংশ্লেষ গ্যাসকে 400°C তাপমাত্রা, 200-300 বায়ুচাপে ZnO + Cr2O, প্রভাবকের উপর দিয়ে চালনা করলে মিথানল উৎপন্ন হয়, যা বিভিন্ন বিক্রিয়ায় দ্রাবক হিসাবে ব্যবহার করা হয়।
বিক্রিয়া: CO(s) + H2(s) CH3OH
V. মিথানলকে (CH3OH) বাতাসের অক্সিজেন দ্বারা জারিত করলে ফরমালডিহাইড উৎপন্ন হয়।
CH2OH + O2 HCHO
এভাবে উৎপন্ন ফরমালডিহাইডের (30-40%) জলীয় দ্রবণকে ফরমালিন বলা হয়। ফরমালিন জীবাণুনাশক, কোন কিছুর পচন রোধ করার জন্য বা জীববিজ্ঞানের নমুনা সংরক্ষণে ব্যাপকভাবে ব্যবহৃত হয়।
vi. ফরমালডিহাইড, অ্যামোনিয়ার সাথে বিক্রিয়া করে হেক্সামিন তৈরি করে, যা মূত্রাশয়ের অসুখ ও বাত জ্বরের ঔষধ হিসাবে ব্যবহার করা হয়।
বিক্রিয়া: 6HCHO+4NH3 (CH2)6N4 (হেক্সামিন)
vii. ফরমালডিহাইডের জলীয় দ্রবণকে নিম্নচাপে উত্তপ্ত করলে ডেলরিন নামক শক্ত পলিমার গঠিত হয়, যা শক্ত প্লাস্টিক হিসাবে দরজা, বালতি, চেয়ার প্রভৃতি তৈরীতে ব্যবহৃত হয়।
বিক্রিয়া: nHCHO(CH2O)n
অতএব, উপরিউক্ত আলোচনা থেকে আমরা বলতে পারি, উদ্দীপকের প্রথম বিক্রিয়ক গ্যাসটির (CH4) বহুমুখী ব্যবহার রয়েছে।
Related Question
View Allপেট্রোলিয়ামের প্রধান উপাদান হলো হাইড্রোকার্বন।
অ্যালকেনসমূহ কার্বন-কার্বন ও কার্বন-হাইড্রোজেন শক্তিশালী একক সমযোজী বন্ধনের মাধ্যমে গঠিত হয়। এরা রাসায়নিকভাবে আসক্তিহীন বা প্যারাফিন নামে পরিচিত। এ কারণে অ্যালকেনসমূহ সাধারণত রাসায়নিক বিক্রিয়ায় অংশগ্রহণ করে না অর্থাৎ কম সক্রিয় জৈব যৌগ। পক্ষান্তরে অ্যালকিনসমূহের অণুতে কার্বন-কার্বন দ্বি-বন্ধন বিদ্যমান থাকে। কার্বন-কার্বন দ্বি-বন্ধনের প্রথমটি সিগমা বন্ধন হওয়ায় প্রথম বন্ধনটি শক্তিশালী হলেও দ্বিতীয় বন্ধটি পাই (গ) বন্ধন হওয়ায়, তুলনামূলকভাবে দ্বিতীয় বন্ধনটি প্রথম বন্ধন অপেক্ষা দুর্বল হয়। তাই পাই (গ) বন্ধনটির সহজে ভাঙ্গন ঘটে। ফলে এরা সংযোজন, পলিমারকরণ, দহন বিক্রিয়ায় অংশগ্রহণ করে। তাই অ্যালকিন রাসায়নিকভাবে অ্যালকেন অপেক্ষা সক্রিয় হয়।
আলুতে প্রচুর পরিমাণে স্টার্চ আছে। উদ্দীপকে বিদ্যমান বিক্রিয়ার মাধ্যমে স্টার্চ থেকে গ্লুকোজ ও গ্লুকোজকে জাইমেজ এনজাইমের উপস্থিতিতে ইথানলে রূপান্তরিত করা হয়। প্রাপ্ত ইথানলকে এসিডযুক্ত পটাসিয়াম ডাইক্রোমেট অথবা পটাসিয়াম পারম্যাঙ্গানেট দ্বারা জারিত করলে প্রথমে ইথান্যাল (অ্যাসিট্যালডিহাইড) ও পরে ইথানয়িক এসিড উৎপন্ন হয়।
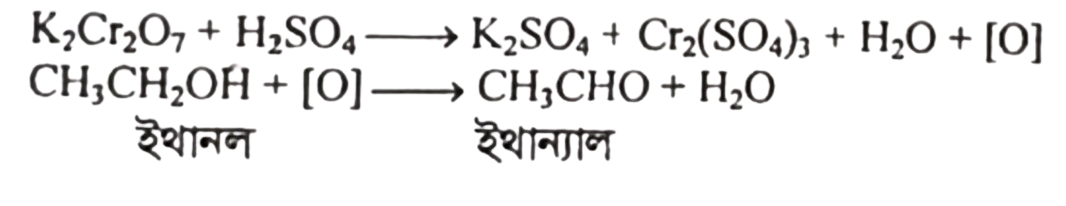
CH3CHO + [O] CH3COOH ইথানয়িক এসিড
এভাবে উৎপন্ন ইথানয়িক এসিডকে NaOH এর সাথে মিশ্রিত করলে সোডিয়াম ইথানয়েট উৎপন্ন হয়।
CH3COOH + NaOH → CH3COONa + H2O সোডিয়াম ইথানয়েট
এখানে প্রাপ্ত সোডিয়াম ইথানয়েটকে (CH3COONa) সোডালাইম (NaOH + CaO এর মিশ্রণ) সহ উত্তপ্ত করলে মিথেন (CH4) পাওয়া যায়।
বিক্রিয়া: CH3COONa CH4 + Na2CO3
এভাবে আমরা আলু থেকে মিথেন (CH4) প্রস্তুত করতে পারি।
আলুতে প্রচুর পরিমাণ স্টার্চ থাকে। অতিরিক্ত আলুতে বিদ্যমান স্টার্চ থেকে আমরা নিম্নলিখিত উপায়ে ইথানল প্রস্তুত করতে পারি যা বিকল্প জ্বালানি হিসেবে ব্যবহার করা যায়।
আলুকে প্রথমে সিদ্ধ করে কাই (Paste) এ পরিণত করা হয়। একে ম্যাস (mash) বলে। এ ম্যাসের সাথে মল্ট মিশ্রিত করে মিশ্রণটি প্রায় 45°C তাপমাত্রায় এক ঘন্টা রেখে দিলে মল্ট থেকে নিঃসৃত "ডায়াস্টেজ” নামক এক প্রকার এনজাইম দ্বারা স্টার্চ আর্দ্র বিশ্লেষিত হয়ে মল্টোজে পরিণত হয়।
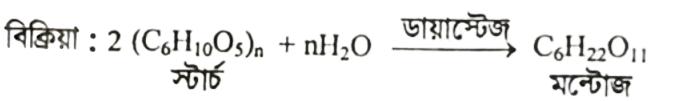
মল্টোজকে 20°C তাপমাত্রায় শীতল করে পানিযোগে লঘু (10%) করে ইস্ট যোগ করলে, ইস্ট থেকে নিঃসৃত ম্যালটেজ এনজাইম মল্টোজকে গ্লুকোজে এবং পরবর্তীতে জাইমেজ নামক এনজাইম গ্লুকোজকে ফারমেন্টেশন করে ইথানলে পরিণত করে।
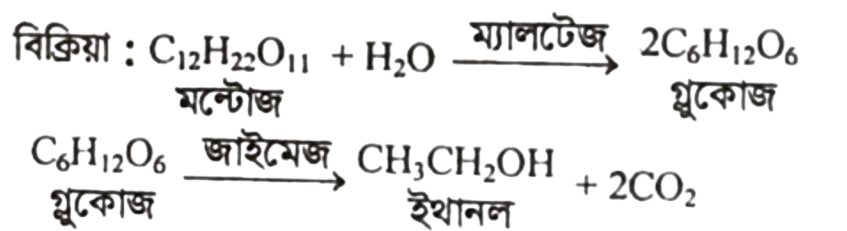
আলু থেকে এভাবে প্রাপ্ত ইথানল পৃথিবীর বিভিন্ন দেশে জীবাশ্ম জ্বালানির পরিবর্তে মটর ইঞ্জিন, বিমান, বাস, ট্রাক, কলকারখানায় বিকল্প জ্বালানিরূপে ব্যবহার করা হচ্ছে। পেট্রোলের সাথে (10-20%) ইথানল মিশ্রিত করে গ্যাসহোল (Gasohol) নামক জ্বালানি তৈরী করা হয়েছে, যা বিভিন্ন দেশে জ্বালানিরূপে ব্যবহৃত হয়ে আসছে।
CH3CH2OH + O2 → 2CO2 + 6H2O + তাপশক্তি
যেহেতু অ্যালকোহল থেকে আমরা প্রচুর পরিমাণ তাপশক্তি পাই, তাই অতিরিক্ত আলু থেকে ইথানল উৎপন্ন করে জীবাশ্ম জ্বালানির বিকল্প হিসেবে ব্যবহার সম্ভব।
হাইড্রোজেন ও কার্বন দ্বারা গঠিত দ্বি-মৌল যৌগসমূহকে হাইড্রোকার্বন বলা হয়।
অ্যারোমেটিক যৌগগুলোতে সাধারণত 5, 6 কিংবা 7 সদস্যের সমতলীয় যৌগ এবং এগুলোতে একান্তর দ্বিবন্ধন থাকে। বেনজিন ছয় সদস্যের সমতলীয় চাক্রিক যৌগ। এতে একান্তর দ্বিবন্ধন বিদ্যমান। অর্থাৎ পর্যায়ক্রমে কার্বন-কার্বন একটি একক বন্ধন এবং একটি দ্বিবন্ধন থাকে। তাই
বেনজিন  একটি অ্যারোমেটিক হাইড্রোকার্বন।
একটি অ্যারোমেটিক হাইড্রোকার্বন।
১ ক্লিকে প্রশ্ন, শীট, সাজেশন ও
অনলাইন পরীক্ষা তৈরির সফটওয়্যার!
শুধু প্রশ্ন সিলেক্ট করুন — প্রশ্নপত্র অটোমেটিক তৈরি!



