পরমাণু হলো ইলেকট্রন, প্রোটন ও নিউট্রন মৌলিক কণিকা দ্বারা গঠিত অতি ক্ষুদ্র কণা।
O এবং O2 এর মধ্যে পার্থক্য নিচে দেখানো হলো-
| O2 | |
| ১. O হচ্ছে অক্সিজেনের একটি পরমাণু। | ১. O2 হচ্ছে অক্সিজেনের একটি অণু, যা দুটি পরমাণুর সমন্বয়ে গঠিত। |
| ২. O সরাসরি রাসায়নিক বিক্রিয়ায় অংশগ্রহণ করতে পারে। | ২. O2 সরাসরি রাসায়নিক বিক্রিয়ায় অংশগ্রহণ করতে পারে না। |
উদ্দীপকের চিত্রে, পরমাণুটির নিউক্লিয়াসে প্রোটন সংখ্যা এটি। তাই মৌলটির ইলেকট্রন সংখ্যাও হবে 6টি। প্রথম কক্ষপথে ২টি ইলেকট্রন থাকলে দ্বিতীয় কক্ষপথে ইলেকট্রন থাকবে (6 – 2টি) = 4 টি। দ্বিতীয় কক্ষপথে যে কয়টি ইলেকট্রন থাকবে তা বসিয়ে পাশে চিত্রটি আঁকা হলো-
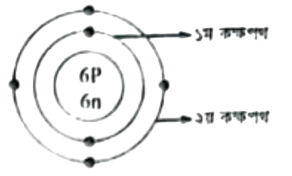
আমার আঁকা চিত্রটির সপক্ষে যুক্তি নিচে দেখানো হলো-
১. পরমাণুর নিউক্লিয়াসে যতটি প্রোটন থাকে, তার সমান সংখ্যক ইলেকট্রন থাকে। যেহেতু পরমাণুটিতে 6টি প্রোটন রয়েছে, তাই ইলেকট্রন সংখ্যাও হবে 6।
২. পরমাণুর কক্ষপথে বা শক্তিস্তরে ইলেকট্রনসমূহ 2n² সূত্র অনুসরণ করে বিন্যস্ত থাকে, যেখানে n = শক্তিস্তর বা কক্ষপথ সংখ্যা। সে হিসাবে প্রথম শক্তিস্তরে 2 (দুই) টি এবং দ্বিতীয় শক্তিস্তরে 2 22 বা ৪ (আট) টি ইলেকট্রন থাকার কথা। যেহেতু এখানে মোট ইলেকট্রন সংখ্যা 6 এবং প্রথম কক্ষপথে ২টি ইলেকট্রন রয়েছে, তাই দ্বিতীয় কক্ষপথে ইলেকট্রন থাকবে = (6-2) টি বা 4টি।
৩. প্রোটন ধনাত্মক চার্জযুক্ত এবং ইলেকট্রন ঋণাত্মক চার্জযুক্ত। এক্ষেত্রে প্রোটন ও ইলেকট্রন সংখ্যা সমান হওয়ায় পরমাণুর নিউক্লিয়াস চার্জ নিরপেক্ষ।
৪. মৌলটির ভরসংখ্যা = প্রোটন সংখ্যা + নিউট্রন সংখ্যা = 6+6=12
Related Question
View Allকার্বন একটি মৌলিক পদার্থ। যেহেতু কার্বনকে ভাঙলে বা বিশ্লেষণ করলে কার্বন ব্যতীত অন্য কোনো পদার্থ পাওয়া যায় না, তাই কার্বন একটি মৌলিক পদার্থ।
উদ্দীপকের ১ নং পদার্থটির রাসায়নিক নাম সোডিয়াম ক্লোরাইড। এটি খাবার লবণ নামেও পরিচিত। এর সংকেত: NaCl.
গঠন প্রক্রিয়া: সোডিয়াম ক্লোরাইড (NaCl) একটি যৌগিক পদার্থ। এটি দুটি মৌলিক পদার্থ সোডিয়াম (Na) ও ক্লোরিন (CI) দ্বারা গঠিত। সংকেত থেকে দেখা যায় যে, সোডিয়াম ক্লোরাইড যৌগটি একটি Na ও একটি CI পরমাণু দ্বারা গঠিত। অর্থাৎ NaCl কে রাসায়নিকভাবে বিশ্লেষণ করলে একটি সোডিয়াম ও একটি ক্লোরিন পরমাণু পাওয়া যাবে। আবার বলা যায় যে, একটি সোডিয়াম পরমাণু ও একটি ক্লোরিন পরমাণু মিলে একটি সোডিয়াম ক্লোরাইড অণু গঠন করে। অর্থাৎ সোডিয়াম ক্লোরাইডের একটি অণুতে মোট দুটি পরমাণু রয়েছে।
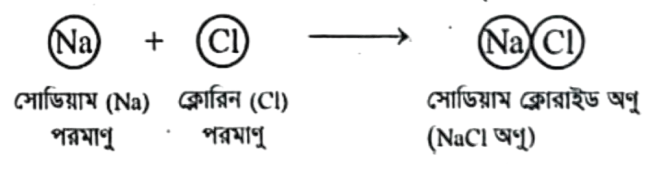
ছকের ২নং পদার্থটি (ফ্লোরিন) মৌলিক অণু। অর্থাৎ ফ্লোরিন মৌলিক পদার্থ। কারণ ফ্লোরিন কে ভাঙলে বা বিশ্লেষণ করলে ফ্লোরিন ব্যতীত অন্য কোনো পদার্থ পাওয়া যায় না।
এক্ষেত্রে ২টি ফ্লোরিন পরমাণু মিলে ফ্লোরিন অণু গঠিত হয়।
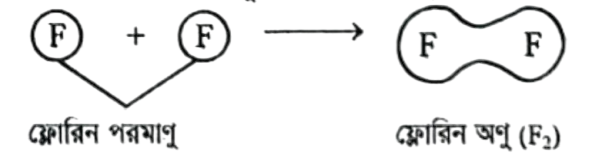
আবার ছকের ৩নং পদার্থটি ১টি C (কার্বন) ও ২টি O (অক্সিজেন) পরমাণু দ্বারা গঠিত একটি যৌগিক পদার্থ (কার্বন ডাইঅক্সাইড)। উৎপন্ন এর ধর্ম C ও O পরমাণু থেকে ভিন্ন। আবার যৌগটিকে ভাঙলে বা বিশ্লেষণ করলে দুটি অক্সিজেন পরমাণু এবং একটি কার্বন পরমাণু পাওয়া যায়। জানা আছে, যে পদার্থকে ভাঙলে বা বিশ্লেষণ করলে একাধিক ভিন্নধর্মী মৌল পাওয়া যায় সেই পদার্থটি যৌগিক পদার্থ। তাই (কার্বন ডাইঅক্সাইড) একটি যৌগিক পদার্থ।
পরমাণু হলো ইলেকট্রন, প্রোটন ও নিউট্রন মৌলিক কণিকা দ্বারা গঠিত অতি ক্ষুদ্র কণা।
O এবং O2 এর মধ্যে পার্থক্য নিচে দেখানো হলো-
| O2 | |
| ১. O হচ্ছে অক্সিজেনের একটি পরমাণু। | ১. O2 হচ্ছে অক্সিজেনের একটি অণু, যা দুটি পরমাণুর সমন্বয়ে গঠিত। |
| ২. O সরাসরি রাসায়নিক বিক্রিয়ায় অংশগ্রহণ করতে পারে। | ২. O2 সরাসরি রাসায়নিক বিক্রিয়ায় অংশগ্রহণ করতে পারে না। |
১ ক্লিকে প্রশ্ন, শীট, সাজেশন ও
অনলাইন পরীক্ষা তৈরির সফটওয়্যার!
শুধু প্রশ্ন সিলেক্ট করুন — প্রশ্নপত্র অটোমেটিক তৈরি!




