শত শত মিলিয়ন বছর আগের প্রাণী এবং উদ্ভিদ দেহের ধ্বংসাবশেষ মাটির নিচে কয়লা, প্রাকৃতিক গ্যাস ও পেট্রোলিয়াম ইত্যাদি জীবাশ্মরূপে পাওয়া গেছে, যা জ্বালানি হিসেবে ব্যবহার করা হয় একেই জীবাশ্ম জ্বালানি বলা হয়। অর্থাৎ, কয়লা, প্রাকৃতিক গ্যাস ও পেট্রোলিয়াম ইত্যাদি হচ্ছে জীবাশ্ম জ্বালানির উদাহরণ।
বিভিন্ন সময় বড় বড় প্রাকৃতিক বিপর্যয়ে বিভিন্ন ধরনের উদ্ভিদ ও প্রাণী মাটিচাপা পড়ে যায়। সময়ের বিবর্তনে তার উপর আরও মাটি পড়ে এক সময় তা মাটির গভীর থেকে আরো গভীরে চলে যায়। ফলে এর উপর চাপ ও তাপমাত্রা বাড়তে থাকে। বায়ুর অনুপস্থিতিতে -এগুলোর ক্ষয় ও রাসায়নিক পরিবর্তন ঘটতে থাকে। শত শত মিলিয়ন বছর ধরে এ পরিবর্তনের কারণে বড় থেকে ছোট সব ধরনের উদ্ভিদ-প্রাণী থেকে জীবাশ্ম জ্বালানির সৃষ্টি হয়েছে।
বহু প্রাচীনকালের উদ্ভিদ এবং প্রাণীর মৃতদেহের যে ধ্বংসাবশেষ মাটির নিচে পাওয়া যায় তাকে জীবাশ্ম বলে। মাটির নিচে বায়ুর অনুপস্থিতিতে শত শত মিলিয়ন বছর ধরে তাপ ও চাপের প্রভাবে ফাইটোপ্লাংকটন, জুওপ্লাংকটন ও, মৃত প্রাণীর দেহাবশেষ থেকে পেট্রোলিয়ামের সৃষ্টি হয় এবং এটি জ্বালানির কাজে ব্যবহার করা হয় বলে একে জীবাশ্ম জ্বালানি বলে।
প্রাকৃতিক গ্যাসে বিভিন্ন উপাদানের শতকরা সংযুক্তি হলো-প্রধান উপাদান, মিথেন
ইথেন → 7%
প্রোপেন 6%
বিউটেন ও আইসোবিউটেন → 4%
পেন্টেন → 3%
কিন্তু বাংলাদেশে এ পর্যন্ত যে প্রাকৃতিক গ্যাস পাওয়া গেছে, তাতে মিথেন ( ৯৫-৯৯)%।
যে পেট্রোলিয়াম খনি থেকে সরাসরি পাওয়া যায়, তাকে বলা হয় অপরিশোধিত তেল (Crude oil)। এই অপরিশোধিত' তেল অস্বচ্ছ। এতে কখনো কখনো সালফারের কিছু কিছু যৌগ থাকার কারণে দুর্গন্ধযুক্ত হয়। এই পেট্রোলিয়াম মূলত বিভিন্ন হাইড্রোকার্বনের মিশ্রণ এবং একে সরাসরি ব্যবহার করা যায় না।
পেট্রোলিয়াম তথা অপরিশোধিত তেল মূলত বিভিন্ন হাইড্রোকার্বন এর মিশ্রণ। কারণ এতে বিভিন্ন জীবাশ্ম জ্বালানি যেমন পেট্রোলিয়াম গ্যাস, গ্যাসোলিন, কেরোসিন, লুব্রিকেটিং তেল, জ্বালানি তেল ও মিশ্রিত থাকে। অর্থাৎ এতে মিথেন, ইথেন, প্রোপেন, অ্যালকেন, অ্যালকিন, অ্যালকাইন ইত্যাদি হাইড্রোকার্বন মিশ্রিত থাকে। আংশিক পাতন প্রক্রিয়ায় এ উপাদানসমূহ পৃথক করে ব্যবহার উপযোগী করা হয়।
অপরিশোধিত তেল বিভিন্ন হাইড্রোকার্বনের মিশ্রণ। এ অপরিশোধিত তেল অস্বচ্ছ এবং সরাসরি ব্যবহার উপযোগী নয়। কিন্তু একে যদি আংশিক পাতনের সাহায্যে পৃথক করা হয়, তবে এ অপরিশোধিত তেল থেকে পেট্রোল গ্যাস, পেট্রোলিয়াম, ন্যাপথা, কেরোসিন, ডিজেল, পিচ প্রভৃতি অংশে বিভক্ত হয়ে যায়, যা বিভিন্ন কাজে ব্যবহার করা যায়। এজন্যই অপরিশোধিত তেলকে আংশিক পাতন করা প্রয়োজন।
পেট্রোলিয়ামের আংশিক পাতনে 0 °C থেকে 20 °C তাপমাত্রার - অঞ্চল থেকে পৃথকীকৃত অংশকে পেট্রোলিয়াম গ্যাস বলে। পেট্রোলিয়ামে শতকরা ২ ভাগ পেট্রোলিয়াম গ্যাস থাকে। এ গ্যাসকে চাপ প্রয়োগ করে তরলে পরিণত করে সিলিন্ডারে ভর্তি করে বাজারজাত করা হয়, যা আমরা রান্নার কাজে ও অন্যান্য কাজে ব্যবহার করি।
LPG এর পূর্ণ রূপ: Liquefied Petroleum Gas। অর্থাৎ, LPG হলে তরলীকৃত পেট্রোলিয়াম গ্যাস। পেট্রোলিয়াম গ্যাসকে চাপ প্রয়োগ করে তরলে পরিণত করে সিলিন্ডারে ভর্তি করা হয় এবং LPG নামে রান্নার কাজে ও অন্যান্য কাজে তাপ উৎপাদনের জন্য ব্যবহৃত হয়।
পেট্রোলিয়ামের আংশিক পাতনে 21° -70°C তাপমাত্রার অঞ্চল থেকে পৃথকীকৃত অংশকে পেট্রোল বা গ্যাসোলিন বলে।
পেট্রোলিয়ামে শতকরা ১ ভাগ পেট্রোল থাকে। যানবাহনের ইঞ্জিনে জ্বালানি হিসেবে গ্যাসোলিন ব্যবহৃত হয়।
পেট্রোলিয়ামের আংশিক পাতনে 71 °C- 120 °C তাপমাত্রার অঞ্চল থেকে পৃথকীকৃত অংশকে ন্যাপথা বলে। পেট্রোলিয়ামে শতকরা 10 ভাগ ন্যাপথা থাকে। জ্বালানি ও পেট্রোকেমিক্যাল শিল্পে ন্যাপথা ব্যবহৃত হয়।
পেট্রোলিয়ামের আংশিক পাতনে 121 °C-170 °C তাপমাত্রার অঞ্চল থেকে পৃথকীকৃত অংশকে কেরোসিন বলে। পেট্রোলিয়ামে শতকরা 13 ভাগ কেরোসিন থাকে। কেরোসিনকে জেট ইঞ্জিনের জ্বালানি হিসেবে ব্যবহার করা হয়।
পেট্রোলিয়ামের আংশিক পাতনে 171 °C-270 °C তাপমাত্রার অঞ্চল থেকে পৃথকীকৃত অংশকে বলা হয় ডিজেল। এ অংশে যে হাইড্রোকার্বনসমূহ থাকে তাদের অণুতে C-সংখ্যা 17- 20 পর্যন্ত। যানবাহনের জ্বালানি, পিচ্ছিলকারক পদার্থ ও দ্রাবক হিসেবে ডিজেল ব্যাপক ব্যবহৃত হয়।
পেট্রোলিয়ামের আংশিক পাতনে 217 °C -340°Cতাপমাত্রার অঞ্চল থেকে পৃথকীকৃত অংশকে প্যারাফিন মোম বলে। এ অংশে যে হাইড্রোকার্বনসমূহ থাকে তাদের অণুতে C-সংখ্যা 20 - 30 পর্যন্ত। প্যারাফিন মোম টয়লেট্রিজ এবং ভ্যাসলিন তৈরিতে ব্যবহৃত হয়।
পেট্রোলিয়ামের আংশিক পাতনে 340 °C থেকে উচ্চ তাপমাত্রার অঞ্চল হতে পৃথকীকৃত অংশকে বলা হয় পিচ। এ অংশে যে হাইড্রোকার্বনসমূহ থাকে তাদের অণুতে C-এর সংখ্যা 30 এর বেশি থাকে। পিচ রাস্তা তৈরিতে ব্যাপক ব্যবহৃত হয়।
শুধু কার্বন ও হাইড্রোজেন এর সমন্বয়ে গঠিত যৌগকে বলা হয় হাইড্রোকার্বন। যেমন- মিথেন , ইথিন , প্রোপিন , বেনজিন ইত্যাদি হচ্ছে হাইড্রোকার্বন। কেননা এসব যৌগসমূহে কার্বন (C) আর হাইড্রোজেন (H) ব্যতীত আর অন্য কোনো মৌল নেই।
যেসব যৌগ শুধুমাত্র কার্বন ও হাইড্রোজেন এর সমন্বয়ে গঠিত তাদেরকে হাইড্রোকার্বন বলে। ইথিন এর সংকেত = । ইথিন কার্বন (C) এবং হাইড্রোজেন (H) মৌলের সমন্বয়ে গঠিত। তাই ইথিন ( = ) একটি হাইড্রোকার্বন।
যে সকল হাইড্রোকার্বনের কার্বন শিকলের দুই প্রান্তের কার্বন (C) দুটি মুক্ত অবস্থায় থাকে, তাদেরকে বলা হয় মুক্ত শিকল হাইড্রোকার্বন। উদাহরণস্বরূপ:
বিউটেন: প্রোপিন দেখা যাচ্ছে, যৌগদ্বয়ের কার্বন শিকলের দুই প্রান্তের C মুক্ত অবস্থায় রয়েছে।
যে মুক্ত শিকল হাইড্রোকার্বনে শুধু কার্বন-কার্বন একক বন্ধন (C-C) থাকে, তাকে বলে সম্পৃক্ত মুক্ত শিকল হাইড্রোকার্বন। উদাহরণস্বরূপ:
একক কন্ধন (C-C)
প্রোপেন হাইড্রোকার্বন কার্বন-কার্বন একক বন্ধন বিদ্যমান। তাই এটি সম্পৃক্ত মুক্ত শিকল হাইড্রোকার্বন।
যে সকল মুক্ত শিকল হাইড্রোকার্বন এক বা একাধিক কার্বন-কার্বন দ্বিবন্ধন (C= C ) বা কার্বন-কার্বন ত্রিবন্ধন (- C = C-)C)থাকে, তাকে অসম্পৃক্ত মুক্ত শিকল হাইড্রোকার্বন বলে। উদাহরণস্বরূপ: ইথিন হাইড্রোকার্বনটিতে কার্বন-কার্বন দ্বিবন্ধন (C=C) রয়েছে, তাই এটি অসম্পৃক্ত মুক্ত শিকল হাইড্রোকার্বন।
যৌগটি অসম্পৃক্ত মুক্ত শিকল হাইড্রোকার্বন, কেননা হাইড্রোকার্বনটিতে কার্বন শিকলের দুই প্রান্তের কার্বন দুইটি মুক্ত অবস্থায় থাকে, তাই এটি মুক্ত শিকল হাইড্রোকার্বন। আবার এ হাইড্রোকার্বনটিতে কার্বন-কার্বন ত্রিবন্ধন ত্রিবন্ধন বিদ্যমান। তাই বলা যায়, হাইড্রোকার্বনটি অসম্পৃক্ত মুক্ত শিকল হাইড্রোকার্বন।
যে সকল হাইড্রোকার্বনের কার্বন শিকলের দুই প্রান্তের কার্বন (C) পরম্পর যুক্ত হয়ে বলয় বা চক্র গঠন করে তাকে বলা হয় বন্ধ শিকল হাইড্রোকার্বন। বন্ধ শিকল হাইড্রোকার্বন সম্পৃক্ত ও অসম্পৃক্ত দুই ধরনের হতে পারে।
উদাহরণস্বরূপ: সাইক্লোপ্রোপেন:
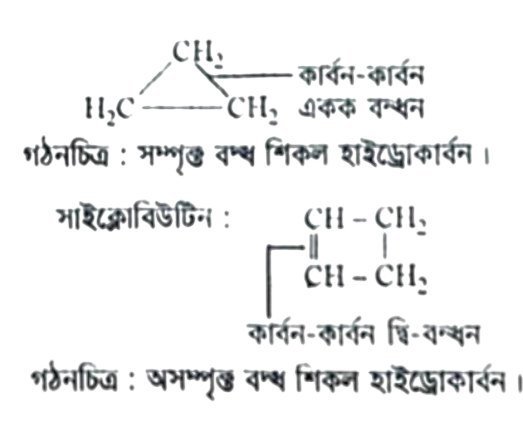
প্রদত্ত যৌগ দুটি হলো. সাইক্লোবিউটেন ও সাইক্লোবিউটিন যৌগ দুটির গাঠনিক সংকেত নিম্নরূপ :
বা
বা
উভয় যৌগই হাইড্রোকার্বন হলেও প্রথম যৌগটি অ্যালকেন এবং দ্বিতীয় যৌগটি অ্যালকিন। প্রথম যৌগটি সম্পৃক্ত হাইড্রোকার্বন এবং দ্বিতীয় যৌগটি অসম্পৃক্ত হাইড্রোকার্বন। প্রথম যৌগটি কার্বন-কার্বন একক বন্ধনে আবদ্ধ এবং দ্বিতীয় যৌগটি কার্বন-কার্বন দ্বিবন্ধন আবদ্ধ।
যেসব বন্ধ শিকল হাইড্রোকার্বনে অন্তত একটি কার্বন-কার্বন দ্বিবন্ধন (C = C) অথবা কার্বন-কার্বন ত্রিবন্ধন (C = C) বিদ্যমান, তাদেরকে অসম্পৃক্ত বদ্ধ শিকল হাইড্রোকার্বন বলে। সাইক্লোপ্রোপিন একটি বন্ধ শিকল হাইড্রোকার্বন এবং এতে একটি C = C বিদ্যমান। এজন্য সাইক্লোপ্রোপিন একটি অসম্পৃক্ত বদ্ধ শিকল হাইড্রোকার্বন।
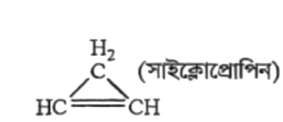
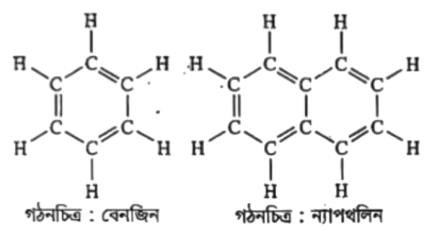
যে হাইড্রোকার্বন যৌগগুলো সাধারণত 5, 6 কিংবা 7 সদস্যের সমতলীয় যৌগ (Planar Compounds) এবং এদের গঠনে একান্তর (alternate) দ্বিবন্ধন থাকে অর্থাৎ পর্যায়ক্রমে কার্বন-কার্বন একটি একক বন্ধন এবং তারপর একটি দ্বিরন্ধন থাকে, তাদেরকে বলে অ্যারোমেটিক হাইড্রোকার্বন। উদাহরণস্বরূপ: বেনজিন ন্যাপথলিন হচ্ছে অ্যারোমেটিক হাইড্রোকার্বন।
বেনজিন যৌগটি হাইড্রোজেন ও কার্বন সমন্বয়ে গঠিত। বেনজিনের ক্ষেত্রে, ছয় কার্বন নিয়ে যৌগটি গঠিত এবং এতে একান্তর দ্বি-বন্ধন থাকে যা অ্যারোমেটিক যৌগের বৈশিষ্ট্য। যেহেতু বেনজিন যৌগটি C ও H নিয়ে গঠিত, তাই এটি হাইড্রোকার্বন এবং যৌগটিতে অ্যারোমেটিক বৈশিষ্ট্য বিদ্যমান, সেহেতু একে অ্যারোমেটিক হাইড্রোকার্বন বলে।
শুধুমাত্র হাইড্রোজেন (H) ও কার্বন (C) দ্বারা গঠিত দ্বিমৌল যৌগসমূহকে হাইড্রোকার্বন বলে যৌগে হাইড্রোজেন ও কার্বনের সাথে অক্সিজেন উপস্থিত আছে। তাই যৌগটিকে হাইড্রোকার্বন বলা যায় না।
ন্যাপথালিন যৌগটিতে একান্তর দ্বি-বন্ধন আছে এবং দুটি বেনজিন চক্র বিদ্যমান। এতে পাই () ইলেকট্রন সংখ্যা 10টি। হ্যাকেল সূত্র মতে
4n = 8
n = 2
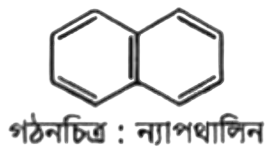
১. n এর মান 1, 2, 3….. ইত্যাদি হলে যৌগটি অ্যারোমেটিক যৌগ। সুতরাং, ন্যাপথালিন একটি অ্যারোমেটিক যৌগ।
অ্যারোমেটিক যৌগের বৈশিষ্ট্য হলো:
১. এরা সাধারণত 5, 6 কিংবা 7 সদস্যের সমতলীয় যৌগ।
২. এতে একান্তর দ্বিবন্ধন থাকে।
এখানে, হলো ন্যাপথালিন। এর গাঠনিক সংকেত নিম্নরূপ-
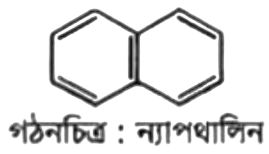
ন্যাপথলিন হলো দশ কার্বনবিশিষ্ট সমতলীয় চাক্রিক যৌগ। এতে পাঁচটি একান্তর দ্বিবন্ধন বিদ্যমান। সুতরাং , অ্যারোমেটিক যৌগ।
বেনজিন বেনজিন-জাতক ও এক বা একাধিক বেনজিন বলয় বিশিষ্ট যৌগ বা বেনজিনের ধর্ম সদৃশ যেকোনো বলয়াকার যৌগকে অ্যারোমেটিক যৌগ বলে। এসব যৌগ সমতলীয় চক্রিয় হয় এবং এতে একান্তর দ্বি-বন্ধনের উপস্থিতি থাকে। ফেনল তথা একটি বেনজিন জাতক এবং সমতলীয় চক্রিয় যৌগ, যাতে ৩টি একান্তর' দ্বি-বন্ধন রয়েছে। কাজেই ফেনল একটি অ্যারোমেটিক যৌগ।
যৌগটি অ্যালিসাইক্লিক। যৌগটির গঠন নিয়ে পাই-
গঠনচিত্র: সাইক্লোবিউটেন
দেখা যাচ্ছে, যৌগটিতে কোনো সঞ্চরণশীল পাই () ইলেকট্রন নেই। কিন্তু যৌগটি একটি চাক্রিক যৌগ। অর্থাৎ, যৌগটি অ্যালিসাইক্লিক যৌগ।
অ্যারোমেটিক যৌগের ২টি বৈশিষ্ট্য নিম্নরূপ-
১. অ্যারোমেটিক যৌগসমূহ 5, 6 বা 7 সদস্যের সমতলীয় চাক্রিক যৌগ।
২. এ ধরনের যৌগে একান্তর (alternate) দ্বিবন্ধন থাকে অর্থাৎ, পর্যায়ক্রমে কার্বন-কার্বন একটি একক বন্ধন এবং তারপর একটি দ্বিবন্ধন থাকে।
যে সকল যৌগের কার্যকরী মূলক একই হওয়ায় এদের ভৌত ও রাসায়নিক ধর্মের গভীর মিল থাকে, তারা একই শ্রেণিভুক্ত; এদেরকে বলা হয় সমগোত্রীয় শ্রেণি (Homologous)। একই সমগোত্রীয় শ্রেণির সকল সদস্যকে একটি সাধারণ সংকেত দ্বারা প্রকাশ করা হয়। যেমন, অ্যালকিন সমগোত্রীয় শ্রেণির সকল যৌগকেসংকেত দ্বারা প্রকাশ করা হয়।
ইথেন ও প্রোপেন একই সমগোত্রীয় শ্রেণিভুক্ত। কারণ ইথেন ও প্রোপেনের মধ্যে একটি মিথিলিন মূলকএর পার্থক্য আছে। যেমন-মিথিলিন মূলক
ইথেন প্রোপেন
এদের সাধারণ সংকেত একই এবং প্রস্তুত প্রণালিও একই। এজন্যই এরা একই সমগোত্রীয় শ্রেণিভুক্ত।
প্রোপেন ও বিউটেন একই সমগোত্রীয় শ্রেণিভুক্ত। কারণ প্রোপেন ও বিউটেনের মধ্যে একটি মিথিলিন মূলক এর পার্থক্য আছে। যেমন-
মিথিলিন মূলক
এদের সাধারণ সংকেত একই এবং প্রস্তুত প্রণালিও একই। এজন্যই এরা একই সমগোত্রীয় শ্রেণিভুক্ত।
দুইটি অ্যারোমেটিক যৌগ হলো বেনজিন এবংন্যাপথলিন এদের বন্ধন দেখিয়ে গাঠনিক সংকেত নিম্নরূপ-গঠন:
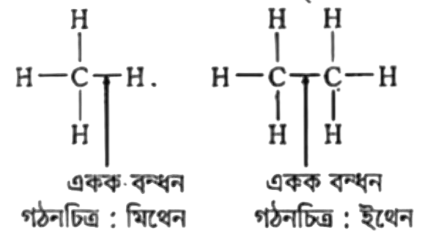
যে সকল হাইড্রোকার্বনে কার্বন-কার্বন একক বন্ধন বিদ্যমান তাদেরকে বলে সম্পৃক্ত হাইড্রোকার্বন। উদাহরণস্বরূপ, মিথেন ইথেন প্রোপেন ইত্যাদি যৌগগুলো সম্পৃক্ত হাইড্রোকার্বন। কেননা যৌগগুলোতে কার্বন-কার্বন একক বন্ধন (C-C) বিদ্যমান। তাই এরা সম্পৃক্ত হাইড্রোকার্বন। যেমন-
বিউটেন এর গঠন নিয়ে পাই,

যৌগটির গঠন হতে দেখা যায়, যৌগটিতে কার্বন-কার্বন একক বন্ধন (C-C) বিদ্যমান। তাই এটি সম্পৃক্ত যৌগ। এটি অসম্পৃক্ত যৌগের ন্যায় যুত, ব্রোমিন দ্রবণ বিক্রিয়া দেয় না।
যে সকল হাইড্রোকার্বনের কার্বন শিকলে কার্বন-কার্বন একক বন্ধন বিদ্যমান থাকে, তারা হচ্ছে অ্যালকেন যৌগ। অ্যালকেনের সাধারণ সংকেত এ শ্রেণির ১ম সদস্য মিথেন কেননা ১ম সদস্য বলে n = 1 তাই যৌগটি বা
প্যারাফিন অর্থ আসক্তিহীন। অ্যালকেনসমূহ কার্বন-কার্বন ও কার্বন-হাইড্রোজেনের একক সমযোজী বন্ধনের 'মাধ্যমে গঠিত হয়। তাই এই যৌগসমূহ সাধারণত রাসায়নিক বিক্রিয়ায় অংশগ্রহণ করে না। এজন্য এদের প্যারাফিন বলা হয়। এরা এসিড, ক্ষার, ধাতু ও জারকের সাথেও বিক্রিয়া করে না।
জৈব যৌগের অ্যালকেনসমূহকে প্যারাফিন বলে। প্যারাফিন একটি ল্যাটিন শব্দ। এর অর্থ হলো নিষ্ক্রিয় বা আকর্ষণ নেই। অ্যালকেনসমূহে কার্বন-কার্বন এবং কার্বন-হাইড্রোজেন বন্ধনসমূহ অত্যন্ত শক্তিশালী হওয়ায় অ্যালকেনসমূহ সাধারণত রাসায়নিকভাবে নিষ্ক্রিয় হয়। ফলে এরা সাধারণত তীব্র এসিড, ক্ষারক ও জারক বা বিজারক পদার্থের সাথে বিক্রিয়া করে না। অর্থাৎ নিষ্ক্রিয় থাকে। তাই অ্যালকেনসমূহকে প্যারাফিন বলে।
প্যারাফিন অর্থ আসক্তিহীন। এরা এসিড, ক্ষার ধাতু ও জারকের সাথে বিক্রিয়া করে না। সাধারণভাবে অ্যালকেন যৌগসমূহকে প্যারাফিন বলা হয়। ইথেন অ্যালকেন জাতীয় যৌগ। এতে উপস্থিত C-C এবং CH বন্ধনগুলো খুব শক্তিশালী ও স্থায়ী। তাই এরা তীব্র এসিড, ক্ষারক, জারক, বিজারকের সাথে বিক্রিয়া করে না। এজন্য ইথেনকে প্যারাফিন বলে।
হচ্ছে বিউটেন, যা একটি প্যারাফিন। প্যারাফিন ল্যাটিন শব্দ যার অর্থ নিষ্ক্রিয় বা আকর্ষণ নেই। বিউটেন এ কার্বন-কার্বন ও কার্বন-হাইড্রোজেন বন্ধনসমূহ অত্যন্ত শক্তিশালী হওয়ায় বিউটেন সাধারণত রাসায়নিকভাবে নিষ্ক্রিয় হয়। ফলে এটি সাধারণত তীব্র এসিড, ক্ষারক ও জারক বা বিজারক পদার্থের সাথে বিক্রিয়া করে না। তাই বিউটেনকে প্যারাফিন বলে।
অ্যালকেন থেকে একটি হাইড্রোজেন পরমাণু অপসারণ করলে যে একযোজী মূলকের সৃষ্টি হয়, তাকে বলা হয় অ্যালকাইল মূলক। যেমন অ্যালকেনের সাধারণ সংকেত ১টি H পরমাণু অপসারণ করলে সৃষ্ট একযোজী মূলক হয় এটাই হচ্ছে অ্যালকাইল মূলক। একে R দ্বারা প্রকাশ করা হয়।
একটি অ্যালকাইল মূলক। কারণ অ্যালকেন থেকে একটি হাইড্রোজেন পরমাণু অপসারণ ক রলে যে একযোজী মূলকের সৃষ্টি হয় তাকে অ্যালকাইল মূলক বলে। অ্যালকেনের সাধারণ সংকেত একটি H অপসারণ হলে সংকেতটি দাঁড়ায় এখন n = 5 হলে অ্যালকাইল মূলক হবে বা একটি অ্যালকাইল মূলক।
প্রোপাইল মূলক এর নামকরণ ব্যাখ্যা কর।
অ্যালকেন থেকে একটি হাইড্রোজেন পরমাণু অপসারণ করলে যে একযোজী মূলকের সৃষ্টি হয় তাকে বলে অ্যালকাইল মূলক। এর সাধারণ সংকেত
উচ্চারণের ক্ষেত্রে শেষে "আইল" শব্দ যোগ করতে হয়। যেমন, প্রোপেন) থেকে একটি প্রোটন (H') অপসারণ করলে মূলক থাকে। সুতরাং মূলকের নাম হবে প্রোপাইল মূলক ।
একটি অ্যালকাইল মূলক। কারণ অ্যালকেন থেকে একটি হাইড্রোজেন পরমাণু অপসারণ করলে যে একযোজী মূলকের সৃষ্টি হয় তাকে অ্যালকাইল মূলক বলে। অ্যালকাইলের সাধারণ সংকেত দাঁড়ায় হলে মুলকটি হবে সুতরাং একটি অ্যালকাইল মূলক।
অ্যালকেন প্রস্তুতি নিকেল প্রভাবকের উপস্থিতিতে কার্বন ডাইঅক্সাইডের সাথে হাইড্রোজেনকে 250 °C তাপমাত্রায় উত্তপ্ত করলে মিথেন এবং পানি উৎপন্ন হয়।
বিক্রিয়া
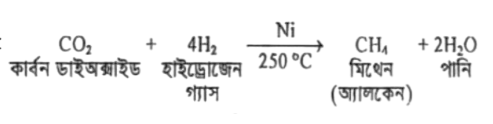
যে বিক্রিয়ায় ক্যালসিয়াম অক্সাইডের উপস্থিতিতে সোডিয়াম ইথানয়েটকে সোডিয়াম হাইড্রোক্সাইড এর সাথে উত্তপ্ত করলে মিথেন এবং সোডিয়াম কার্বনেট উৎপন্ন হয়, তাকে বলে ডিকার্বক্সিলেশন বিক্রিয়া।
উদাহরণ-
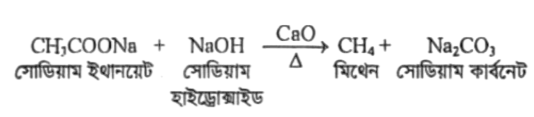
অ্যালকেনের ২টি ভৌত ধর্ম নিম্নরূপ-
১. 1 থেকে 4 কার্বন সংখ্যার সম্পৃক্ত হাইড্রোকার্বন তথা অ্যালকেন সাধারণত গ্যাসীয় অবস্থায় থাকে।
২. সম্পৃক্ত হাইড্রোকার্বনের কার্বন সংখ্যা 16 থেকে বেশি হলে এগুলো কঠিন প্রকৃতির হয়ে থাকে।
অ্যালকেনের ২টি রাসায়নিক ধর্ম নিম্নরূপ-
১. অ্যালকেনসমূহ রাসায়নিকভাবে অনেকটা নিষ্ক্রিয়; এরা সাধারণ অবস্থায় এসিড, ক্ষারক বা বিজারকের সাথে বিক্রিয়া করে না।
২. অ্যালকেনসমূহ দহন বিক্রিয়ায় কার্বন ডাইঅক্সাইড, জলীয় বাষ্প ও তাপশক্তি উৎপন্ন করে।
যেসব হাইড্রোকার্বনের কার্বন শিকলে অন্তত একটি দ্বি-বন্ধন (=) বা একটি ত্রিবন্ধন (=) থাকে তাদেরকে অসম্পৃক্ত হাইড্রোকার্বন বলে। যেমন, অ্যালকিন বা অ্যালকাইনসমূহ অসম্পৃক্ত হাইড্রোকার্বন। ইথিন অণুতে কার্বন-কার্বন দ্বিবন্ধন (C = C) রয়েছে। তাই এটি অসম্পৃক্ত হাইড্রোকার্বন আবার ইথাইন (CH = CH) অণুতে কার্বন-কার্বন ত্রিবন্ধন (C= C) রয়েছে। তাই এটিও অসম্পৃক্ত হাইড্রোকার্বন।
যে সকল জৈব যৌগের কার্বন শিকলে অন্তত একটি কার্বন-কার্বন দ্বিবন্ধন (C = C) থাকে, তাকে অ্যালকিন বলে। অ্যালকিনের সাধারণ সংকেত অ্যালকিনের সর্বনিম্নতর সদস্য ইথিন
অ্যালকিনকে অলিফিন বলা হয়। কারণ অ্যালকিনের নিম্নতর সদস্যগুলো (ইথিন, প্রোপিন ইত্যাদি) হ্যালোজেনের ( সঙ্গে বিক্রিয়ায় তৈলাক্ত পদার্থ উৎপন্ন করে। এজন্য অ্যালকিনকে অলিফিন (Olifin, Greek: Olefiant = Oil forming) বলে।
তথা অ্যালকিনকে.. অলিফিন বলা হয়। কারণ অ্যালকিনের নিম্নতর সদস্যগুলো (ইথিন, প্রোপিন ইত্যাদি) হ্যালোজেনের () সঙ্গে বিক্রিয়ায় তৈলাক্ত পদার্থ উৎপন্ন করে। এজন্য অ্যালকিনকে অলিফিন (Olifin, Greek: Olefiant= Oil forming) বলে।
প্রোপিনকে অলিফিন বলা হয়। কারণ প্রোপিন নিম্নতর সদস্যবিশিস্ট অ্যালকিন, যা হ্যালোজেনের সাথে বিক্রিয়ায় তৈলাক্ত পদার্থ উৎপন্ন করে। এজন্য C₂H₂ অলিফিন (Olifin. Greck; olefiant - Oil forming) বলে।
যৌগটি অসম্পৃক্ত যৌগ। কারণ নিষ্ক্রিয় দ্রাবক এর উপস্থিতিতে বিউটিন () এর সঙ্গে ব্রোমিন দ্রবণের যুত বিক্রিয়ায় বর্ণহীন 1, 2 ডাইব্রোমো বিউটেন উৎপন্ন করে। এই পরীক্ষাটি হলো অসম্পৃক্ততা প্রমাণ পরীক্ষা, তাই বলা যায় একটি অসম্পৃক্ত যৌগ।
বিক্রিয়া
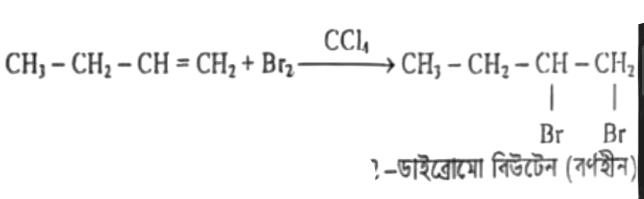
ইথিন অসম্পৃক্ত হাইড্রোকার্বন। কারণ এটি লাল বর্ণের ব্রোমিন দ্রবণের সাথে বিক্রিয়া করে কার্বন-কার্বন দ্বি-বন্ধনে ব্রোমিন অণু যুক্ত হয়। ফলে ব্রোমিনের লাল বর্ণ বর্ণহীন হয়ে যায়।
বর্ণহীন যৌগ
এ কারণে ইথিন অসম্পক হাইডোকার্বন।
অ্যালকিন প্রস্তুতি: ইথানলের সাথে অতিরিক্ত গাঢ় সালফিউরিক এসিডকে উত্তপ্ত করলে ইথিন এবং পানি উৎপন্ন হয়।
বিক্রিয়া
ইথানল ইথিন পানি
অ্যালকিনের সংযোজন বিক্রিয়া: নিকেল প্রভাবকের উপস্থিতিতে ইথিনকে হাইড্রোজেনের সাথে 180-200 °C তাপমাত্রায় উত্তপ্ত করলে ইথেন উৎপন্ন হয়।
বিক্রিয়া
ইথিন হাইড্রোজেন ইথেন
ইথিন থেকে ইথানল প্রস্তুতি: ফসফরিক এসিড প্রভাবকের উপস্থিতিতে ইথিন পানির বাষ্পের সাথে উচ্চ তাপ এবং উচ্চ চাপে বিক্রিয়া করে ইথানল উৎপন্ন করে।
বিক্রিয়া :

ইথিনের ব্রোমিন সংযোজন বিক্রিয়া: ইথিনের মধ্যে লাল বর্ণের ব্রোমিন দ্রবণ যোগ করলে পরস্পরের সাথে বিক্রিয়া করে ডাইব্রোমো ইথেন উৎপন্ন করে। এ বিক্রিয়ায় ব্রোমিনের লাল বর্ণ দূরীভূত হয়। এ বিক্রিয়া দ্বারা অ্যালকিনের অসম্পৃক্ততা প্রমাণ করা যায়।
বিক্রিয়া:
ইথিন লালবর্ণের ব্রোমিন ডাইব্রোমো ইথেন বর্ণহীন
ইথিনের মধ্যে গোলাপি বর্ণের পটাশিয়াম পারম্যাঙ্গানেট এর দ্রবণ, পটাশিয়াম হাইড্রোক্সাইড যোগ করলে জারণ বিক্রিয়ায় ইথিলিন গ্লাইকল উৎপন্ন হয়। এ বিক্রিয়ায় পটাশিয়াম পারম্যাঙ্গানেটের গোলাপি বর্ণ দূরীভূত হয়। সকল অসম্পৃক্ত হাইড্রোকার্বন এ বিক্রিয়া প্রদর্শন করে।
বিক্রিয়া:
ইথিন ইথিলিন গ্লাইকল
ইয়িনকে সামান্য পরিমাণ অক্সিজেনের উপস্থিতিতে 100 atm চাপে ও 200 °C তাপমাত্রায় উত্তপ্ত করলে পলিথিন উৎপন্ন হয়; এই বিক্রিয়াকে বলা হয় পলিমারকরণ বিক্রিয়া। এ বিক্রিয়ায় ইথিন হচ্ছে মনোমার। এক্ষেত্রে বিক্রিয়াটি হবে-
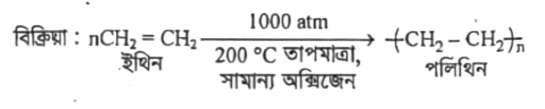
অ্যালকেনসমূহ কার্বন-কার্বন ও কার্বন-হাইড্রোজেন শক্তিশালী একক সমযোজী বন্ধনের মাধ্যমে গঠিত। তাই এ যৌগসমূহ সহজে রাসায়নিক বিক্রিয়ায় অংশগ্রহণ করে না। কিন্তু অ্যালকিন অণুতে কার্বন-কার্বন দ্বিবন্ধন বিদ্যমান যার প্রথমটি শক্তিশালী হলেও দ্বিতীয় বন্ধনটি খুবই দুর্বল। ফলে অ্যালকিন অণুসমূহ রাসায়নিকভাবে অত্যন্ত সক্রিয় হয়।
অ্যালকেন ও অ্যালকিনসমূহ C ও H দ্বারা গঠিত। C ও H. দাহ্য পদার্থ। তবে C অপেক্ষা H অধিকতর দাহ্য। এক্ষেত্রে অ্যালকেন অতিরিক্ত বায়ুর সাথে বিক্রিয়া করে ও শক্তি উৎপন্ন করে। কিন্তু অ্যালকিনে অ্যালকেন অপেক্ষা কম H থাকে বলে বিক্রিয়ায় উৎপন্ন তাপের পরিমাণও কম হয়। তাই অ্যালকেন, অ্যালকিন অপেক্ষা ভালো জ্বালানি।
যৌগই কার্বন ও হাইড্রোজেনের সমন্বয়ে গঠিত। কার্বন ও হাইড্রোজেন উভয়ই দাহ্য পদার্থ হলেও কার্বনের তুলনায় হাইড্রোজেন অধিকতর দাহ্য। অ্যালকিনে হাইড্রোজেনের শতকরা পরিমাণ অ্যালকেনের তুলনায় কম। তাই অপেক্ষা কম দাহ্য।
প্রোপিন ও প্রোপেন এর মধ্যে বিক্রিয়াসহ পার্থক্য
| প্রোপিন | প্রোপেন |
| ১. প্রোপিন অসম্পৃক্ত হাইড্রোকার্বন। | ১. প্রোপেন সম্পৃক্ত হাইড্রোকার্বন। |
| ২. প্রোপিনে দ্বিবন্ধন বিদ্যমান। | ২. প্রোপেনে একক বন্ধন বিদ্যমান। |
| ৩. প্রোপিন এর সাথে ব্রোমিন পানির বিক্রিয়ায় ডাইব্রোমো প্রোপেন উৎপন্ন হয়। | ৩. প্রোপেন ব্রোমিন পানির সাথে বিক্রিয়া করে না। বিক্রিয়া হয় না। |
অ্যালকেন ও অ্যালকিনের মধ্যে রাসায়নিক ধর্মের পার্থক্য:
যে জৈব যৌগে কার্বন শিকলে অন্তত একটি কার্বন-কার্বন ত্রিবন্ধন (-CC-) থাকে, তাকে বলা হয় অ্যালকাইন। অ্যালকাইনের সাধারণ সংকেত । অ্যালকাইন শ্রেণির ক্ষুদ্রতম সরল সদস্য ইথাইন (CH = CH) বা অ্যাসিটিলিন (acetylene) ।
অ্যালকাইন প্রস্তুতি: ক্যালসিয়াম কার্বাইডের মধ্যে পানি যোগ করলে ইথাইন তথা অ্যালকাইন এবং ক্যালসিয়াম হাইড্রোক্সাইড উৎপন্ন হয়। এক্ষেত্রে সংঘটিত বিক্রিয়াটি নিম্নরূপ-
ক্যালসিয়াম কার্বাইড ইথাইন [অ্যালকাইন] ক্যালসিয়াম হাইড্রোক্সাইড
অ্যালকাইনের ২টি বৈশিষ্ট্য নিম্নরূপ-
১. অ্যালকাইনে কার্বন-কার্বন ত্রিবন্ধন (-C=C-) থাকে।
২. অ্যালকাইনের দুর্বল বন্ধনগুলো ভেঙে সংযোজন বিক্রিয়ায় অংশগ্রহণ করে।
নিকেল প্রভাবকের উপস্থিতিতে ইথাইন এর সাথে হাইড্রোজেন সংযোগ করে উত্তপ্ত করলে ইথেন উৎপন্ন হয়।
বিক্রিয়া:
ইথাইন হাইড্রোজেন ইথেন
ইথাইনের অসম্পৃক্ততার পরীক্ষা: ইথাইনের মধ্যে লাল বর্ণের ব্রোমিন দ্রবণ চালনা করলে পরস্পরের সাথে বিক্রিয়া করে টেট্রাব্রোমো ইথেন উৎপন্ন করে। এই বিক্রিয়ায় ব্রোমিনের লালবর্ণ অপসারিত হয়। এই বিক্রিয়া দ্বারাই প্রমাণিত হয় যে, ইথাইন একটি অসম্পৃক্ত যৌগ।
বিক্রিয়া:
ইথাইন ব্রোমিন [লালবর্ণ] টেট্রাব্রোমো ইথেন [বর্ণহীন]
ক্যালসিয়াম কার্বাইডের মধ্যে পানি যোগ করলে ইথাইন এবং ক্যালসিয়াম হাইড্রক্সাইড উৎপন্ন হয়।'
বিক্রিয়া: ইথাইন
অ্যালকাইনের সংযোজন বিক্রিয়াসমূহ:
(i) হাইড্রোজেন সংযোজন
(ii) ব্রোমিন সংযোজন
(iii) পানি সংযোজন
ইথাইন এর সাথে 80 °C তাপমাত্রায় 20% সালফিউরিক এসিড এবং 2% মারকিউরিক সালফেট দ্রবণ যোগ করলে ইথান্যাল উৎপন্ন হয়।
বিক্রিয়া:
ইথাইন ইথান্যাল
সাধারণ সংকেতবিশিষ্ট যৌগগুলো অ্যালকাইন নামে পরিচিত। এ যৌগগুলোতে কার্বন-কার্বন ত্রিবন্ধন রয়েছে। যৌগটিতে H পরমাণুর সংখ্যা C পরমাণুর দ্বিগুণের চেয়ে ২টা কম এবং যৌগটিতে কার্বন-কার্বন ত্রিবন্ধন (-C=C-) বিদ্যমান। তাই এটি অসম্পৃক্ত যৌগ। যেমন- যৌগটির গঠন নিয়ে পাই,
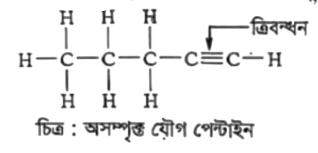
যে সকল জৈব যৌগে হাইড্রোক্সিল মূলক (-OH) বিদ্যমান থাকে, তাকে বলা হয় অ্যালকোহল। অ্যালকোহলের সাধারণ সংকেত একে ROH দ্বারা প্রকাশ করা হয়; যেখানে R হলো অ্যালকাইল মূলক। অ্যালকোহল শ্রেণির ১ম সদস্য হলো মিথানল ৩য় সদস্য প্রোপানল ইত্যাদি।
অ্যালকোহলের ২টি বৈশিষ্ট্য নিম্নরূপ-
১. অ্যালকোহল শ্রেণির ১ম দিকের সদস্যগুলো বর্ণহীন তরল পদার্থ।
২. এ শ্রেণির ১ম দিকের সদস্যগুলো পানিতে যে কোনো অনুপাতে মিশ্রিত হয়।
যে সকল জৈব যৌগে হাইড্রক্সিল মূলক (-OH) বিদ্যমান, তা হচ্ছে অ্যালকোহল। এদের সাধারণ সংকেত এ শ্রেণির 'প্রথম সদস্য হচ্ছে মিথানল ২য় সদস্য ইথানল ফেনল যৌগে OH মূলক থাকা সত্ত্বেও একে অ্যালকোহল বলা হয় না। কারণ ফেনল অ্যালকোহলের সাধারণ সংকেতঅনুসরণ করে না।
ফার্মেন্টেশন পদ্ধতিতে ইথানল উৎপাদন গ্লুকোজের লঘু জলীয় দ্রবণে (10%) ঈস্ট মিশ্রিত করে 20-25°C তাপমাত্রায় রেখে দিলে ঈস্ট থেকে নিঃসৃত জাইমেজ নামক এনজাইমের প্রভাবন ক্রিয়ায় গ্লুকোজের ফার্মেন্টেশন ঘটে এবং গ্লুকোজ বিযোজিত হয়ে ইথানল ও উৎপন্ন হয়।
বিক্রিয়া :
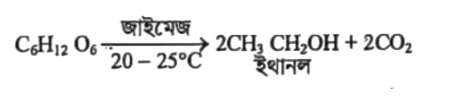
উচ্চ তাপ (300°C), উচ্চচাপ (60 বায়ুচাপ) ও প্রভাবকের উপস্থিতিতে কোন যৌগে পানিযোজনকে হাইড্রেশন বা পানিযোজন বলে। যেমন, ইথিনকে ফসফরিক এসিড প্রভাবকের উপস্থিতিতে হাইড্রেশন করলে ইথানল উৎপন্ন হয়।
ইথিন ইথানল
অ্যালকেনের নামের শেষের 'ও' বাদ দিয়ে অল (ol) যোগ করে অ্যালকোহলের নামকরণ করা হয়। যেমন, ইথেন (Ethene) নামের শেষের 'e' বাদ দিয়ে অল (ol) যোগ করলে অ্যালকোহলের নাম হয় Ethenol তথা ইথানল এর সংকেত: এইরূপ প্রোপেন (Propene) অ্যালকেন থেকে অ্যালকোহলের নাম হয় প্রোপানল (Propenol); যার সংকেত:
অ্যালকোহল প্রস্তুতি: ব্রোমো ইথেন এর মধ্যে সোডিয়াম হাইড্রোক্সাইড এর জলীয় দ্রবণ যোগ করে উত্তপ্ত করলে ইথানল তথা অ্যালকোহল এবং সোডিয়াম ব্রোমাইড উৎপন্ন হয়।
বিক্রিয়া:
ইথাইল ব্রোমাইড সোডিয়াম হাইড্রোক্সাইড ইথানল সোডিয়াম ব্রোমাইড
অ্যালকোহল থেকে অ্যালকিন প্রস্তুতি: গাঢ় এর উপস্থিতিতে 170°C তাপমাত্রা অ্যালকোহলকে তাপ দিলে অ্যালকিন পাওয়া যায়।
অ্যালকোহল অ্যালকিন
অ্যালকিন হতে অ্যালকোহল প্রস্তুতি: অ্যালকিনকে এর উপস্থিতিতে বিক্রিয়া করলে অ্যালকোহল উৎপন্ন হয়।
অ্যালকিন অ্যালকোহল
ফার্মেন্টেশন পদ্ধতিতে ইথানল উৎপাদন নিম্নরূপ: গ্লুকোজের লঘু জলীয় দ্রবণে (10%) ঈস্ট মিশ্রিত করে 20 25°C তাপমাত্রায় রেখে দিলে ঈস্ট থেকে নিঃসৃত জাইমেজ নামক এনজাইমের প্রভাবন ক্রিয়ায় গ্লুকোজের ফার্মেন্টেশন ঘটে এবং গ্লুকোজ বিযোজিত হয়ে ইথানল ও উৎপন্ন হয়।

যে সকল জৈব যৌগে অ্যালডিহাইড গ্রুপ (- CHO) বিদ্যমান থাকে, তাকে বলা হয় অ্যালডিহাইড। অর্থাৎ, IUPAC অনুসারে, অ্যালডিহাইড শ্রেণির যৌগের কার্যকরী মূলক CHO। এদের নামের শেষে 'অ্যাল' কথাটি যুক্ত থাকে। অ্যালডিহাইডের সাধারণ সংকেত R – CHO; যেখানে R' হলো অ্যালকাইল মূলক। তবে কেবল ১ম যৌগ ফরম্যালডিহাইড (H-CHO) এর ক্ষেত্রে R = H।
অ্যালডিহাইডের সাধারণ সংকেত: RCHO. এখানে R হচ্ছে অ্যালকাইল মূলক এবং CHO হচ্ছে এর কার্যকরী মূলক। যেখানে R = তবে ব্যতিক্রম এ শ্রেণির ১ম যৌগ ফরমালডিহাইডের ক্ষেত্রে R = H। অর্থাৎ অ্যালকেনের নামের শেষের '' 'বাদ দিয়ে অ্যাল (al) যোগ করে অ্যালডিহাইডের নামকরণ করা হয়। যেমন: প্রোপেন অ্যালকেন থেকে অ্যালডিহাইডের নামকরণ: প্রোপান্যাল
অ্যালডিহাইড প্রস্তুতি: 80°C তাপমাত্রায় ইথাইন এর মধ্যে 20% সালফিউরিক এসিড এবং 2% মারকিউরিক সালফেট দ্রবণ যোগ করলে ইথান্যাল তথা অ্যালডিহাইড উৎপন্ন হয়।
বিক্রিয়া:
ইথান্যাল
ফরমালডিহাইড (মিথান্যাল) এর 40% জলীয় দ্রবণকে বলা হয় ফরমালিন (Formalin)। ফরমালিনে 60% এবং 40% মিধান্যাল (HCHO) থাকে। এটি বর্ণহীন ও দুর্গন্ধযুক্ত গ্যাস হিসেবে এর সবিশেষ পরিচিতি রয়েছে। এটি আগুনে জ্বলে এবং বিষাক্ত পদার্থ।
ফরমালিনের প্রধান ২টি ব্যবহার নিম্নরূপ-
১. বিভিন্ন স্মৃত প্রাণিদেহ সংরক্ষণ করার জন্য ফরমালিন ব্যাপকভাবে ব্যবহৃত হয়।
২. গবেষণাগারে ফরমালিন এর ব্যাপক ব্যবহার রয়েছে।
ফরমালিনের দুইটি ক্ষতিকর দিক নিচে উল্লেখ করা হলো-
১. ফরমালিন যুক্ত খাবার খেলে মানুষ মরণব্যাধি ক্যান্সারে আক্রান্ত হতে পারে।
২. ফরমালিন দেহের সংস্পর্শে এলে যেমন ত্বক, চোখ, নাক, গলা, পরিপাকতন্ত্র ও শ্বাসযন্ত্রে গুরুতর উপসর্গ সৃষ্টি করতে পারে,। তেমনি ঘটাতে পারে মৃত্যু।
মিথান্যাল এর ব্যবহার:
i. মিথান্যাল থেকে ডেরলিন নামক পলিমার প্রস্তুত, করা হয়। ডেরলিন দিয়ে চেয়ার, ডাইনিং টেবিল, বালতি ইত্যাদি প্লাস্টিক দ্রব্য তৈরি করা হয়।
ii. মিথান্যাল ও ইউরিয়া থেকে ইউরিয়া-ফরমালডিহাইড রেজিন নামক পলিমার প্রস্তুত করা হয়, যা গৃহের প্লেট, গ্লাস ও মগ ইত্যাদি তৈরিতে ব্যবহৃত হয়।
মিথান্যাল (H CHO) একটি জৈব যৌগ। এজন্য পানিতে দ্রবণীয় হওয়ার কথা না। কিন্তু মিথান্যাল (H- CHO) এর কার্বনাইল গ্রুপ (> C = ০) টি একটি পোলার গ্রুপ। C ও ০ এর তড়িৎ ঋণাত্মকতার পার্থক্য বেশি হওয়ায়
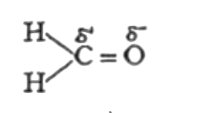 যৌগে পোলারিটির সৃষ্টি হয়। এজন্য পোলার অণু সহজেই এতে যুক্ত হতে পারে বলে "মিথান্যাল পানিতে দ্রবণীয়।"
যৌগে পোলারিটির সৃষ্টি হয়। এজন্য পোলার অণু সহজেই এতে যুক্ত হতে পারে বলে "মিথান্যাল পানিতে দ্রবণীয়।"
জৈব যৌগে কার্বক্সিল গ্রুপ (-COOH) বিদ্যমান থাকে, তাকে বলে জৈব এসিড বা ফ্যাটি এসিড। জৈব এসিডের সাধারণ সংকেত । এর কার্যকরী মূলক –COOH। এটি জলীয় দ্রবণে H' আয়ন দান করে। উদাহরণস্বরূপ: ইথানয়িক এসিড প্রোপানয়িক এসিড ইত্যাদি জৈব এসিড।
জৈব এসিডের সাধারণ সংকেত এর নামকরণের ক্ষেত্রে, মূল অ্যালকেনের ইংরেজি নামের শেষের '' বাদ দিয়ে অয়িক এসিড (oic acid) যুক্ত করে জৈবু এসিডের নামকরণ করা হয়। যেমন: অ্যালকেনের ২য় সদস্য ইথেন থেকে জৈব এসিডের নামকরণ হয় ইথানয়িক এসিড আবার প্রোপেন অ্যালকেন থেকে জৈব এসিডের নামকরণ হয় প্রোপানয়িক এসিড ইত্যাদি।
ফ্যাটি এসিড প্রস্তুতি: ইথান্যালের মধ্যে লঘু সালফিউরিক এসিড ও পটাশিয়াম ডাইক্রোমেট যোগ করলে ইথানয়িক এসিড উৎপন্ন হয়।
বিক্রিয়া:
ইথান্যাল জারমান অক্সিজেন ইথানয়িক এসিড বা অ্যাসিটিক এসিড
ফ্যাটি এসিডের ২টি ভৌত ধর্ম নিম্নরূপ-
১. সকল ফ্যাটি এসিড হলো দুর্বল এসিড।
২. ফ্যাটি এসিডসমূহ টক স্বাদযুক্ত; যেমন আঙুর, লেবু, টমেটো প্রভৃতি টক ফলে ফ্যাটি এসিড বিদ্যমান।
ফ্যাটি এসিডের ২টি রাসায়নিক ধর্ম নিম্নরূপ-
১. ফ্যাটি এসিডসমূহের জলীয় দ্রবণ নীল লিটমাসকে লাল করে।
২. ফ্যাটি এসিড ক্ষারের সাথে বিক্রিয়া করে লবণ ও পানি উৎপন্ন করে। যেমন-
বিক্রিয়া:

ইথানয়িক এসিড এর 4% থেকে 10% জলীয় দ্রবণকে বলা হয় ভিনেগার (Vinegar)। ভিনেগারের দ্রবণ মৃদু অম্লীয় বলে খাদ্যে ব্যবহার করলে খাদ্যে ব্যাকটেরিয়া বা ঈস্ট জন্মাতে পারে না। ফলে খাদ্য পচে না। তাই ভিনেগার খাবার তৈরিতে ও খাদ্য সংরক্ষক হিসেবে কাজ করে।
ইথানয়িক এসিডের (410)% জলীয় দ্রবণকে ভিনেগার বলা হয়। ভিনেগার এক ধরনের খাদ্য সংরক্ষক। কারণ এটি মানুষের, খাদ্য উপযোগী দুর্বল এসিড যা খাবারের ব্যাকটেরিয়া ধ্বংস করে এবং খাদ্যকে পঁচনের হাত থেকে রক্ষা করে।
COOH জৈব এসিডের কার্যকরী মূলকের সংকেত। COOH মূলক বিশিষ্ট যেকোনো জৈব এসিডকে নিম্নোক্ত উপায়ে শনাক্তকরণ করা যায়।
১. এটি নীল লিটমাসকে লাল করে।
২. এটি ক্ষার বা ক্ষারকের সাথে বিক্রিয়ায় লবণ ও পানি উৎপন্ন করে।
(লবণ)
এর বুদবুদ বিক্রিয়ায় - COOH মূলক বিশিষ্ট জৈব এসিডের উপস্থিতি নিশ্চিত করে।
প্রোপানয়িক এসিডের সাথে পটাশিয়াম হাইড্রোক্সাইডের জলীয় দ্রবণ যোগ করলে পরস্পরের সাথে বিক্রিয়া করে পটাশিয়াম প্রোপানয়েট লবণ ও পানি উৎপন্ন করে। যেমন-
বিক্রিয়া:
উপরিউক্ত বিক্রিয়া ২টি পূর্ণ করে পাই,
অ্যালকাইল সোডিয়াম ইথানল সোডিয়াম হ্যালাইড হ্যালাইড হাইড্রোক্সাইড X-Cl, F. I ইত্যাদি
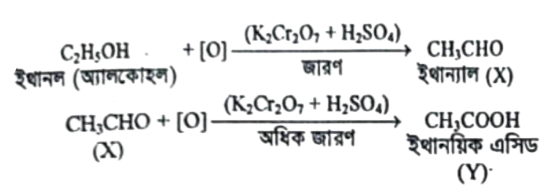
উপরিউক্ত বিক্রিয়াদ্বয় পূর্ণ করে পাই-
ইথিন পানি ইথানল
(অ্যালকিন)
ইথাইন পানি ইথান্যাল
(অ্যালকাইন)
অ্যালকোহলের দুইটি ব্যবহার নিম্নরূপ-
১. অ্যালকোহল তথা ইথানলকে প্রধানত পারফিউম, কসমেটিকস ও ওষুধ শিল্পে দ্রাবক হিসেবে ব্যবহার করা হয়।
২. বর্তমানে ব্রাজিলে জীবাশ্ম জ্বালানির পরিবর্তে ইথানলকে মোটর ইঞ্জিনের জ্বালানিরূপে ব্যবহার করা হচ্ছে।
অ্যালডিহাইডের ২টি গুরুত্বপূর্ণ ব্যবহার নিম্নরূপ-
১. অ্যালডিহাইড এর পলিমারকরণ বিক্রিয়ায় বিভিন্ন প্লাস্টিক দ্রব্য প্রস্তুত করা হয়।
২. অ্যালডিহাইড তথা ফরমালডিহাইড ও ইউরিয়ার ঘনীভবন পলিমারকরণ বিক্রিয়ায় উৎপন্ন ইউরিয়া-ফরমালডিহাইড রেজিন গৃহের প্লেট, মগ ইত্যাদি তৈরিতে ব্যবহৃত হয়।
মিথানলকে শক্তিশালী জারক দ্বারা জারিত করলে মিথান্যাল পাওয়া যায়। উৎপন্ন মিথান্যালের জলীয় দ্রবণকে অতি নিম্নচাপে উত্তপ্ত করলে ডেরলিন নামক শক্ত পলিমার উৎপন্ন হয়।
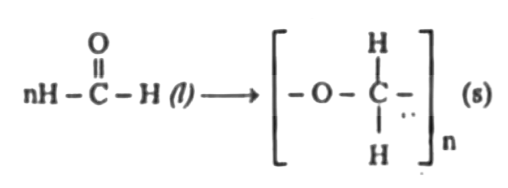
জৈব এসিডের ২টি গুরুত্বপূর্ণ ব্যবহার নিম্নরূপ-
১. লেবুর রস (সাইট্রিক এসিড), দধি (ল্যাকটিক এসিড), চা (ট্যানিক এসিড) ইত্যাদি জৈব এসিডকে আমরা খাবার হিসেবে গ্রহণ করি।
২. জৈব এসিডের ব্যাকটেরিয়া ধ্বংস করার ক্ষমতা থাকায় খাদ্য সংরক্ষক হিসেবে ব্যবহৃত হয়; যেমন ভিনেগার (ইথানয়িক এসিড) সস ও আচার সংরক্ষণের জন্য ব্যবহৃত হয়।
পলিমারকরণ বিক্রিয়ায় যে ছোট অণুগুলো অংশগ্রহণ করে তাদের প্রত্যেকটিকে এক একটি মনোমার (monomer) বলে এবং বিক্রিয়ার ফলে যে বৃহৎ অণু গঠিত হয় তাকে বলে পলিমার অণু। দুটি, তিনটি মনোমার একসাথে যুক্ত হলে তাকে বলে যথাক্রমে ডাইমার (dimer), ট্রাইমার (trimer)। এভাবে অনেকগুলো মনোমার একসাথে যুক্ত হয়ে সৃষ্টি হয় পলিমার। উদাহরণ: প্রোটিন হচ্ছে অ্যামাইনো এসিডের পলিমার।
পলিপ্রোপিন প্রস্তুতি: প্রায় 120°C তাপমাত্রায় উত্তপ্ত টাইটেনিয়াম ট্রাইক্লোরাইড প্রভাবকের উপস্থিতিতে ও 140 atm চাপে হেন্টেন দ্রাবকে দ্রবীভূত প্রোপিলিন বা প্রোপিন এর অসংখ্য অণু যুক্ত হয়ে পলিপ্রোপিন পলিমার গঠন করে।
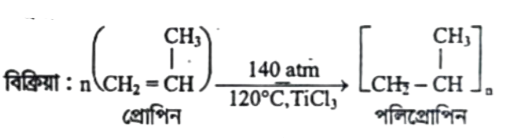
যে বিক্রিয়ায় কোনো পদার্থের অনেকগুলো ক্ষুদ্র অণু পরস্পর যুক্ত হয়ে বৃহৎ অণু গঠন করে সেই বিক্রিয়াকে বলা হয় পলিমারকরণ বিক্রিয়া (Polymerization Reaction) ।
বিক্রিয়ায় অনেকগুলো মনোমার একত্রে সংযুক্ত হয়ে বৃহৎ আকারের অণু তথা পলিমার অণু গঠিত হয়। এ বিক্রিয়ায় যে ছোট অণুগুলো অংশগ্রহণ করে তাদের প্রত্যেকটিকে এক একটি মনোমার (monomer) বলা হয়।
উচ্চতাপ (200 °C) ও উচ্চচাপে (1000 atm) অসংখ্য অ্যালকিন অণু পরস্পরের সাথে যুক্ত হয়ে বৃহৎ অণু গঠন করে; এ বিক্রিয়াটিকে বলা হয় অ্যালকিনের পলিমারকরণ, বিক্রিয়া। যেমন, ইথিলিন অণু থেকে প্রাপ্ত পলিমারকে পলিথিন বলে।

যে পলিমারকরণ বিক্রিয়ায় মনোমার অণুগুলো সরাসার একে অপরের সাথে যুক্ত হয়ে দীর্ঘ শিকলবিশিষ্ট পলিমার গঠন করে তাকে বলা হয় সংযোজন পলিমারকরণ বিক্রিয়া (Addition polymer Reaction)। এ বিক্রিয়ায় গঠিত পলিমারকে বলা হয় সংযোজন 'পলিমার বা যুত পলিমার।
পলিথিন উচ্চ তাপ ও উচ্চ চাপে অসংখ্য অ্যালকিন অণু পরস্পরের সাথে যুক্ত হয়ে বৃহৎ আকৃতির অণু গঠন করে। এ বিক্রিয়ায় উৎপন্ন বৃহৎ অণুকে পলিমার এবং বিক্রিয়াকে পলিমারকরণ বিক্রিয়া বলে। সকল প্লাস্টিক দ্রব্য ও কৃত্রিম তন্তু পলিমারকরণ বিক্রিয়ার মাধ্যমে তৈরি হয়। ইথিলিন অণু থেকে প্রাপ্ত পলিমারকে পলিথিন বলে।

সামান্য পরিমাণ অক্সিজেনের উপস্থিতিতে 1000 atm চাপে ও 200 °C তাপমাত্রায় ইথিনকে উত্তপ্ত করলে পলিথিন উৎপন্ন হয়। এ বিক্রিয়াকে সংযোজন পলিমারকরণ বিক্রিয়া বলা হয়। যেমন-
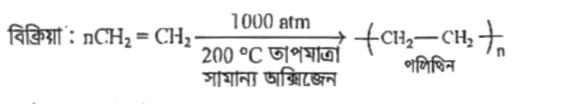
প্রোপিনকে টাইটানিয়াম ক্লোরাইডের উপস্থিতিতে 140 atm চাপে 120 °C তাপমাত্রায় উত্তপ্ত করলে পলিপ্রোপিন উৎপন্ন হয়।
যেমন- বিক্রিয়া
প্রোপিন পলিপ্রোপিন
পলিপ্রোপিনের উল্লেখযোগ্য ২টি বৈশিষ্ট্য নিম্নরূপ-
১. পলিপ্রোপিন পলিথিনের চেয়ে মজবুত ও হালকা।
২. এটি উচ্চতাপ সহ্য করতে পারে, তাই এটি দ্বারা কার্পেট, দড়ি, প্রড়তি তৈরি করা যায়।
PVC হচ্ছে পলি ভিনাইল ক্লোরাইড, যা জৈব পার অক্সাইডের উপস্থিতিতে ডিনাইল ক্লোরাইডকে উচ্চ চাপ ও উচ্চ তাপমাত্রায় উত্তপ্ত করলে পাওয়া যায়।
বিভিন্ন ধরনের পাইপ, তার; এমনকি মেডিকেল ডিভাইস তৈরিতে এই পলিমার বহুল ব্যবহৃত হয়।
পলিমারকরণ বিক্রিয়ায় উচ্চ তাপ ও চাপের প্রভাবে একই যৌগের অসংখ্য ক্ষুদ্র অণু বা মনোমারসমূহ পরস্পরের সাথে যুক্ত হয়ে বৃহৎ আণবিক ভরবিশিষ্ট নতুন যৌগের অণু বা পলিমার গঠন করে। যেমন, উচ্চ ভাপ ও চাপের প্রভাবে ভিনাইল ক্লোরাইড ( = CHCI) যৌগের অসংখ্য অণু পরস্পরের সাথে যুক্ত হয়ে বৃহৎ আণবিক ভরবিশিষ্ট নতুন যৌগ পলিভিনাইল ক্লোরাইড (PVC) গঠন করে।
বিক্রিয়া
ভিনাইল ক্লোরাইডকে জৈব প্যরঅক্সাইডের উপস্থিতিতে উচ্চ চাপ ও তাপমাত্রায় উত্তপ্ত করলে পলিভিনাইল ক্লোরাইড বা পিভিসি (PVC) উৎপন্ন হয়। যেমন-

একই ধরনের একাধিক মনোমারের সমন্বয়ে যে পলিমার গঠিত হয় তাকে যুত পলিমার (Homo Polymer) বলে। PVC (Poly Vinyl Chloride) একটি যুত পলিমার। কারণ এতে মনোমার ডিনাইল ক্লোরাইড ( = CH.CI) কে জৈব পারঅক্সাইড় প্রভাবকের উপস্থিতিতে অধিক চাপ ও উচ্চ তাপমাত্রায় উত্তপ্ত করলে PVC উৎপন্ন হয়।

যে পলিমারকরণ বিক্রিয়ায় মনোমার অণুসমূহ পরস্পরের সাথে যুক্ত হবার সময় ক্ষুদ্র ক্ষুদ্র অণু যেমন: ইত্যাদি অপসারণ করে সেই পলিমাকরণ বিক্রিয়াকে বলা হয়া ঘনীভবন পলিমারকরণ বিক্রিয়া। ঘনীভবন পলিমারকরণ বিক্রিয়ায় নাইলন
নাইলন 6: 6 প্রস্তুতি: টাইটানিয়াম অক্সাইড এর উপস্থিতিতে হেক্সামেথিলিন ডাইঅ্যামিন এর সাথে অ্যাডিপিক এসিড উত্তপ্ত করলে নাইলন 6:6 উৎপন্ন হয়।
বিক্রিয়া:
হেক্সামেথিলিন ডাই অ্যামিন
নাইলন 6:6
প্রাকৃতিকভাবে যেসব পলিমার উৎপন্ন হয় তা হচ্ছে- প্রাকৃতিক পলিমার। যেমন, উদ্ভিদের সেলুলোজ ও স্টার্চ দুটোই প্রাকৃতিক পলিমারের উদাহরণ। রাবার গাছের কষও হচ্ছে প্রাকৃতিক পলিমারের উদাহরণ। আমাদের দেশে বর্তমানে পার্বত্য চট্টগ্রামে, কক্সবাজার, হবিগঞ্জ, সিলেট ও টাঙ্গাইল জেলায় রাবারের ব্যাপক চাষ হচ্ছে।
পলিথিন এর ২টি ধর্ম নিম্নরূপ-
১. পলিথিনকে সহজে কাটা যায় না।
২.. পলিথিন যথেষ্ট টেকসই।
PVC এর ২টি ধর্ম নিম্নরূপ-
১. PVC শক্ত ও কঠিন
২. PVC পলিথিনের তুলনায় কম নমনীয়।
নাইলন 6:6 এর ২টি ব্যবহার নিম্নরূপ-
১. কৃত্রিম কাপড় তৈরিতে ব্যবহৃত হয়।
২. রশি, দাঁতের ব্রাশ তৈরিতে নাইলন 6:6 ব্যাপক ব্যবহৃত হয়।
প্লাস্টিক শব্দটি এসেছে গ্রিক শব্দ Plastikos থেকে। Plastikos এর অর্থ হলো গলানো সম্ভব। প্লাস্টিককে গলানো যায় এবং ছাঁচে ঢেলে যেকোনো আকার দেওয়া যায়। প্লাস্টিক দ্রব্যকে পোড়ালে অনেক রকম বিষাক্ত গ্যাস উৎপন্ন হয়। খাবার রাখার পাত্র, মোড়ক, বলপেন, গামলা, বালতি প্রভৃতি সামগ্রী প্রস্তুতিতে ব্যাপকভাবে প্লাস্টিক ব্যবহৃত হয়।
প্লাস্টিক ব্যবহারের ২টি সুবিধা হলো-
১. প্লাস্টিক জাতীয় পদার্থ থেকে আমাদের নিত্য প্রয়োজনীয় জিনিস যেমন- থালাবাসন, বিভিন্ন ধরনের পাইপ, কন্টেইনার প্রভৃতিপ্রস্তুত করা যায়।
২. প্লাস্টিককে ইচ্ছামতো রূপ দিয়ে বিভিন্ন আকারের জিনিস তৈরি করা যায়।
প্লাস্টিক ব্যবহারের ২টি অসুবিধা হলো-
১. প্লাস্টিক ব্যবহারের বড় অসুবিধা হচ্ছে- এরা পরিবেশের জন্য ক্ষতিকর; একে উত্তপ্ত করলে অনেক রকম বিষাক্ত গ্যাস উৎপন্ন হয়।
২. প্লাস্টিক জাতীয় দ্রব্য মাটিতে বা পানিতে ফেললে তা একই রকম থাকে, ফলে তা মাটি ও পানির দূষণ ঘটায়।
থার্মোসেটিং এবং থার্মোপ্লাস্টিকের মধ্যে ২টি পার্থক্য নিম্নরূপ-
| থার্মোসেটিং | থার্মোপ্লাস্টিক |
| ১. এ ধরনের প্লাস্টিক অধিক শক্ত এবং কম নমনীয়। | ১. এ ধরনের প্লাস্টিক কম শক্ত ও নমনীয়। |
| ২. একবার মাত্র বাঁকানো ও আকার দেওয়া যায়। | ২. একাধিকবার বাঁকানো বা আকার দেওয়া যায়। |
সাধারণত কার্বন ঘটিত যৌগই হচ্ছে জৈব যৌগ। অর্থাৎ, জৈব যৌগে কার্বন (C) অবশ্যই থাকবে। জৈব যৌগের সংখ্যা পৃথিবীতে অনেক বেশি। উদাহরণস্বরূপ: ইথেন , প্রোপেন , মিথানল, অ্যাসিটিক এসিড ইত্যাদি সবই হচ্ছে জৈব যৌগ। এক্ষেত্রে প্রতিটি যৌগেই কার্বন (C) মৌলটি বিদ্যমান রয়েছে।
সাধারণত কার্বনবিহীন যৌগই হচ্ছে অজৈব যৌগ। দু-একটি ব্যতিক্রম ছাড়া অজৈব যৌগে কার্বন থাকে না। পৃথিবীতে অজৈব যৌগের সংখ্যা জৈব যৌগ অপেক্ষা কম। উদাহরণস্বরূপ: সালফার ডাই অক্সাইড , সালফিউরিক এসিড ইত্যাদি হচ্ছে অজৈব যৌগ; যেখানে যৌগদ্বয় C-বিহীন। ব্যতিক্রম: কার্বন ডাইঅক্সাইড অজৈব যৌগ।
জৈব যৌগের দুইটি বৈশিষ্ট্য নিম্নরূপ-
১. জৈব যৌগের বিক্রিয়া সংঘটিত হতে অনেক বেশি সময় নেয়।
২. সমযোজী বন্ধনের মাধ্যমে জৈব যৌগসমূহ গঠিত হয়।
অজৈব যৌগের দুইটি বৈশিষ্ট্য নিম্নরূপ:
১. অজৈব যৌগের বিক্রিয়া সংঘটিত হতে অনেক কম সময় নেয়।
২. অজৈব যৌগসমূহ সাধারণত আয়নিক বা সমযোজী বন্ধনের মাধ্যমে গঠিত হয়।
জৈব এবং অজৈব যৌগের মধ্যে ২টি পার্থক্য নিম্নরূপ:
জৈব যৌগ | অজৈব যৌগ |
১. সাধারণত কার্বন দ্বারা জৈব যৌগ গঠিত। যেমন-মিথেন (CH4)। | ১. কার্বন পরমাণুবিহীন সকল যৌগই অজৈব যৌগ। যেমন- হাইড্রোজেন সালফাইড (H2S) |
২. জৈব যৌগের বিক্রিয়া সম্পন্ন হতে সাধারণত অনেক বেশি সময় লাগে। | ২. অজৈব যৌগের বিক্রিয়া সম্পন্ন হতে সাধারণত অনেক কম সময় লাগে। |
বহু প্রাচীনকালের উদ্ভিদ এবং প্রাণীর মৃতদেহের যে ধ্বংসাবশেষ মাটির নিচে পাওয়া যায় তাকে জীবাশ্ম বলে।
শত শত মিলিয়ন বছর আগের প্রাণী এবং উদ্ভিদ দেহের ধ্বংসাবশেষ মাটির নিচে কয়লা, প্রাকৃতিক গ্যাস ও পেট্রোলিয়াম ইত্যাদি জীবাশ্মরূপে পাওয়া গেছে, যা জ্বালানি হিসেবে ব্যবহার করা হয়- একেই জীবাশ্ম জ্বালানি বলা হয়।
Liquefied Petroleum Gas I
গ্যাসহোল এক প্রকার জ্বালানি, যেখানে পেট্রোলের সাথে 10-20% ইথানল মিশ্রিত থাকে।
কাঠ কয়লা বা কার্বনকে কোক বলে।
পেট্রোলিয়ামের আংশিক পাতনে 71 120 °C তাপমাত্রা অঞ্চল থেকে পৃথকীকৃত পেট্রোলিয়ামের অংশই ন্যাপথা।
পেট্রোলিয়ামের আংশিক পাতনে 121 -170°C তাপমাত্রা অঞ্চল থেকে পৃথকীকৃত অংশকে কেরোসিন বলে।
যে সকল যৌগের কার্যকরী মূলক একই হওয়ায় তাদের ভৌত ও রাসায়নিক ধর্মের গভীর মিল থাকে তারা একই শ্রেণিভুক্ত, এদেরকে সমগোত্রীয় শ্রেণি বলে।
শুধু কার্বন ও হাইড্রোজেন এর সমন্বয়ে গঠিত যৌগসমূহকে
হাইড্রোকার্বন বলে।
যে সকল যৌগের কার্যকরী মূলক একই হওয়ায় তাদের ভৌত ও রাসায়নিক ধর্মের গভীর মিল থাকে তারা একই শ্রেণিভুক্ত, এদেরকে সমগোত্রীয় শ্রেণি বলে।
যে সকল হাইড্রোকার্বনের কার্বন শিকলের দুই প্রান্তের কার্বন দুইটি মুক্ত অবস্থায় থাকে, তাদেরকে মুক্ত শিকল হাইড্রোকার্বন বলে।
যেসব জৈব যৌগ যৌগ গঠনের দিক থেকে সাইক্লিক বা বলয়াকার কিন্তু ধর্মের দিক থেকে অ্যালিফেটিক বা মুক্ত শিকল যৌগের মতো তাদেরকে অ্যালিসাইক্লিক যৌগ বলে।
যে মূলক কোনো যৌগে উপস্থিত থেকে উক্ত যৌগের ধর্ম ও বিক্রিয়া নির্ধারণ করে তাকে কার্যকরী মূলক বলে।
যে সকল জৈব যৌগের অণুতে কার্বন পরমাণুসমূহের মুক্ত শিকল বিদ্যমান তাদেরকে অ্যালিফেটিক যৌগ বলা হয়।
সাইক্লোবিউটেনের সংকেত:
একই আণবিক সংকেতবিশিষ্ট একাধিক যৌগের ধর্ম ভিন্ন হলে তাদেরকে পরস্পরের সমাণু বলে।
যে সকল হাইড্রোকার্বনে কার্বন-কার্বন একক বন্ধন বিদ্যমান তাদেরকে সম্পৃক্ত হাইড্রোকার্বন বলে।
যে সকল হাইড্রোকার্বনের কার্বন শিকলে কার্বন-কার্বন একক বন্ধন বিদ্যমান থাকে তাকে অ্যালকেন বলে।
অ্যালকেন থেকে একটি হাইড্রোজেন (H) পরমাণু অপসারণ করলে যে একযোজী মূলকের সৃষ্টি হয় তাকে অ্যালকাইল মূলক বলে
অ্যালকাইল মূলকের সাধারণ সংকেত হলো
রাসায়নিকভাবে নিষ্ক্রিয় তথা আসক্তিহীন অ্যালকেনকে প্যারাফিন বলা হয়।
যেসব হাইড্রোকার্বনের কার্বন শিকলে অন্তত একটি দ্বি-বন্ধন (=) বা একটি ত্রিবন্ধন (=) থাকে তাদেরকে অসম্পৃক্ত হাইড্রোকার্বন বলে।
যে জৈব যৌগের কার্বন শিকলে অন্তত: একটি কার্বন-কার্বন দ্বিবন্ধন থাকে, তাকে অ্যালকিন বলে।
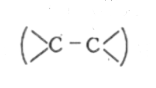
যে জৈব যৌগের কার্বন শিকলে অন্ততঃ একটি কার্বন-কার্বন ত্রিবন্ধন (-C =C-) থাকে তাকে অ্যালকাইন বলে।
নিম্নতর সদস্য বিশিষ্ট যেসব অ্যালকিন ইথিন, প্রোপিন ইত্যাদি হ্যালোজেনের এর সঙ্গে বিক্রিয়া করে তৈলাক্ত পদার্থ উৎপন্ন করে তাকে অলিফিন বলা হয়।
যে জৈব যৌগে তথা অ্যালিফেটিক হাইড্রোকার্বনে হাইড্রোক্সিল মূলক (-OH) বিদ্যমান থাকে তাকে অ্যালকোহল বলে।
যে জৈব যৌগে কার্বক্সিল গ্রুপ (-COOH) বিদ্যমান থাকে তাকে কার্বক্সিলিক এসিড বা জৈব এসিড বা ফ্যাটি এসিড বলে।
ইথানলের 96% জলীয় দ্রবণকে রেকটিফাইড স্পিরিট বলে।
গ্লিসারলের সংকেত: CH-OH
l
CH-OH
ফ্যাটি এসিডের সাধারণত সংকেত
অ্যাডিপিক এসিড এর সংকেত:
যে জৈব যৌগে অ্যালডিহাইড গ্রুপ (CHO) বিদ্যমান থাকে, তাকে অ্যালডিহাইড বলে।
অ্যালডিহাইডের কার্যকরী মূলক- CHO l
ফরমালডিহাইড (HCHO) এর 40% জলীয় দ্রবণকে ফরমালিন বলে।
মিথান্যাল এর জলীয় দ্রবণকে অতি নিম্নচাপে উত্তপ্ত করলে যে পলিমার উৎপন্ন হয়, তাকে ডেলরিন বলা হয়।
ডেলরিনের মনোমার হলো মিথান্যাল (HCHO)।
ইথানয়িক এসিডের 4% থেকে 10% জলীয় দ্রবণকে ভিনেগার (vinegar) বলে।
যে পলিমারকরণ বিক্রিয়ায় মনোমার অণুসমূহ পরস্পরের সাথে যুক্ত হবার সময় ক্ষুদ্র ক্ষুদ্র অণু যেমন: ইত্যাদি অপসারণ করে সেই পলিমাকরণ বিক্রিয়াকে ঘনীভবন পলিমারকরণ বিক্রিয়া বলা হয়।
পলিমারকরণ বিক্রিয়ায় যে ছোট অণুগুলো অংশগ্রহণ করে তাদের প্রত্যেকটিতে এক একটি মনোমার বলে।
যেসব পলিমার সূর্যের আলো এবং প্রাকৃতিকভাবে ব্যাকটেরিয়া জীবাণু দ্বারা বিযোজিত হতে পারে তাদেরকে বায়োডিগ্রেডেবল পদার্থ বলা হয়।
কার্বন ও হাইড্রোজেন দ্বারা গঠিত হাইড্রোকার্বন এবং এদের থেকে উদ্ভূত যৌগসমূহকে জৈব যৌগ বলা হয়।
মেলামাইন পলিমারের মনোমার হলো ইউরিয়া 1
টাইটানিয়াম অক্সাইড এর উপস্থিতিতে হেক্সামিথিলিন ডাইঅ্যামিন এর সাথে অ্যাড়িপিক্ষ এসিড উত্তপ্ত করলে যে যৌগ পাওয়া যায় তাকে নাইলন বলে।
PVC হচ্ছে পলি ভিনাইল ক্লোরাইড, যা জৈব পার অক্সাইডের উপস্থিতিতে ডিনাইল ক্লোরাইডকে উচ্চ চাপ ও উচ্চ তাপমাত্রায় উত্তপ্ত করলে পাওয়া যায়।
পলিমারকরণ বিক্রিয়ায় উৎপন্ন বৃহৎ অণুকে পলিমার বলে।
যে পলিমারকরণ বিক্রিয়ায় মনোমার অণুগুলো সরাসরি একে অপরের সাথে যুক্ত হয়ে দীর্ঘ শিকলবিশিষ্ট পলিমার গঠন করে তাকে সংযোজন পলিমারকরণ বিক্রিয়া বলা হয়।
যে বিক্রিয়ায় কোনো পদার্থের অনেকগুলো ক্ষুদ্র অণু পরস্পর যুক্ত হয়ে বৃহৎ অণু গঠন করে সেই বিক্রিয়াকে পলিমারকরণ বিক্রিয়া (Polymerization Reaction) বলা হয়
কার্বন ও হাইড্রোজেন দ্বারা গঠিত যৌগকে হাইড্রোকার্বন এবং হাইড্রোকার্বন ও এদের জাতকসমূহকে জৈব যৌগ বলে।
অজৈব যৌগ সাধারণত কার্বন (C) বিহীন অন্যান্য মৌলিক উপাদান দিয়ে গঠিত যৌগকে বুঝায়, যা প্রাকৃতিকভাবে বা মানবসৃষ্ট | প্রক্রিয়ায় তৈরি হয়।
উদ্ভিদ ও প্রাণীর মৃতদেহের যে ধ্বংসাবশেষ মাটির নিচে পাওয়া যায় তা জীবাশ্ম l
কয়লার মূল উপাদান কার্বন
উদ্ভিদ ও প্রাণীর মৃতদেহের ধ্বংসাবশেষ মাটির নিচে কীরূপে পাওয়া যায় জীবাশ্মl
কয়লা, প্রাকৃতিক গ্যাস ও পেট্রোলিয়ামকে জীবাশ্ম জ্বালানি বলা হয় l
ফাইটোপ্ল্যাঙ্কটন শৈবাল
জুওপ্ল্যাঙ্কটন ক্ষুদ্র প্রাণীl
মাটির নিচে বড় বড় উদ্ভিদের রাসায়নিক পরিবর্তনে কয়লা সৃষ্টি হয়েছে
ফাইটোপ্ল্যাঙ্কটন ও জুওপ্ল্যাঙ্কটন এর রাসায়নিক পরিবর্তনে পেট্রোলিয়াম সৃষ্টি হয়েছে l
পেট্রোলিয়াম পরিবর্তিত হয়ে প্রাকৃতিক গ্যাস সৃষ্টি হয়েছে l
বাংলাদেশের কোথায় প্রাকৃতিক গ্যাসের সাথে পেট্রোলিয়াম পাওয়া গেছে বাংলাদেশের হরিপুর গ্যাসক্ষেত্রে
জীবাশ্ম জ্বালানির মূল উপাদান কার্বন ও কার্বন যৌগ
প্রাকৃতিক গ্যাসের প্রধান উপাদান মিথেন (80%)
প্রাকৃতিক গ্যাসে ইথেনের শতকরা পরিমাণ 7% l
প্রাকৃতিক গ্যাসে 6% উপাদানের শতকরা পরিমাণ l
বাংলাদেশে প্রাপ্ত প্রাকৃতিক গ্যাসের শতকরা পরিমাণ 99.99% l
প্রাকৃতিক গ্যাসে পেন্টেনের শতকরা পরিমাণ 3% l
শিলাস্তরের মধ্যে 5000 ফুট বা তার বেশি গভীরে পেট্রোলিয়াম পাওয়া যায় l
পেট্রোলিয়ামকে ভূ-পৃষ্ঠের উপরিভাগে উঠে আসতে সাহায্যে করে প্রাকৃতিক গ্যাস l
যে পেট্রোলিয়াম খনি থেকে সরাসরি পাওয়া যায় তাকে অপরিশোধিত তেল বলে l
অপরিশোধিত তেলে সালফার যৌগ যৌগ মিশ্রিত থাকলে তেল দুর্গন্ধযুক্ত হয় l
আংশিক পাতন কলামে পেট্রোলিয়াম গ্যাস অংশের স্ফুটনাঙ্ক 0 °C-20 °C l
সিলিন্ডারে যে LPG ভর্তি করা হয় তা মূলত পেট্রোলিয়াম গ্যাস l
আংশিক পাতন কলামে গ্যাসোলিন অংশের স্ফুটনাঙ্ক l
গ্যাসোলিনের কার্বন সংখ্যা l
পেট্রোলের অপর নাম গ্যাসোলিনl
আংশিক পাতন কলামে ন্যাপথা অংশের স্ফুটনাঙ্ক l
পেট্রোলিয়ামের শতকরা 10 ভাগ ন্যাপথা থাকে l
প্যারাফিন মোম ট্রয়লেট্রিজ এবং ভ্যাসলিন তৈরিতে কাজে ব্যবহৃত হয় l
কার্বন ও হাইড্রোজেন দ্বারা গঠিত যৌগ মূলত হাইড্রোকার্বন নামে পরিচিত l
হাইড্রোকার্বন মূলত দুই প্রকার l
অ্যালিফেটিক কথাটির অর্থ চর্বিজাত l
যৌগটি সম্পৃক্ত মুক্ত শিকল হাইড্রোকার্বন ধরনের হাইড্রোকার্বন l
CH = CH যৌগটি অসম্পৃক্ত মুক্ত শিকল হাইড্রোকার্বন ধরনের হাইড্রোকার্বন l
কার্বন কার্বন দ্বিবন্ধনযুক্ত হাইড্রোকার্বনকে অ্যালকিন বলে l
গ্রিক শব্দ অ্যারোমা শব্দ থেকে অ্যারোমেটিক শব্দটি এসেছে l
অ্যারোমেটিক শব্দের অর্থ সুগন্ধ l
ন্যাপথলিন অ্যারোমেটিক হাইড্রোকার্বন ধরনের যৌগ l
অ্যারোমেটিক যৌগগুলো 5, 6 বা কিংবা 7 সদস্যের সমতলীয় যৌগ l
অ্যারোমেটিক যৌগে কীরূপ বন্ধন থাকে একান্তর দ্বিবন্ধনl
অ্যালকেনের সাধারণ সংকেত
মিথেন, প্রোপেন অ্যালকেন সমগোত্রীয় শ্রেণির অন্তর্গত l
অ্যালকোহলের সাধারণ সংকেত l
কার্বক্সিলিক এসিডের সাধারণ সংকেত l
এর সাধারণ সংকেত
কার্বক্সিলিক এসিড সমগোত্রীয় শ্রেণির অন্তর্গত l
ইথান্যাল, প্রোপান্যাল অ্যালডিহাইড সমগোত্রীয় শ্রেণির অন্তর্গত
অ্যালকেনের সাধারণ সংকেত l
অ্যালকেন যৌগসমূহে কার্বন-কার্বন কীরূপ বন্ধনে আবদ্ধ একক বন্ধনl
অ্যালকেন শ্রেণির ১ম সদস্যের নাম মিথেন
অ্যালকেনের অপর নাম প্যারাফিনl
প্যারাফিন অর্থ আসক্তিহীন l
অ্যালকেনের রাসায়নিক ধর্ম অনেকটা নিষ্ক্রিয় l
তিন কার্বনবিশিষ্ট অ্যালকেনের সংকেত
অ্যালকেন থেকে একটি হাইড্রোজেন পরমাণু অপসারণে অ্যালকাইল মূলক মূলকের সৃষ্টি হয়
ইথাইল মূলকের সংকেত l
7 কার্বন সংখ্যাবিশিষ্ট অ্যালকেনের নাম হেপ্টেন l
10 কার্বনবিশিষ্ট অ্যালকেনের সংকেত (ডেকেন) l
কার্বন ডাইঅক্সাইডের সাথে হাইড্রোজেনের বিক্রিয়ায় মিথেন প্রস্তুতিতে প্রভাবক নিকেল (Ni) l
l বিক্রিয়ায় প্রয়োজনীয় তাপমাত্রা l
বিক্রিয়ায় A যৌগ ইথিন) l
ডিকার্বক্সিলেশন বিক্রিয়ায় মিথেন প্রস্তুতি CaO যৌগের উপস্থিতিতে করা l
ডিকার্বক্সিলেশন বিক্রিয়ায় মিথেন প্রস্তুতি গ্যাসীয় যৌগের উপস্থিতিতে করা হয় l
সম্পৃক্ত হাইড্রোকার্বনের কার্বন সংখ্যা 16 এর বেশি হলে এগুলোর প্রকৃতি অতিবেগুনি রশ্মি (UV) l
5- 15 কার্বন সংখ্যাবিশিষ্ট অ্যালকেনের ভৌত অবস্থা তরল
পেন্টেনের এর স্ফুটনাঙ্ক
অ্যালকিন যৌগে কার্বন-কার্বন কীরূপ বন্ধনে আবদ্ধ দ্বিবন্ধনl
অ্যালকিন কীসের সাথে বিক্রিয়ায় তৈলাক্ত পদার্থ উৎপন্ন করে
অ্যালকিন কীসের সাথে বিক্রিয়ায় তৈলাক্ত পদার্থ উৎপন্ন করে হ্যালোজেনl
তৈলাক্ত পদার্থ উৎপন্ন করায় অ্যালকিনকে অলিফিন বলা হয়l
অলিফিন শব্দটি গ্রিক অলিফিয়েন্ট ভাষা হতে আগত l
প্রোপিনের সংকেত l
বিক্রিয়ায় A যৌগটি (ইথাইল ক্লোরাইড)
ইথানলের সাথে গাঢ় সালফিউরিক এসিড যৌগকে উত্তপ্ত করলে ইথিন উৎপন্ন হয়
অ্যালকিন রাসায়নিকভাবে খুব সক্রিয় হওয়ার কারণ কার্বন-কার্বন দ্বিবন্ধন l
অ্যালকিন কী ধরনের বিক্রিয়ায় অংশগ্রহণ করে সংযোজন বিক্রিয়া l
ইথিনকে হাইড্রোজেনের সাথে কত তাপমাত্রায় উত্তপ্ত করলে ইথেন উৎপন্ন হয় l
বিক্রিয়ার প্রভাবক ফসফরিক এসিড l
পরিবেশ বান্ধব জ্বালানি ইথানল l
ব্রোমিন দ্রবণ হ্যালোজেন দ্রবণ দ্বারা ইথিনের অসম্পৃক্ততা প্রমাণ করা হয়
জারক পদার্থের সাথে পানি বা ক্ষারক পদার্থের বিক্রিয়ায় অস্থায়ী একটি বিচ্ছিন্ন অক্সিজেন পরমাণু সৃষ্টি হয়, তাকে জায়মান অক্সিজেন [O]বলে l
ইথিলিন গ্লাইকল এর সংকেত l
পলিথিনের মনোমার (ইথিন) l
ইথিনের পলিমারকরণ বিক্রিয়ায় প্রয়োজনীয় তাপমাত্রা l
অ্যালকাইনের সাধারণ সংকেত l
অ্যালকাইন কার্বন-কার্বন কীরূপ বন্ধনে আবদ্ধ কার্বন-কার্বন ত্রিবন্ধন l
যৌগটির নাম প্রোপাইন l
বিক্রিয়ায় A যৌগ l
অ্যালকাইনের ত্রিবন্ধনে দুইটি বন্ধন দুর্বল l
ক্যালসিয়াম কার্বাইডের মধ্যে পানি যোগ করলে ক্ষার যৌগটি উৎপন্ন হয় l
ইথাইন থেকে ইথান্যাল প্রস্তুতিতে ইথাইনের সাথে দ্রবণ যোগ করতে হবে l
ইথাইনের মধ্যে ব্রোমিন দ্রবণ যোগ করলে টেট্রাব্রোমো ইথেন যৌগ উৎপন্ন হয় l
অ্যালকোহলকে প্রতীকে প্রকাশ করা হয় l
অ্যালকোহলের কার্যকরী মূলক
অ্যালকোহল শ্রেণির প্রথম সদস্য - OH l
অ্যালকোহল শ্রেণির প্রথম সদস্য মিথানল l
ব্রোমো ইথেন এর সাথে সোডিয়াম হাইড্রোক্সাইড (NaOH) ক্ষারটি যোগ করে উত্তপ্ত করলে ইথানল উৎপন্ন হয়
অ্যালডিহাইড মূলকের সংকেত (CHO-) l
প্রোপান্যাল কোন শ্রেণির অন্তর্গত অ্যালডিহাইড l
B; B যৌগটি l
মিথান্যাল এর 40% ভাগ জলীয় দ্রবণকে ফরমালিন বলে l
ফরমালিনে 60 ভাগ পানি থাকে l
মৃত প্রাণিদেহ সংরক্ষণে ফরমালিন রাসায়নিক করা হয়? পদার্থ ব্যবহার l
জৈব এসিডে -COOH মূলক বিদ্যমান l
জৈব এসিডের সাধারণ সংকেত l
বিক্রিয়া B [O]
ফ্যাটি এসিডসমূহ দুর্বল এসিড ধরনের এসিড l
ইথানয়িক এসিডের 4-10% ভাগ জলীয় দ্রবণকে ভিনেগার বলে
খাদ্য সংরক্ষক হিসেবে ফ্যাটি এসিড বহুল ব্যবহৃত
হাইড্রোজেন পার-অক্সাইড যৌগের উপস্থিতিতে অ্যালকিন হাইড্রোজেন ব্রোমাইডের সাথে বিক্রিয়া করে অ্যালকাইল ব্রোমাইড উৎপন্ন করে l
অ্যালকিনের সাথে জলীয় বাষ্পের বিক্রিয়ায় অ্যালকোহল উৎপাদনে ফসফরিক এসিড এসিডের উপস্থিতি প্রয়োজন
অ্যালকেনকে উচ্চ তাপ ও চাপে বায়ুর অক্সিজেন দ্বারা জারিত করলে জৈব এসিড উৎপন্ন হয়
শিল্পক্ষেত্রে এর ব্যবহার নিরুৎসাহিত করা হয় বিষাক্ত হওয়ায় l
পারফিউম, কসমেটিক ও ওষুধ শিল্পে ইথানল যৌগকে দ্রাবক হিসেবে ব্যবহার করা হয় l
ফার্মাসিউটিক্যাল গ্রেডের রেকটিফাইড স্পিরিট যৌগকে হোমিও ওষুধে ব্যবহার করা হয় l
রেকটিফাইড স্পিরিট ইথানলের 96% জলীয় দ্রবণ l
পারফিউমে ইথানল ব্যবহারের পূর্বে ইথানলকে গন্ধমুক্ত করা হয় l
রেকটিফাইড স্পিরিটে সামান্য মিথানল যোগ করে মেথিলেটেড স্পিরিট তৈরি করা হয়?
কাঠ এবং ধাতুর তৈরি আসবাবপত্র বার্নিশে মেথিলেটেড স্পিরিট ব্যবহার করা হয় l
বর্তমানে ব্রাজিলে মোটর ইঞ্জিনে জীবাশ্ম জ্বালানির পরিবর্তে ইথানল ব্যবহার করা হয়l
স্টার্চ থেকে গাঁজন প্রক্রিয়ায় অ্যালকোহল প্রস্তুত করা l
দেশের চাহিদা পূরণের লক্ষ্যে বাংলাদেশের দর্শনায় কেরু এন্ড কেরু কোম্পানি কোম্পানিতে ইথানল প্রস্তুত করা হয় l
মিথান্যাল যৌগ থেকে ডেরালিন প্রস্তুত করা হয়
চেয়ার, টেবিল, বালতি ইত্যাদি প্রস্তুতিতে ডেরালিন পলিমার ব্যবহার করা হয়l
জৈব এসিডকে খাদ্য সংরক্ষক হিসেবে ব্যবহারের কারণ ব্যাকটেরিয়া ধ্বংস l
লেবুর রসে সাইট্রিক এসিড এসিড থাকে l
দধিতে ল্যাকটিক এসিড এসিড থাকে l
ইথানয়িক এসিডের শতকরা 6% থেকে 10% ভাগ জলীয় দ্রবণ ভিনেগারl
তিনটি মনোমার অণু একসাথে যুক্ত হলে তাকে ট্রাইমার বলে l
প্রোটিনের মনোমার অণু অ্যামাইনো এসিড l
গঠন প্রকৃতি অনুযায়ী পলিমার দুই প্রকার l
পলিথিন প্রস্তুতি সংযোজন ধরনের পলিমারকরণ বিক্রিয়া l
পলিপ্রোপিন প্রস্তুতিতে বায়ুমণ্ডলীয় চাপ ও তাপমাত্রা l
পাইপ, কার্পেট তৈরিতে পলিপ্রোপিন পলিমার ব্যবহার করা হয় l
পলিপ্রোপিন প্রস্তুতিতে প্রভাবক হিসেবে টাইটানিয়াম ক্লোরাইড ব্যবহার করা হয় l
পিভিসি এর মনোমার যৌগ ভিনাইল ক্লোরাইড
নাইলন 6:6 পলিমার উৎপাদন ঘনীভবন পলিমারকরণ ধরনের বিক্রিয়া l
অ্যাডিপিক এসিডের সংকেত l
উৎসের ভিত্তিতে পলিমার দুই প্রকার l
রাবার গাছের কষ প্রাকৃতিক পলিমার ধরনের পলিমার l
সেলুলোজ ও স্টার্চ এর মনোমার অণু গ্লুকোজ l
দাঁতের ব্রাশ তৈরিতে নাইলন পলিমার ব্যবহার করা হয় l
পানির পাইপ তৈরিতে পলিভিনাইল ক্লোরাইড (PVC)পলিমার ব্যবহার করা হয় l
প্লাস্টিকের ক্ষতিকর প্রভাব থেকে পরিবেশকে রক্ষা করতে আমাদের করণীয় প্লাস্টিকের পুনঃপ্রক্রিয়াজাতকরণ l
প্লাস্টিক জাতীয় দ্রব্যের সবচেয়ে বড় অসুবিধা পরিবেশের জন্য ক্ষতিকর l
এ পৃথিবীর বয়স প্রায় 4.54 বিলিয়ন বছর। আজকে পৃথিবীকে যেমন দেখছো, অনেক অনেক বছর আগে পৃথিবীর রূপ কিন্তু এমন ছিল না। আজ থেকে 500 বা 600 মিলিয়ন বছর আগে এই পৃথিবী ছিল ঘন বনজঙ্গল, নিচু জলাভূমি আর সাগর-মহাসাগরে পরিপূর্ণ। প্রাকৃতিক বিপর্যয়ে ধ্বংসপ্রাপ্ত মৃত প্রাণী, উদ্ভিদ, শৈবাল-ছত্রাক নিচু এলাকাগুলোতে জমা হয়েছিল। তার উপর পড়তে থাকল পলির আস্তরণ। এভাবে মিলিয়ন মিলিয়ন বছর ধরে এ সকল উদ্ভিদ আর প্রাণীর দেহাবশেষের উপর হাজার হাজার ফুট মাটি, বিভিন্ন শিলার আস্তরণ হয়ে গেল। উচ্চচাপ, উচ্চ তাপমাত্রা, মিলিয়ন মিলিয়ন বছর ধরে বিভিন্ন ভৌত আর রাসায়নিক পরিবর্তন ঘটে কয়লা, পেট্রোলিয়াম আর প্রকৃতিক গ্যাস সৃষ্টি হলো৷ এদেরকে বলে জীবাশ্ম জ্বালানি। কয়লার মূল উপাদান কার্বন। আর পেট্রোলিয়ামের মূল উপাদান শুধু কার্বন ও হাইড্রোজেনের দ্বারা সৃষ্ট যৌগ হাইড্রোকার্বন। হাইড্রোকার্বন হলো জৈব যৌগ। অ্যালকোহল, অ্যালডিহাইড, কিটোন, কার্বক্সিলিক এসিডসহ আরও যে সকল জৈব যৌগ আছে তারা মূলত হাইড্রোকার্বন থেকেই সৃষ্ট। এগুলো নিয়েই এ অধ্যায়ে আলোচনা করা হবে।
এ অধ্যায় পাঠ শেষে আমরা
- জীবাশ্ম জ্বালানির ধারণা ব্যাখ্যা করতে পারব।
- পেট্রোলিয়ামকে জৈব যৌগের মিশ্রণ হিসেবে ব্যাখ্যা করতে পারব।
- পেট্রোলিয়ামের ব্যবহার ব্যাখ্যা করতে পারব।
- হাইড্রোকার্বনের ধরন ও শ্রেণিবিভাগ ব্যাখ্যা করতে পারব।
- সম্পৃক্ত ও অসম্পূৰ্ণ হাইড্রোকার্বনের প্রস্তুতির বিক্রিয়া ও ধর্ম ব্যাখ্যা এবং এদের মধ্যে পার্থক্য করতে পারব।
- প্লাস্টিক দ্রব্য ও ভন্ড্রু তৈরির রাসায়নিক বিক্রিয়া এবং এর ব্যবহার বর্ণনা করতে পারব।
- পরিবেশের ওপর প্লাস্টিক দ্রব্য অপব্যবহারের কুফল উল্লেখ করতে পারব।
- প্রাকৃতিক গ্যাস, পেট্রোলিয়াম এবং কয়লা ব্যবহারের সুবিধা, অসুবিধা ও ব্যবহারের কৌশল ব্যাখ্যা করতে পারব।
- হাইড্রোকার্বন থেকে অ্যালকোহল অ্যালডিহাইড ও জৈব এসিডের প্রস্তুতির কৌশল ব্যাখ্যা করতে পারব।
- অ্যালকোহল, অ্যালডিহাইড ও জৈব এসিডের ব্যবহার করতে পারব।
- পরিবেশের উপর প্লাস্টিক দ্রব্যের প্রভাব সম্পর্কিত অনুসন্ধানমূলক কাজ করতে পারব।
- পরীক্ষার মাধ্যমে জৈব ও অজৈব যৌগের মধ্যে পার্থক্য করে দেখাতে পারব।
- জীবাশ্ম জ্বালানির সঠিক ব্যবহার সম্পর্কে সচেতনতা প্রদর্শন করতে পারব।
Related Question
View Allপেট্রোলিয়ামের প্রধান উপাদান হলো হাইড্রোকার্বন।
অ্যালকেনসমূহ কার্বন-কার্বন ও কার্বন-হাইড্রোজেন শক্তিশালী একক সমযোজী বন্ধনের মাধ্যমে গঠিত হয়। এরা রাসায়নিকভাবে আসক্তিহীন বা প্যারাফিন নামে পরিচিত। এ কারণে অ্যালকেনসমূহ সাধারণত রাসায়নিক বিক্রিয়ায় অংশগ্রহণ করে না অর্থাৎ কম সক্রিয় জৈব যৌগ। পক্ষান্তরে অ্যালকিনসমূহের অণুতে কার্বন-কার্বন দ্বি-বন্ধন বিদ্যমান থাকে। কার্বন-কার্বন দ্বি-বন্ধনের প্রথমটি সিগমা বন্ধন হওয়ায় প্রথম বন্ধনটি শক্তিশালী হলেও দ্বিতীয় বন্ধটি পাই (গ) বন্ধন হওয়ায়, তুলনামূলকভাবে দ্বিতীয় বন্ধনটি প্রথম বন্ধন অপেক্ষা দুর্বল হয়। তাই পাই (গ) বন্ধনটির সহজে ভাঙ্গন ঘটে। ফলে এরা সংযোজন, পলিমারকরণ, দহন বিক্রিয়ায় অংশগ্রহণ করে। তাই অ্যালকিন রাসায়নিকভাবে অ্যালকেন অপেক্ষা সক্রিয় হয়।
আলুতে প্রচুর পরিমাণে স্টার্চ আছে। উদ্দীপকে বিদ্যমান বিক্রিয়ার মাধ্যমে স্টার্চ থেকে গ্লুকোজ ও গ্লুকোজকে জাইমেজ এনজাইমের উপস্থিতিতে ইথানলে রূপান্তরিত করা হয়। প্রাপ্ত ইথানলকে এসিডযুক্ত পটাসিয়াম ডাইক্রোমেট অথবা পটাসিয়াম পারম্যাঙ্গানেট দ্বারা জারিত করলে প্রথমে ইথান্যাল (অ্যাসিট্যালডিহাইড) ও পরে ইথানয়িক এসিড উৎপন্ন হয়।
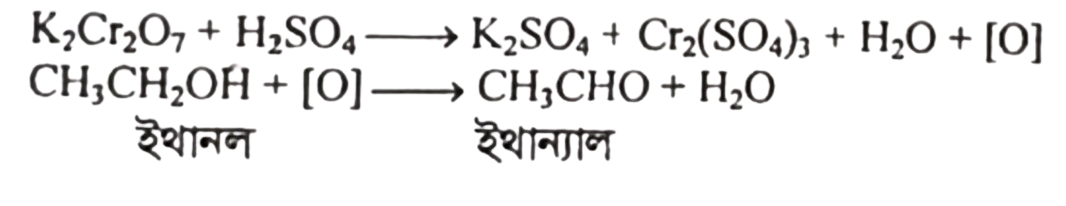
CH3CHO + [O] CH3COOH ইথানয়িক এসিড
এভাবে উৎপন্ন ইথানয়িক এসিডকে NaOH এর সাথে মিশ্রিত করলে সোডিয়াম ইথানয়েট উৎপন্ন হয়।
CH3COOH + NaOH → CH3COONa + H2O সোডিয়াম ইথানয়েট
এখানে প্রাপ্ত সোডিয়াম ইথানয়েটকে (CH3COONa) সোডালাইম (NaOH + CaO এর মিশ্রণ) সহ উত্তপ্ত করলে মিথেন (CH4) পাওয়া যায়।
বিক্রিয়া: CH3COONa CH4 + Na2CO3
এভাবে আমরা আলু থেকে মিথেন (CH4) প্রস্তুত করতে পারি।
আলুতে প্রচুর পরিমাণ স্টার্চ থাকে। অতিরিক্ত আলুতে বিদ্যমান স্টার্চ থেকে আমরা নিম্নলিখিত উপায়ে ইথানল প্রস্তুত করতে পারি যা বিকল্প জ্বালানি হিসেবে ব্যবহার করা যায়।
আলুকে প্রথমে সিদ্ধ করে কাই (Paste) এ পরিণত করা হয়। একে ম্যাস (mash) বলে। এ ম্যাসের সাথে মল্ট মিশ্রিত করে মিশ্রণটি প্রায় 45°C তাপমাত্রায় এক ঘন্টা রেখে দিলে মল্ট থেকে নিঃসৃত "ডায়াস্টেজ” নামক এক প্রকার এনজাইম দ্বারা স্টার্চ আর্দ্র বিশ্লেষিত হয়ে মল্টোজে পরিণত হয়।
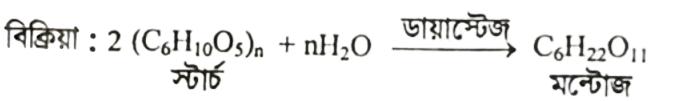
মল্টোজকে 20°C তাপমাত্রায় শীতল করে পানিযোগে লঘু (10%) করে ইস্ট যোগ করলে, ইস্ট থেকে নিঃসৃত ম্যালটেজ এনজাইম মল্টোজকে গ্লুকোজে এবং পরবর্তীতে জাইমেজ নামক এনজাইম গ্লুকোজকে ফারমেন্টেশন করে ইথানলে পরিণত করে।
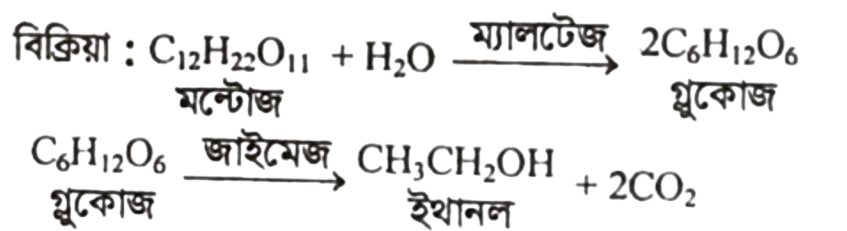
আলু থেকে এভাবে প্রাপ্ত ইথানল পৃথিবীর বিভিন্ন দেশে জীবাশ্ম জ্বালানির পরিবর্তে মটর ইঞ্জিন, বিমান, বাস, ট্রাক, কলকারখানায় বিকল্প জ্বালানিরূপে ব্যবহার করা হচ্ছে। পেট্রোলের সাথে (10-20%) ইথানল মিশ্রিত করে গ্যাসহোল (Gasohol) নামক জ্বালানি তৈরী করা হয়েছে, যা বিভিন্ন দেশে জ্বালানিরূপে ব্যবহৃত হয়ে আসছে।
CH3CH2OH + O2 → 2CO2 + 6H2O + তাপশক্তি
যেহেতু অ্যালকোহল থেকে আমরা প্রচুর পরিমাণ তাপশক্তি পাই, তাই অতিরিক্ত আলু থেকে ইথানল উৎপন্ন করে জীবাশ্ম জ্বালানির বিকল্প হিসেবে ব্যবহার সম্ভব।
হাইড্রোজেন ও কার্বন দ্বারা গঠিত দ্বি-মৌল যৌগসমূহকে হাইড্রোকার্বন বলা হয়।
অ্যারোমেটিক যৌগগুলোতে সাধারণত 5, 6 কিংবা 7 সদস্যের সমতলীয় যৌগ এবং এগুলোতে একান্তর দ্বিবন্ধন থাকে। বেনজিন ছয় সদস্যের সমতলীয় চাক্রিক যৌগ। এতে একান্তর দ্বিবন্ধন বিদ্যমান। অর্থাৎ পর্যায়ক্রমে কার্বন-কার্বন একটি একক বন্ধন এবং একটি দ্বিবন্ধন থাকে। তাই
বেনজিন  একটি অ্যারোমেটিক হাইড্রোকার্বন।
একটি অ্যারোমেটিক হাইড্রোকার্বন।
১ ক্লিকে প্রশ্ন, শীট, সাজেশন ও
অনলাইন পরীক্ষা তৈরির সফটওয়্যার!
শুধু প্রশ্ন সিলেক্ট করুন — প্রশ্নপত্র অটোমেটিক তৈরি!


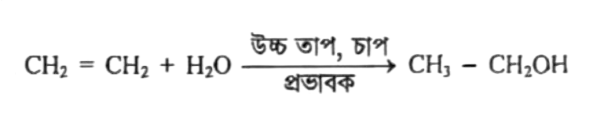 বিক্রিয়ার প্রভাবক কোনটি?
বিক্রিয়ার প্রভাবক কোনটি?
