এক মোল পরিমাণ পদার্থের আয়তন 22.4 এবং এই আয়তনকে মোলার আয়তন বলে।
Na মৌলের পরমাণুর পারমাণবিক সংখ্যা 11 এবং এর ইলেকট্রন বিন্যাস-
Na(11) - বা, [Ne]
Na পরমাণু এর 3s অরবিটালে ইলেকট্রনটির দান করে N a^ + আয়নে পরিণত হয় এবং স্থায়ী নিষ্ক্রিয় মৌলের ইলেকট্রনীয় গঠন কাঠামো প্রাপ্ত হয়।
Na মৌলের বিভবের মান 495.8 kJ mol-1 । এ অবস্থায় আয়ন সম্পূর্ণ অষ্টক অবস্থা প্রাপ্ত হয় এবং নিষ্ক্রিয় মৌল Ne এর গঠন কাঠামো প্রাপ্ত হয়। অবস্থা হতে আরও একটি ইলেকট্রনকে অপসারিত করতে উচ্চ আয়নিকরণ বিভবের প্রয়োজন হয়। Na এর ২য় আয়নিকরণ বিভবের মান 4562. kJ mol-1 । এ উচ্চ আয়নিকরণ বিভবের মানের কারণে আয়ন গঠিত হয় না।
উদ্দীপকের C3H8 যৌগটি হলো প্রাপেন। তিনটি কার্বন পরমাণুর সাথে ৪টি হাইড্রোজেন পরমাণু যুক্ত হয়ে গঠিত হয়েছে C₂H₃। C3H8 যৌগে কার্বনের পরমাণু তিনটি একে অপরের সাথে শিকল আকারে যুক্ত হয়। শিকলটি নিম্নরূপ:
C-C-C
কার্বনের অবশিষ্ট যোজনীগুলো হাইড্রোজেন দ্বারা পূর্ণ হয়ে প্রতিটি কার্বনের যোজনী 4 হয়। তাহলে C3H8 যৌগটি গাঠনিক সংকেত হলো:
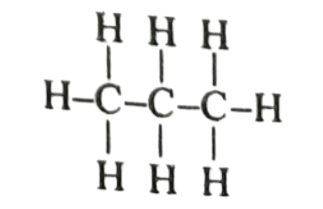
এখানে উল্লেখ্য যে, কার্বন পরমাণুটি উক্ত যৌগের গাঠনিক সংকেতে কেন্দ্রে অবস্থান করে এবং সকল হাইড্রোজেন পরমাণু শাখা পরমাণু হিসাবে সংযুক্ত হয়। কার্বন ও হাইড্রোজেনের যোজনী যথাক্রমে 4 ও 1 বজায় থাকে।
উদ্দীপকের এর গাঠনিক সংকেত যথাক্রমে নিম্নরূপ:
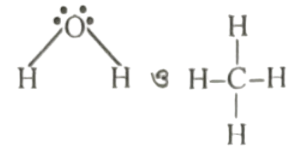
এখানে অণুতে একটি অক্সিজেন পরমাণুর সাথে দুইটি হাইড্রোজেন পরমাণু যুক্ত হয়েছে। অক্সিজেন হলো কেন্দ্রীয় পরমাণু এবং হাইড্রোজেন হলো শাখা পরমাণু। অক্সিজেন পরমাণুতে দুই জোড়া মুক্ত জোড়া ইলেকট্রন রয়েছে যা O-H বন্ধন জোড় ইলেকট্রনকে বিকর্ষণ করে। যার ফলে H-O-H এর বন্ধন কোণ 180 deg বা সরল কোণ না হয়ে 104.5 deg হয়। তাই এর গঠন হলো উল্টা "V" এর অনুরূপ।
আবার অণুতে একটি কার্বন পরমাণুর সাথে চারটি হাইড্রোজেন পরমাণু যুক্ত রয়েছে। কার্বন পরমাণু হলো কেন্দ্রীয় এবং শাখা পরমাণু হলো হাইড্রোজেন। কার্বন পরমাণুতে কোনো মুক্ত জোড় ইলেকট্রন নেই। যার ফলে চারটি C-H বন্ধন পরস্পরকে সমানভাবে বিকর্ষণ করে চতুস্তলকীয় আকার গঠন করে এবং H-C-H বন্ধন কোণ হয় 109.5 deg । .. সুতরাং ও এর গাঠনিক সংকেত থেকে জ্যামিতিক রূপ ।
যথাক্রমে কৌণিক ও চতুস্তলকীয় বোঝা গেলো। তাই বলা যায় কোনো যৌগে পরমাণুগুলো কীভাবে সাজানো রয়েছে তা গাঠনিক সংকেত থেকে স্পষ্টতভাবেই জানা সম্ভব।
Related Question
View All১ ক্লিকে প্রশ্ন, শীট, সাজেশন ও
অনলাইন পরীক্ষা তৈরির সফটওয়্যার!
শুধু প্রশ্ন সিলেক্ট করুন — প্রশ্নপত্র অটোমেটিক তৈরি!



