অ্যামোনিয়া দ্রবণ মিশ্রিত সিলভার নাইট্রেটের বর্ণহীন দ্রবণকে টলেন বিকারক বলে।
যে তাপমাত্রায় কোনো পদার্থ কঠিন থেকে তরলে পরিণত হয় তাকে ঐ পদার্থের গলনাঙ্ক বলে। আবার যে তাপমাত্রায় কোনো পদার্থ তরল থেকে বাষ্পে পরিণত হয় তাকে ঐ পদার্থের স্ফুটনাঙ্ক বলে। কঠিন পদার্থের অণুসমূহের মধ্যে আন্তঃআণবিক দূরত্ব অনেক কম। পদার্থটি তরলে পরিণত হলে এ দূরত্ব বাড়ে, আবার বাষ্পে পরিণত হলে দূরত্ব অনেক বেড়ে যায়। তাই কঠিন থেকে তরলে পরিণত করার সময় আন্তঃআণবিক দূরত্ব অল্প বৃদ্ধি করার জন্য যে তাপের প্রয়োজন হয়, গ্যাসে পরিণত করার সময় অনেক বেশি তাপের প্রয়োজন হয়। কারণ এক্ষেত্রে আন্তঃআণবিক দূরত্ব অনেক বেশি বৃদ্ধি করতে হয়। তাই বলা যায়, একই পদার্থের গলনাঙ্ক অপেক্ষা স্ফুটনাঙ্ক বেশি হয়।
A মৌলটির পারমাণবিক সংখ্যা হলো 19। তাই এটি হলো পটাসিয়াম মৌল। D মৌলটির পারমাণবিক সংখ্যা হলো 9। তাই এটি হলো ফ্লোরিন মৌল।
পটাসিয়াম ক্ষার ধাতু এবং ফ্লোরিন অত্যন্ত সক্রিয় অধাতু।
ধাতুসমূহ ইলেকট্রন ত্যাগ এবং অধাতুসমূহ ধাতু কর্তৃক বর্জনকৃত ইলেকট্রন গ্রহণ করে যথাক্রমে ইলেকট্রন গ্রহণ করে যথাক্রমে ক্যাটায়ন ও অ্যানায়ন গঠন করে।
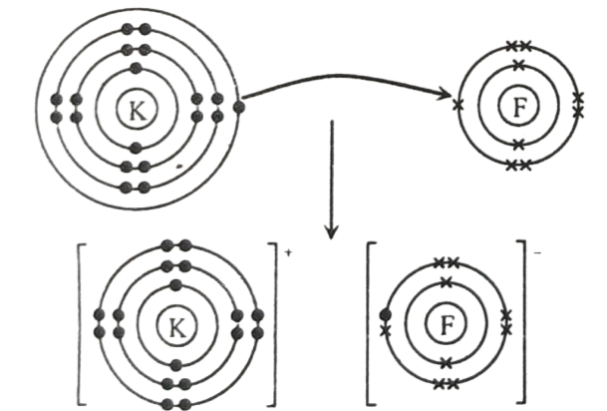
পটাসিয়াম ও ফ্লোরিনের সংযোগে পটাসিয়াম ফ্লোরাইডের গঠনঃ
নিকটতম নিষ্ক্রিয় গ্যাস, আর্গন পরমাণুর (18Ar) ইলেকট্রন বিন্যাস লাভের চেষ্টায় K পরমাণু তার সর্ববহিঃস্থ কক্ষের 4s অরবিটালের ইলেকট্রনটি ত্যাগ করে K+ আয়নে পরিণত হয়। অন্যদিকে, ফ্লোরিন তার নিকটতম নিস্ক্রিয় গ্যাস, নিয়ন (10Ne) পরমাণুর ইলেকট্রন বিন্যাস লাভের চেষ্টায় ঐ বর্জিত ইলেকট্রনটি গ্রহণ করে F আয়নে পরিণত হয়। এভাবে উৎপন্ন দুটি বিপরীত তড়িৎগ্রস্থ আয়ন পরস্পরের সঙ্গে স্থির তড়িৎ আকর্ষণে যুক্ত হয়ে পটাশিয়াম ফ্লোরাইড (KF) যৌগ গঠন করে।
অক্সজেনের মৌলিক অণু গঠন: অক্সিজেনে ইলেকট্রন বিন্যাস:
ইলেকট্রন বিন্যাস হতে দেখা যায়, এর যোজ্যতা স্তরের ইলেকট্রন সংখ্যা 6, অযুগ্ম e- 2 টি এবং নিকটবর্তী নিষ্ক্রিয় গ্যাস নিয়নের চেয়ে দুটি ইলেকট্রন কম আছে। তাই একটি অক্সিজেন পরমাণু অপর একটি অক্সিজেন পরমাণুর সাথে দুটি করে ইলেকট্রন শেয়ার করে অক্সিজেন অণু গঠন করে। ফলে অক্সিজেন অণুতে দ্বিবন্ধন দেখা যায়।
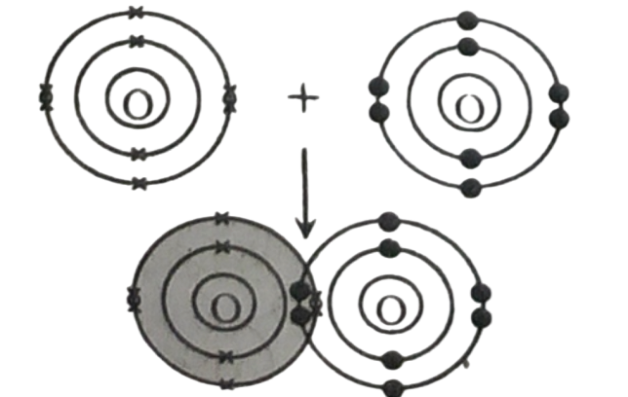
চিত্র: ইলেকট্রন শেয়ারের মাধ্যমে O2 মৌলিক অণুর গঠন
উদ্দীপকের তথ্যমতে A, D ও E মৌল তিনটি যথাক্রমে পটাসিয়াম (K), ফ্লোরিন (F) ও অক্সিজেন (O)। এক্ষেত্রে F ও O মৌল দুটি যথাক্রমে F2 ও O2 মৌলিক অণু গঠন করে। নিম্নে বিশ্লেষণ করা হলো-
ফ্লোরিনের মৌলিক অণু গঠন: ফ্লোরিনের ইলেকট্রন বিন্যাস,
ইলেকট্রন বিন্যাস হতে দেখা যায়, দুটি ফ্লোরিন পরমাণুর প্রতিটিতে টি যোজনী ইরেকট্রন রয়েছে যার মধ্যে একটি করে অযুগ্ম ইলেকট্রন বিদ্যমান। এজন্য দুটি ফ্লোরিন পরমাণু তাদের অযুগ্ম ইলেকট্রন শেয়ার করে একটি ইলেকট্রন যুগল সৃষ্টি করে। ফলে উভয় ফ্লোরিন পরমাণুর সর্ববহিঃস্থ স্তরে পৃথকভাবে আটটি করে ইলেকট্রন (নিয়নের অনুরূপ) পাওয়া সম্ভব হয়। এভাবে দুটি ফ্লোরিন পরমাণুর মধ্যে সমযোজী একক বন্ধন সৃষ্টি হয় এবং দ্বিপরমাণুক ফ্লোরিন অণু (F2) গঠিত হয়।
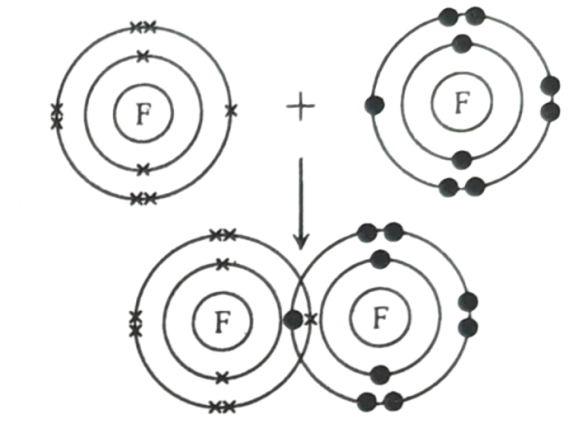
চিত্র: ইলেকট্রন শেয়ারের মাধ্যমে F2 মৌলিক অণুর গঠন।
সুতরাং উদ্দীপকের দুটি মৌল অক্সিজেন ও ফ্লোরিন যথাক্রমে মৌলিক অণু O2 ও F2 গঠন করে।
Related Question
View All১ ক্লিকে প্রশ্ন, শীট, সাজেশন ও
অনলাইন পরীক্ষা তৈরির সফটওয়্যার!
শুধু প্রশ্ন সিলেক্ট করুন — প্রশ্নপত্র অটোমেটিক তৈরি!



