A মৌলটির পারমাণবিক সংখ্যা হলো 19। তাই এটি হলো পটাসিয়াম মৌল। D মৌলটির পারমাণবিক সংখ্যা হলো 9। তাই এটি হলো ফ্লোরিন মৌল।
পটাসিয়াম ক্ষার ধাতু এবং ফ্লোরিন অত্যন্ত সক্রিয় অধাতু।
ধাতুসমূহ ইলেকট্রন ত্যাগ এবং অধাতুসমূহ ধাতু কর্তৃক বর্জনকৃত ইলেকট্রন গ্রহণ করে যথাক্রমে ইলেকট্রন গ্রহণ করে যথাক্রমে ক্যাটায়ন ও অ্যানায়ন গঠন করে।
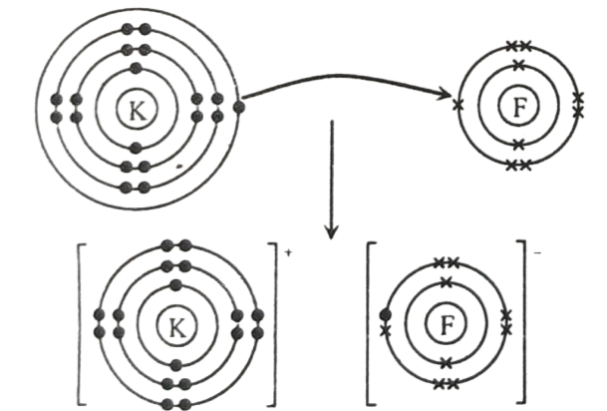
পটাসিয়াম ও ফ্লোরিনের সংযোগে পটাসিয়াম ফ্লোরাইডের গঠনঃ
নিকটতম নিষ্ক্রিয় গ্যাস, আর্গন পরমাণুর (18Ar) ইলেকট্রন বিন্যাস লাভের চেষ্টায় K পরমাণু তার সর্ববহিঃস্থ কক্ষের 4s অরবিটালের ইলেকট্রনটি ত্যাগ করে K+ আয়নে পরিণত হয়। অন্যদিকে, ফ্লোরিন তার নিকটতম নিস্ক্রিয় গ্যাস, নিয়ন (10Ne) পরমাণুর ইলেকট্রন বিন্যাস লাভের চেষ্টায় ঐ বর্জিত ইলেকট্রনটি গ্রহণ করে F আয়নে পরিণত হয়। এভাবে উৎপন্ন দুটি বিপরীত তড়িৎগ্রস্থ আয়ন পরস্পরের সঙ্গে স্থির তড়িৎ আকর্ষণে যুক্ত হয়ে পটাশিয়াম ফ্লোরাইড (KF) যৌগ গঠন করে।
Related Question
View All১ ক্লিকে প্রশ্ন, শীট, সাজেশন ও
অনলাইন পরীক্ষা তৈরির সফটওয়্যার!
শুধু প্রশ্ন সিলেক্ট করুন — প্রশ্নপত্র অটোমেটিক তৈরি!



