সর্বপ্রথম মৌলিক পদার্থসমূহকে ধাতু ও অধাতুতে বিভক্ত করেন বিজ্ঞানী ল্যাভয়সিয়ে ।
ল্যাভয়সিয়ে 1789 সালে মৌলিক পদার্থসমূহকে ধাতু ও অধাতুতে বিভক্ত করেন।
ডোবেরাইনারের ত্রয়ীসূত্র আবিষ্কৃত হয় 1829 সালে ।
ত্রয়ীসূত্রে তিনটি করে মৌল সাজানো হয়।
প্রথম ত্রয়ী মৌল ক্লোরিন, ব্রোমিন, আয়োডিন।
অষ্টক সূত্র প্রদান করেন বিজ্ঞানী নিউল্যান্ড।
নিউল্যান্ড এর অষ্টক সূত্র আবিষ্কৃত হয় 1864 সালে ।
মেন্ডেলিফের পর্যায় সূত্রের মূল ভিত্তি পারমাণবিক ভর ।
মৌলসমূহের পারমাণবিক, ভরের ভিত্তিতে পর্যায় সূত্র আবিষ্কার করেন বিজ্ঞানী মেন্ডেলিফ।
মেন্ডেলিফের পর্যায় সারণিতে 12 টি সারি ও ৪টি কলাম অনুভূমিক সারি ও খাড়া কলাম রয়েছে।
পর্যায় সারণিতে কিছু মৌলিক পদার্থের অস্তিত্ব সম্পর্কে ভবিষ্যদ্বাণী করেন বিজ্ঞানী মেন্ডেলিফ।
মোসলে প্রদত্ত পর্যায় সূত্রের মূল ভিত্তি ছিল পারমাণবিক সংখ্যা।
IUPAC এখন পর্যন্ত 118 টি মৌলিক পদার্থ শনাক্ত করেছে।
মাত্র 33 টি মৌল নিয়ে ছক তৈরির কাজ শুরু করেছিলেন ল্যাভয়সিয়ে।
মেন্ডেলিফ 4 টি অনাবিষ্কৃত মৌল নিয়ে পর্যায় সারণি তৈরি করেছিলেন।
মেন্ডেলিফ 63 টি আবিষ্কৃত মৌল নিয়ে পর্যায় সারণি তৈরি করেছিলেন।
পর্যায় সারণির খাড়া কলামগুলোকে গ্রুপ বা শ্রেণি বলে ।
পর্যায় সারণির বাম থেকে ডান পর্যন্ত বিস্তৃত সারিগুলোকে পর্যায় বলে।
আধুনিক পর্যায় সারণিতে 7 টি পর্যায় রয়েছে ।
আধুনিক পর্যায় সারণিতে 1৪ টি গ্রুপ রয়েছে ।
পর্যায় সারণিতে গ্রুপ বামদিক থেকে শুরু হয়।
পর্যায় সারণিতে ল্যাম্বানাইড সারির অবস্থান 6 নং পর্যায়ে ।
পর্যায় সারণিতে অ্যাকটিনাইড সারির অবস্থান 7 নং পৃর্যায়ে ।
পর্যায় I এ 2 টি মৌল রয়েছে।
পর্যায় 2 এবং পর্যায় 3 এ এ ৮টি করে মৌল রয়েছে ।
পর্যায় 4 এবং 1 এ ৪ টি করে মৌল রয়েছে ।
পর্যায় 6 এবং 7 এ 32 টি করে মৌল রয়েছে ।
গ্রুপ 3 এ 32 টি মৌল রয়েছে ।
গ্রুপ 7 টি এ কয়টি মৌল রয়েছে ।
ল্যান্থানাইড সারিতে 57 থেকে 71 পারমাণবিক সংখ্যাবিশিষ্ট মৌলের অবস্থান
অ্যাকটিনাইড সারিতে ৮৯ - ১০৩ পারমাণবিক সংখ্যাবিশিষ্ট মৌলের অবস্থান ।
একই পর্যায়ে বাম থেকে ডানের দিকে মৌলসমূহের ধর্ম ক্রমান্বয়ে পরিবর্তিত হয় ।
প্রায় অভিন্ন
পর্যায় সারণিতে গ্রুপ 13-17 পর্যন্ত প্রত্যেকটিতে 6 টি করে মৌল রয়েছে।
I উপস্তরের মৌলসমূহকে পর্যায় সারণির পৃথকভাবে স্থান দেয়া হয়েছে.
পর্যায় সারণির 17 নং গ্রুপের মৌলের সংখা 5 টি।
লিথিয়ামের ইলেকট্রন সংখ্যা 3।
লিথিয়ামের বাইরের শক্তিস্তরে মোট কতটি ইলেকট্রন আছে।
1s22s22p63s23p64sI কোন মৌলের ইলেকট্রন বিন্যাস?
পটাসিয়াম ৪র্থ পর্যায়ের মৌল ।
গ্রুপ সংখ্যা নির্ণয়ে' ও অরবিটালের ইলেকট্রনের সাথে গ্রুপ সংখ্যা নির্ণয়ে' ও অরবিটালের ইলেকট্রনের সাথে 10 যোগ করতে হয়।
বোরন মৌলটি 13 গ্রুপে অবস্থিত ।
বোরনের p অরবিটালে । টি ইলেকট্রন বিদ্যমান ।
আয়রনের পারমাণবিক সংখ্যা 26 ।
আয়রনের ইলেকট্রনসমূহ 4 টি শক্তিস্তরে বিন্যস্ত।
আয়রন ৮ নম্বর গ্রুপের মৌল ।
Is2 2s2 2p4 অক্সিজেন (O) মৌলের ইলেকট্রন বিন্যাস।
Ar(18) মৌলের সবচেয়ে বাইরের শক্তিস্তরের ইলেকট্রন বিন্যাস 3s23p0
K এর 19 তম ইলেকট্রনটি 4s অরবিটালে প্রবেশ করে ।
Sc এর পারমাণবিক সংখ্যা 21 ।
Si' এর নিউক্লিয়াসে প্রোটন সংখ্যা 14 ।
Ti(22) এর ইলেকট্রনসমূহ 4 টি শক্তিস্তরে বিন্যস্ত ।
Ar(18) 18 গ্রুপের মৌল।
Zn পরমাণুর শক্তিস্তরে ইলেকট্রন সংখ্যা 30 ।
Cu(29) এর সর্বশেষ ইলেকট্রনটি 4s অরবিটালে প্রবেশ করে ।
Sc এর সর্বশেষ শক্তিস্তরে 3 টি ইলেকট্রন থাকে।
মৌলটির অবস্থান ৩য় স্তরে ।
আয়নের ইলেকট্রন বিন্যাস
পরমাণুর সর্ববহিঃস্থ শক্তিস্তরে পূর্ণ ইলেকট্রন সংখ্যা থেকে 2টি কম থাকলে ঐ মৌলের অবস্থান 16 নং গ্রুপে ।
27X মৌলটি গ্রুপ ৪ গ্রুপের , যেখানে X একটি প্রতীকী মৌল।
A মৌলটি পর্যায় সারণির ৪র্থ পর্যায়ের মৌল।
Zn(30) এর 3d উপস্তরে 10 টি ইলেকট্রন রয়েছে।
Ni(28) এর d উপস্তরে ৮ টি ইলেকট্রন রয়েছে ।
Cu(29) ।। নং গ্রুপের মৌল ।
Mn(25) 7 নং গ্রুপের মৌল ।
A মৌলটি 14 গ্রুপের।
পর্যায় সারণির মূল ভিত্তি ইলেকট্রন বিন্যাস।
Hc গ্রুপ-2 গ্রুপের মৌল ।
পর্যায় সারণিতে মৌলের অবস্থান নির্ণয় করা হয় ইলেকট্রন বিন্যাস এর মাধ্যমে ।
যে মৌলের বাইরের শক্তিস্তরে ইলেকট্রন সংখ্যাটি সেটি ধনাত্মক বা ক্যাটায়ন আয়ন সৃষ্টি করে ।
বাইরের শক্তিস্তরে। টি ইলেকট্রন থাকলে যৌগ গঠনে মৌলটি ইলেকট্রন দান করে ।
Na কর্তৃক সৃষ্ট আয়ন Na+
CI কর্তৃক সৃষ্ট আয়ন CI -
বাইরের শক্তিস্তরে 7 টি ইলেকট্রন থাকলে মৌলটি । টি ইলেকট্রন গ্রহণ করবে।
ইলেকট্রন বিন্যাস বিশিষ্ট মৌলটি কয়টি ইলেকট্রন দান বা গ্রহণ করতে পারে-- একটিও না
ইলেকট্রন বিন্যাস বিশিষ্ট মৌলটি ।টি গ্রহণ করতে পারে।
ইলেকট্রন বিন্যাস বিশিষ্ট মৌলটি ক্যাটায়ন গঠন করতে পারে।
2 টি মৌলের বাইরের প্রধান শক্তিস্তরের ইলেকট্রন বিন্যাস একই হল এদের অবস্থান একই গ্রুপে হয়।
একই গ্রুপে Mg এর পরবর্তী মৌল Ca ।
একই গ্রুপে পটাসিয়ামের পূর্ববর্তী মৌল সোডিয়াম (Na)।
একই গ্রুপে ব্রোমিনের পূর্ববর্তী মৌল ক্লোরিন (CI)।
পর্যায় সারণির গ্রুপ 2 এর ১ম মৌল বেরিলিয়াম (Bc ) ।
গ্রুপ 17 এর মৌলসমূহ যৌগ গঠনকালে ঋণাত্মকআয়ন গঠনের প্রবাতা দেখায় ।
(I- এর ইলেকট্রন বিন্যাস ।
গ্রুপ । এর সর্বশেষ শক্তিস্তরের ইলেকট্রন বিন্যাস nsI
গ্রুপ 2 এর সর্বশেষ শক্তিস্তরের ইলেকট্রন বিন্যাস ns2 ।
গ্রুপ 17 এর সর্বশেষ শক্তিস্তরের ইলেকট্রন বিন্যাস ns2 np5
ইলেকট্রন বিন্যাস মৌলটির গ্রুপ সংখ্যা 12 ।
গ্রুপ ।। এর সর্বশেষ শক্তিস্তরের ইলেকট্রন বিন্যাস
ক্লোরিন সর্বশেষ শক্তিস্তরে । টি ইলেকট্রন গ্রহণ করতে পারে ।
অধাতু হওয়া সত্ত্বেও পর্যায় সারণিতে ক্ষার ধাতুর সাথে অবস্থান হাইড্রোজেন মৌলটির ।
পর্যায় সারণিতে তীব্র তড়িৎ ধনাত্মক ক্ষার ধাতুর অবস্থান গ্রুপ-। এ গ্রুপে।
Na, K, Rb মৌলগুলো তীব্র তড়িৎ ধনাত্মক ক্ষার ধাতু।
হাইড্রোজেনের বেশিরভাগ ধর্ম ক্ষার ধাতুসমূহ মৌলসমূহের সাথে সামঞ্জস্যপূর্ণ।
হাইড্রোজেনের অবস্থান গ্রুপ-। এ ।
ধাতব বৈশিষ্ট্যের ভিত্তিতে হাইড্রোজেন মূলত একটি অধাতু ।
ক্ষারধাতুসমূহ ব্যতীত হাইড্রোজেনের ধর্ম আর হ্যালোজেন মৌলসমূহের সাথে সামঞ্জস্যপূর্ণ ।
F. Cl. Br. I মৌলগুলোকে হ্যালোজেন বলা হয়।
হাইড্রোজেন তার বহিঃস্তরে I টি ইলেকট্রন গ্রহণ করতে পারে।
গ্রুপ-২ এর মৌলসমূহের চার্জ তীব্র তড়িৎ ধনাত্মক।
হিলিয়াম মূলত নিষ্ক্রিয় গ্যাস ।
হিলিয়ামকে ধর্মের ভিত্তিতে গ্রুপ-১৪ গ্রুপে স্থান দেয়া হয়েছে ।
ইলেকট্রন বিন্যাস অনুযায়ী মৃৎক্ষার ধাতু মৌলসমূহের সাথে হিলিয়ামের অবস্থান হওয়ার কথা ।
ল্যাম্বানাইড ও অ্যাকটিনাইড সারির মৌলগুলোর অবস্থান গ্রুপ ৩ এ
ল্যান্থানাইড ও অ্যাকটিনাইড সারির মৌলসমূহকে পর্যায় সারণির নিচে রাখার কারণ পর্যায় সারণির সুন্দরভাবে উপস্থাপন।
ল্যান্থানাইড সারিতে 15 টি মৌল রয়েছে।
ল্যান্থানাইড সারির সর্বশেষ মৌল লুটেসিয়াম (Lu)।
অ্যাকটিনিয়ামের নিউক্লিয়াসে প্রোটন সংখ্যা 89 ।
অ্যাকটিনাইড সারির সর্বশেষ মৌল লরেনসিয়াম (L) ।
মৌলের ধাতব ধর্ম, পরমাণুর আকার, আয়নিকরণ শক্তি তড়িৎ ঋণাত্মকতা ইত্যাদিকে পর্যায়বৃত্ত ধর্ম বলে।
এক বা একাধিক ইলেকট্রন ত্যাগ করে ক্যাটায়নে পরিণত হলে তাকে ধাতু বলে ।
ধাতুর ইলেকট্রন ত্যাগের ধর্মকে ধাতব ধর্ম বলে।
একই পর্যায়ে বাম থেকে ডানে গেলে ধাতব ধর্মের হ্রাস পায়।
অধাতুসমূহের বিদ্যুৎ পরিবাহী ধর্ম অপরিবাহী।
ধাতুসমূহের বিদ্যুৎ পরিবাহিতার ধর্ম পরিবাহী।
এক বা একাধিক ইলেকট্রন গ্রহণ করে অ্যানায়নে পরিণত হলে তাকে অধাতু বলে।
যেকোনো পর্যায়ের বাম থেকে ডানে গেলে অধাতব ধর্মের বৃদ্ধি পায় ।
ক্ষেত্র বিশেষে ইলেকট্রন দান ও গ্রহণ উভয়ই করতে পারলে তাকে অর্ধধাতু বা অপধাতু বলে।
ধাতব বৈশিষ্ট্যের ভিত্তিতে সিলিকন অপধাতু।
পর্যায় সারণির মাঝের মৌলগুলো সাধারণত অর্ধধাতু ।
পর্যায় সারণির ডান দিকের মৌলগুলো সাধারণত অধাতু ।
একটি পর্যায়ের যতই বাম থেকে ডানে যাওয়া যায় পারমাণবিক ব্যাসার্ধের কমতে থাকে।
একটি গ্রুপের উপর থেকে নিচের দিকে গেলে পরমাণবিক ব্যাসার্ধের বৃদ্ধি পায় ।
পরমাণুর নিউক্লিয়াসের অধিক প্রোটন এবং শক্তিস্তরের অধিক ইলেকট্রন সংখ্যার মধ্যে আকর্ষণ বেশি হলে পরমাণুর আকার ছোট হয় ।
পরমাণুর নিউক্লিয়াসের বাইরের দিকে শক্তিস্তর সংখ্যা বৃদ্ধি পেলে পরমাণুর আকার বৃদ্ধি পায়।
সোডিয়ামের তুলনায় রুবিডিয়ামের আকার বড়।
Na. Mg. Si. Al এর মধ্যে Si আয়নিকরণ শক্তির মান বেশি ।
Mg. Na. Al. Si এর মধ্যে Na পারমাণবিক ব্যাসার্ধের মান বেশি।
F. Cl, Br, I, At এর মধ্যে F আয়নিকরণ শক্তির মান সরচেয়ে বেশি ।
গ্রুপ-। এর মৌলগুলোর মধ্যে Li আয়নিকরণ শক্তির মান রেশি।
পারমাণবিক ব্যাসার্ধ কমলে ইলেকট্রন আসক্তির মানের বৃদ্ধি পায় ।
Be. Ca. Sn, Ba এর মধ্যে Be ইলেকট্রন আসক্তির মান সবচেয়ে বেশি ।
Sr, Ba. Mg, Ra এর মধ্যে Ra ইলেকট্রন আসক্তি সবচেয়ে কম।
ও নং পর্যায়ের মৌলগুলোর মধ্যে সোডিয়াম (Na) ইলেকট্রন আসক্তির মান সবচেয়ে কম।
Cs. Rb. K, Na এর মধ্যে Cs সক্রিয়তা সবচেয়ে বেশি ।
পরমাণবিক ব্যাসার্ধ বাড়লে তড়িৎ ঋণাত্মকতার হ্রাস পায় ।
মৌলসমূহের ভৌত ও রাসায়নিক ধর্ম ভিত্তিতে বিশেষ নাম দেওয়া হয় ।
গ্রুপ-। এর হাইড্রোজেন মৌলটি ক্ষারধাতু নয় ।
ক্ষারধাতুসমূহ পানিতে দ্রবীভূত হয়ে হাইড্রোজেন গ্যাস তৈরি করে ।
পর্যায় সারণির গ্রুপ-2 এর মৌলসমূহকে মৃৎক্ষার ধাতু বলা হয়।
Na. K. Mg. Ag মৌলগুলোর মধ্যে Mg (ম্যাগনেসিয়াম) মাটিতে বিভিন্ন যৌগ হিসেবে পাওয়া যায়।
গ্রুপ-।। গ্রুপের মৌলগুলোকে মুদ্রা ধাতু বলা হয় ।
গ্রুপ-।। এর রন্টজেনিয়াম (Rg) মৌলটির মুদ্রা তৈরিতে ব্যবহার নেই ।
Cu, Ag, Au তিনটি মৌলকে মুদ্রা ধাতু বলা হয়।
গ্রুপ-17 এর মৌলগুলোকে হ্যালোজেন বলা হয়।
হ্যালোজেন মৌলকে X দ্বারা প্রকাশ করা হয় ।
হ্যালোজেন মানে লবণ উৎপাদনকারী ।
হ্যালোজেনের মূল উৎস সামুদ্রিক লবণ।
লবণ গঠনে হ্যালোজেনের সাথে ধাতু যুক্ত হয়।
গ্রুপ-18 গ্রুপের মৌলসমূহকে নিষ্ক্রিয় গ্যাস বলা হয় ।
পর্যায় সারণির গ্রুপ-18 এর মৌলগুলো সাধারণ তাপমাত্রায় গ্যাসীয় অবস্থায় থাকে ।
নিষ্ক্রিয় মৌলগুলো ইলেকট্রন বিনিময় বা শেয়ার করার কারণ অষ্টক পূর্ণতা।
অবস্থান্তর মৌলগুলো রঙিন যৌগ গঠন করে ।
নিকেল রাসায়নিক বিক্রিয়া জৈব বিক্রিয়ার প্রভাবক হিসেবে কাজ করে ।
রসায়ন পাঠ সহজীকরণের প্রধান ভূমিকা পালন করে পর্যায় সারণি।
পর্যায় সারণির 18 টি গ্রুপের ধর্ম জানা থাকলে 118 টি মৌলের ধর্ম সম্পর্কে জানা যায় ।
আবিষ্কৃত ।।৪টি মৌলের 4টি ভৌত ও 4টি রাসায়নিক ধর্ম দিয়ে মোট 944টি বৈশিষ্ট্য লক্ষ্য করা যায় ।
বিভিন্ন মৌল দ্বারা গঠিত যৌগের ধর্ম সম্পর্কে ধারণা লাভের জন্য পর্যায় সারণি জানতে হবে ।
পর্যায় সারণির 55 টি অনাবিষ্কৃত মৌল সম্পর্কে ভবিষ্যদ্বাণী করেছিলেন বিজ্ঞানী মেন্ডেলিফ ।
নতুন পদার্থ আবিষ্কার করতে চাইলে পর্যায় সারণি বিষয়ে ধারণা থাকতে হবে।
হাইড্রোজেন হ্যালাইডকে পানিতে দ্রবীভূত করলে হাইড্রোহ্যালাইড এসিড উৎপন্ন হয়।
হাইড্রোহ্যালাইড এসিড কার্বনেট লবণের সাথে বিক্রিয়ায় কার্বন ডাইঅক্সাইড গ্যাস তৈরি করে।
ক্যালসিয়াম কার্বনেটের মধ্যে হাইড্রোহ্যালাইড এসিড যোগ করলে CO2গ্যাস পাওয়া যায় ।
ম্যাগনেসিয়াম কার্বনেট লঘু হাইড্রোক্লোরিক এসিডের সাথে বিক্রিয়া Mg Cl2 লবণ উৎপন্ন করে ।
ম্যাগনেসিয়াম কার্বনেট লঘু হাইড্রোক্লোরিক এসিডের সাথে বিক্রিয়া উৎপন্ন তরল পদার্থ পানি (H২O) ।
1789 সালে বিজ্ঞানী ল্যাভয়সিয়ে O, N, H, P, Hg, Zn এবং S ইত্যাদি মৌলিক পদার্থসমূহকে ধাতু ও অধাতু এ দুইভাগে ভাগ করেন। এই সময় থেকেই মৌলগুলোকে বিভিন্ন ভাগে ভাগ করার চিন্তা ভাবনা শুরু হয় যেন, একই ধরনের মৌলিক পদার্থগুলো একটি নির্দিষ্ট ভাগে থাকে।
তিনটি মৌলকে তাদের পারমাণবিক ভর অনুসারে সাজালে দ্বিতীয় মৌলের পারমাণবিক ভর প্রথম ও তৃতীয় মৌলের পারমাণবিক ভরের যোগফলের অর্ধেক বা গড় হয়" - এটিই ডোবেরাইনার ত্রয়ী সূত্র। উদাহরণ, লিথিয়াম (7) ও পটাসিয়াম (39) এর পারমাণবিক ভরের গড় সোডিয়াম (23) এর পারমাণবিক ভরের প্রায় সমান।
নিউল্যান্ডের অষ্টক সূত্রটি হলো- "মৌলগুলোকে যদি ক্রমবর্ধমান পারমাণবিক ভর হিসেবে সাজানো হয় তাহলে প্রত্যেক অষ্টম মৌলে ভৌত ও রাসায়নিক ধর্মের সাথে মিলে যায়।" যেমন, Li কে ১ম মৌল ধরে পরে'র X অষ্টম মৌল হয় Na। প্রকৃতপক্ষে দেখা যায় Li, Na এবং K মৌলসমূহের মধ্যে ভৌত ও রাসায়নিক ধর্মের অনেক মিল রয়েছে।
বিজ্ঞানী মেন্ডেলিফ 1'869 সালে সকল মৌলের ধর্ম পর্যালোচনা করে একটি পর্যায়সূত্র প্রদান করেন, যা মেন্ডেলিফের পর্যায়সূত্র নামে পরিচিত। সূত্রটি হলো- "মৌলসমূহের ভৌত ও রাসায়নিক ধর্মাবলি তাদের পারমাণবিক ভর বৃদ্ধির সাথে পর্যায়ক্রমে আবর্তিত হয়। এ সূত্র মতে, 63টি মৌলকে 12 টি আনুভূমিক সারি আর ৪টি খাড়া কলাম, এর একটি ছকে পারমাণবিক ভর অনুসারে সাজানো হয়েছে। এ ছকটি হলো পর্যায় সারণি।
মেন্ডেলিফের পর্যায় সূত্র অনুযায়ী, কম পারমাণবিক ভরবিশিষ্ট পরমাণু পর্যায়সারণির আগে বসবে এবং বেশি পারমাণবিক ভরবিশিষ্ট পরমাণু সারণির পরে বসবে। কিন্তু এর ব্যতিক্রম ঘটছে Ar ও K এর ক্ষেত্রে। যেমন Ar এর পারমাণরিব ভর 40 ও K এর পারমাণবিক ভর 39। অর্থাৎ Ar এর পারমাণবিক ভর তুলনামূলক বেশি হওয়া সত্ত্বেও K এর পূর্বে Ar কে বসানো হয়েছে- এটাই মেন্ডিলিফের পর্যায় সারণির অন্যতম একটি ত্রুটি।
বিজ্ঞানী মোসলে মেন্ডেলিফের পর্যায় সারণির ত্রুটি সংশোধন করেন। মোসলে পারমাণবিক ভরের পরিবর্তে পারমাণবিক সংখ্যা অনুযায়ী মৌলগুলোকে সংঞ্জান যার ফলে মেন্ডেলিফের পর্যায় সামাণর ত্রুটি দূর হয়। যেমন- আর্পনের (Ar) পারমাণবিক সংখ্যা ১৪ এবং পটাশিয়াম (K) এর পা রমাণবিক সংখ্যা 19। কাজেই কম পারমাণবিক সংখ্যাবিশিষ্ট মৌল 18/T, 10K এর আগে. বসবে।
JUPAC হচ্ছে আন্তর্জাতিক রসায়ন ও ফলিত রসায়ন। সংস্থা (International Union of Pure & Applied Chemistry)। IUPAC সংস্থাটি আন্তর্জাত্যি কভাবে রসায়ন ও ফলিত রসায়নের বিভিন্ন নিয়মকানুন, ক্রমবর্ধমান পরিবর্তনের কোনটি গ্রহণ করা 'যায় এবং কোনটি বর্জন করা উচিত- এ বিষয়গুলো দেখাশোনা এবং নিয়ন্ত্রণ করে।
আধুনিক পর্যায় সারণির দুইটি বৈশিষ্ট্য নিম্নরূপ-
১. পর্যায় সারণিতে 7টি পর্যায় (period) বা আনুভূসিক সারি এবং 1৪টি গ্রুপ বা খাড়া স্তম্ভ রয়েছে।
২. প্রতিটি পর্যায় বামদিকে গ্রুপ 1 থেকে শুরু করে ডানদিকে গ্রুপ 18 পর্যন্ত বিস্তৃত।
যে সকল মৌলের পারমাণবিক সংখ্যা 57 থেকে 71 পর্যন্ত এ রকম 15টি মৌলকে ল্যাম্বানাইড সারির মৌল বলা হয়। উদাহর' ণস্বরূপ, 57La, 58Ce. 60Nd, 70Yb, 71Lu 'ইত্যাদি মৌলগুলো ল্যাম্প নাইড সারির মৌল। এসব মৌলসমূহের ধর্ম খুব কাছাকাছি। এদো একে মূল পর্যায় সারণির নিচে আলাদাভাবে, ল্যান্থানাইড সারির মৌল হিসেবে দেখানো হয়েছে।
যে সকল মৌলের পারমাণবিক সংখ্যা ৪:9 থেকে 103 পর্যন্ত এ র/কম 15টি মৌলকে অ্যাকটিনাইড সারির মৌল বলা হয়। উদাহরণস্বরূপ, 89AC, 99Th, 92U, 93Np, 94Pu, 102 No, 103Lr ইত্যাদি মৌলগুলো অ্যাকটিনাইড সারির মৌল। এসব। মৌলসমূহের ধর্মসমূহ খুব কাছাকাছি। এদেরকে মূল পর্যায় সারণির নিচে আলাদাভাবে 'অ্যাকটিনাইড সারির মৌল হিসেবে দেখানো হয়েছে।
মৌলসমূহের ধর্মের ভিত্তিতে পর্যায় সারণির দুইটি বৈশিষ্ট্য নিম্নরূপ-
১. একই পর্যায়ের বাম থেকে ডানের 'দিকে গেলে মৌলসমূহের ধর্ম ক্রমান্বয়ে পরিবর্তিত হয়।
২. একই গ্রুপের মৌলগুলোর ভৌত ও রাসায়নিক ধর্ম প্রায় একই রকমের হয়।
পর্যায় সারণির 7টি পর্যায়ের। মৌল সংখ্যা নিচে দেওয়া হলো-
➡️প্রথম পর্যায়ে মাত্র 2টি মৌল 'অবস্থিত।
➡️দ্বিতীয় ও তৃতীয় পর্যায়ে ৪টি করে মৌল অবস্থিত।
➡️৪র্থ পর্যায় ও ৫ম পর্যায়ে 1টি করে মৌল অবস্থিত।
➡️৬ষ্ঠ পর্যায়ে 32টি মৌল আছে।
➡️৭ম পর্যায়ে রাকী 32টি মৌল অবস্থিত।
বোরন (B) এর ইলেকট্রন বিন্যাস-1B(5) = 1s22s22p1 | সর্বশেষ ইলেকট্রন অরবিটালে যায় বলে-গ্রুপ সংখ্যা = 10+ যোজ্যতা স্তরের মোট e- সংখ্যা= 10+3=13 আবার, ইলেকট্রন বিন্যাস দুইটি স্তরে বিনাস্ত হওয়ায় এটি ২য় পর্যায়ের মৌল। সুতরাং, B মৌলটি ২য় পর্যায়ের গ্রুপ-13 তে অবস্থিত।
ফসফরাস (P) এর ইলেকট্রন বিন্যাস-P(15) = 1s2 2s2 2p6 3s2 3p3 জানা আছে, ফসফরাস (15) এর ইলেকট্রন বিন্যাসে (2. 8. 5) এর শেল সংখ্যা ১টি এবং সর্ববহঃস্থ স্তরে (s ও p orbital) ইলেকট্রন সংখ্যা 5টি। তাহলে P এর গ্রুপ সংখ্যা = 10+5=15। অর্থাৎ, ফসফরাস ৩য় পর্যায়ের 15 নং গ্রুপে অবস্থিত।
ফসফরাস (P) এর ইলেকট্রন বিন্যাস-P(15) = 1s2 2s2 2p6 3s2 3p3 জানা আছে, ফসফরাস (15) এর ইলেকট্রন বিন্যাসে (2. 8. 5) এর শেল সংখ্যা ১টি এবং সর্ববহঃস্থ স্তরে (s ও p orbital) ইলেকট্রন সংখ্যা 5টি। তাহলে P এর গ্রুপ সংখ্যা = 10+5=15। অর্থাৎ, ফসফরাস ৩য় পর্যায়ের 15 নং গ্রুপে অবস্থিত।
Y(20) = 1s2 2s2 2p6 3s2 3p6 4s2
ইলেকট্রন বিন্যাস অনুযায়ী, ইলেকট্রনগুলো চারটি শক্তিস্তরে বিন্যস্ত। কাজেই মৌলটির অবস্থান হবে চতুর্থ পর্যায়ে। আবার, সর্ববহিঃস্থ শক্তিস্তরে s orbital-এ ইলেকট্রন সংখ্যা 2। অতএব, Y মৌলটির গ্রুপ সংখ্যা হবে 2।
প্রদত্ত Z মৌলটি ড্যানাডিয়াম (V)। কারণ ভ্যানাডিয়ামের (V) পারমাণবিক সংখ্যা 23।
V(23) 1s2 2s2 2p6 3s2 3p6 4s2
পর্যায় নির্ণয়: ইলেকট্রন বিন্যাসে সর্বশেষ শক্তিস্তর 4। এ কারণে এটি 4নং পর্যায়ে অবস্থিত।
গ্রুপ নির্ণয়: V এর সর্বশেষ ইলেকট্রন এ অরবিটালে প্রবেশ করে। তাই, এটির গ্রুপ = d অরবিটালের e- সংখ্যা + s অরবিটালের e - সংখ্যা = 3 + 2 = 5
সুতরাং বলা যায় যে, Z মৌল তথা ভ্যানাডিয়াম (V) পর্যায় সারণিতে ৪র্থ পর্যায়ের ১ নং গ্রুপে অবস্থিত।
ক্লোরিনের ইলেকট্রন বিন্যাস্ নিম্নরূপ-Cl(17)-1s2 2s22p6 3s2 3p5 ইলেকট্রন বিন্যাস অনুযায়ী, ইলেকট্রনগুলো তিনটি শক্তিস্তরে বিন্যস্ত। কাজেই, ক্লোরিনের অবস্থান হবে তৃতীয় পর্যায়ে। আবার, সর্ববহিঃস্থ শক্তিস্তরে ইলেকট্রন সংখ্যা 7 । অতএব ক্লোরিনের গ্রুপ সংখ্যা হবে 7 + 10 = 17 ।
আর্গন (Ar) এর ইলেকট্রন বিন্যাস-Ar(18) 1s2 2s2 2p6 3s2 3p6 = পর্যায় নির্ণয়: Ar এর ইলেকট্রনসমূহ মোট তিন স্তরে বিন্যস্ত হওয়ায় Ar ৩য় পর্যায়ের মৌল।
গ্রুপ নির্ণয়: যোজ্যতা স্তরে ও অরবিটাল থাকায় এর গ্রুপ সংখ্যা 10+6+2 = 18 সুতরাং, Ar মৌলটি ৩য় পর্যায়ে 18 নং গ্রুপে অবস্থিত।
Ti(22) = 1s2 2s2 2p6 3s2 3p6 3d2 4s2
পর্যায় নির্ণয়: e- বিন্যাস 4টি স্তরে বিন্যস্ত। তাই এটি ৪র্থ পর্যায়ে অবস্থিত ।
গ্রুপ নির্ণয়: (n-1)d ns এর মোট e- = (2 + 2) = 4 অর্থাৎ গ্রুপ-4 এর মৌল।
As(33) এর ইলেকট্রন বিন্যাস:
As(33) = 1s2 2s2 2p6 3s2 3p6 3d10 4s24p3
পর্যায় নির্ণয়: As এর ইলেকট্রন বিন্যাসে সবচেয়ে বাইরের শক্তিস্তর 4। এ কারণে এটি 4নং পর্যায়ের মৌল।
গ্রুপ নির্ণয়: As এর যোজ্যতান্তরে s ও p অরবিটাল রয়েছে।
∴ গ্রুপ = যোজ্যতা স্তরের মোট ইলেকট্রন সংখ্যা + 10 (2+3)+10=15
Rb(37) এর ইলেকট্রন বিন্যাস:
Rh(37) = 1s2 2s2 2p6 3s2 3p6 3d10 4s24p65s
পর্যায় নির্ণয়: Ri এর ইলেকট্রন বিন্যাসে সবচেয়ে বাইরের শক্তিস্তর 5। তাই এটি ৫ম পর্যায়ের মৌল।
গ্রুপ নির্ণয়: যেহেতু Rb এর সর্বশেষ শন্তিস্তর 5s অরবিটালে 1টি e- আছে। তাই এটি গ্রুপ-1 এর মৌল।
যেসব মৌলের শেষ ইলেকট্রনটি p উপশক্তিস্তরে যায় সেগুলোকে 'ব্লক মৌল বলা হয়। এসব মৌলের শেষ কক্ষপথের s ও p অরবিটালের মোট ইলেকট্রন সংখ্যার সাথে 10 যোগ করে গ্রুপ নির্ণয় করা হয়। যেমন- 14Si 1s2 2s2 2p6 3s2 3p2
এক্ষেত্রে s ও p অরবিটালের মোট সংখ্যা (2+2) = 4। অর্থাৎ, Si মৌলটির গ্রুপ সংখ্যা = 10 + 4 = 14।
Cu(29) এর ইলেকট্রন বিন্যাস:
Cu(29) = 1s2 2s2 2p6 3s2 3p2
পর্যায় নির্ণয়: Cu এর ইলেকট্রনসমূহ মোট চারটি স্তরে বিন্যস্ত হওয়ায় এটি ৪র্থ পর্যায়ের মৌল।
গ্রুপ নির্ণয়: Cu এর গ্রুপ (s+d) অরবিটালের মোট e- সংখ্যা = (1+10) = 11 নং গ্রুপ।
অর্থাৎ পর্যায় সারণিতে Cu এর অবস্থান হলো ৪র্থ পর্যায়ের গ্রুপ-11 তে।
ক্রোমিয়াম (Cr) এর ইলেকট্রন বিন্যাস-
Cr(24) = 1s2 2s2 2p6 3s2 3p6 3d54s1
পর্যায় নির্ণয়: Cr এর ইলেকট্রনসমূহ মোট চারটি স্তরে বিন্যস্ত হওয়ায়
Cr(24) ৪র্থ পর্যায়ের মৌল।
গ্রুপ নির্ণয়:
Cr(24) মৌলটি ১ ব্লকভুক্ত হওয়ায় এর গ্রুপ ১ অরবিটালে মোট ইলেকট্রন সংখ্যা যোজ্যতা স্তরের মোট ইলেকট্রন সংখ্যা = 5+1=6 সুতরাং বলা যায়, Cr মৌলটি পর্যায় সারণির ৪র্থ পর্যায়ের নেং গ্রুপে অবস্থিত।
Zn(30) এর ইলেকট্রন বিন্যাস-
Zn(30)=
পর্যায় নির্ণয়: e- বিন্যাস 4টি স্তরে বিন্যস্ত। তাই এটি ৪র্থ পর্যায়ের মৌল।
গ্রুপ নির্ণয়: (n-1)d ns এর মোট e (10+2) = 12 অর্থাৎ গ্রুপ-12 এর মৌল।
প্রতিটি মৌলের পারমাণবিক সংখ্যা নির্দিষ্ট বলে প্রতিটি মৌলের ইলেকট্রন বিন্যাসও নির্দিষ্ট এবং একটির ইলেকট্রন বিন্যাস অন্যটি থেকে ভিন্ন। আবার প্রতিটি পারমাণবিক সংখ্যার জন্য পর্যায় সারণিতে একটি নির্দিষ্ট অবস্থান হয়েছে। তাই পর্যায় সারণিতে একটি মৌল একটিমাত্র খান দখল করে।
পর্যায় সারণিতে মৌলের অবস্থান নির্ণয় ও মৌলসমূহের অনেক ধর্ম ইলেকট্রন বিন্যাসের মাধ্যমে ব্যাখ্যা করা যায়। যেমন,
মৌলটির ইলেকট্রন বিন্যাস ওটি স্তরে বিন্যস্ত, তাই এর পর্যায় 3 এবং যোজ্যতান্তরে s orbital-এ ২টি e- আছে। এজন্য এর গ্রুপ সংখ্যা 2। আবার বহিঃস্থ স্তরের e- 2টি দান করে ক্যাটায়নে পরিণত হতে পারে। তাই এটি ধাতু। সুতরাং বলা যায়, ইলেকট্রন বিন্যাসই পর্যায় সারণির মূল ভিত্তি।
হলো ম্যাগনেসিয়ামের দ্বিধনাত্মক আয়ন।
Mg এর ইলেকট্রন বিন্যাস নিম্নরূপ:
মৌলটির শেষ শক্তিস্তরে 2টি ইলেকট্রন থাকায় এটি সহজেই উক্ত ইলেকট্রন দুটি ত্যাগ করে নিষ্ক্রিয় গ্যাস Ne এর ইলেকট্রন বিন্যাস অর্জন করে এবং তড়িৎ ধনাত্মক আয়ন গঠন করে। যেমন-
হাইড্রোজেন (H) কে গ্রুপ-1 এ স্থান দেওয়া হয়। কারণ গ্রুপ-। এর মৌলগুলোর যোজ্যতা স্তরে 1টি মাত্র ইলেকট্রন থাকে। গ্রুপ-। এর মৌলগুলোর যোজনী-1, H এর যোজনীও ।। গ্রুপ-1 এর মৌলগুলো হ্যালোজেনের সাথে ধাতব হ্যালাইড (MX) গঠন করে; Hও হ্যালোজেনের সাথে HX যৌগ গঠন করতে পারে। অর্থাৎ গ্রুপ-। এর মিল থাকায় H কে গ্রুপ-। এ স্থান দেওয়া হয়েছে।
হিলিয়াম. (He) এর ইলেকট্রন বিন্যাস 1s2; সর্বশেষ কক্ষপথে 2টি ইলেকট্রন থাকায় He এর অবস্থান 2 নং গ্রুপে মৃৎক্ষার ধাতুদের সাথে হওয়া উচিত। কিন্তু He এর সর্বশেষ কক্ষপথ ইলেকট্রন দ্বারা পূর্ণ থাকায় এটি গ্রুপ-২নং এর মৌলসমূহের মত সক্রিয়তা, ধাতব বৈশিষ্ট্য প্রদর্শন করে না। সর্বোপরি, মৃৎক্ষার ধাতুদের সাথে ইলেকট্রন বিন্যাস ব্যতীত বৈশিষ্ট্যগত কোনো মিল না থাকায় একে গ্রুপ-২নং এ না রেখে 18 নং গ্রুপে রাখা হয়েছে।
He এর ইলেকট্রন বিন্যাস He (2) = 1s2এ সর্বশেষ কক্ষপথ ইলেকট্রন দ্বারা পূর্ণ থাকে। এজন্য এটি অপর কোনো মৌলের সাথে ইলেকট্রন গ্রহণ, বর্জন বা শেয়ার করে না। অর্থাৎ নিষ্ক্রিয় অবস্থায় থাকে। আবার ১৪ নং গ্রুপ হচ্ছে নিষ্ক্রিয় মৌলুসমূহের গ্রুপ। তাই He কে নিষ্ক্রিয় গ্যাসের সাথে গ্রুপ-18 তে রাখা হয়।
পর্যায় সারণিতে ল্যান্থানাইড সারির মৌলগুলো ৬ষ্ঠ পর্যায়ের 3 নং গ্রুপে অবস্থিত এবং অ্যাকটিনাইড সারির মৌলগুলো ৭ম পর্যায়ের 3 নং গ্রুপে অবস্থিত। এই অবস্থানগুলোতে ল্যান্থানাইড ও অ্যাকটিনাইড সারির মৌলগুলো বসালে পর্যায় সারণির সৌন্দর্য নষ্ট হয়। তাই পর্যায়সারণিকে সুন্দরভাবে উপস্থাপন করার জন্য প্রদত্ত মৌলগুলোকে পর্যায়সারণির নিচে আলাদাভাবে রাখা হয়েছে।
মৌলসমূহের ভৌত, রাসায়নিক ধর্মাবলি তাদের ইলেকট্রন বিন্যাসের উপর বিশেষভাবে নির্ভরশীল। যেহেতু মৌলসমূহের ইলেকট্রন বিন্যাস পর্যায়ক্রমে পরিবর্তিত হয়, সেহেতু মৌলসমূহের কিছু ধর্ম পর্যায়ক্রমে আবর্তিত হয়। এসব ধর্মকে পর্যায়বৃত্ত ধর্ম বলা হয়। যেমন-ইলেকট্রন আসক্তি, আয়নিকরণ বিভব, তড়িৎ ঋণাত্মকতা, পারমাণবিক ব্যাসার্ধ ইত্যাদি মৌলের পর্যায়বৃত্ত ধর্ম।
যে সকল মৌল এক বা একাধিক ইলেকট্রন ত্যাগ করে ধনাত্মক আয়নে পরিণত হয় তাদেরকে বলে ধাতু। ধাতুর কয়েকটি বৈশিষ্ট্য হলো-
১. এসব ধাতব মৌল চকচকে
২. আঘাতে ধাতব শব্দ করে
৩. তাপ ও বিদ্যুৎ সুপরিবাহী।
ধাতুর ইলেকট্রন ত্যাগের মাধ্যমে ধনাত্মক আয়নে পরিণত হওয়ার ধর্মকে বলে ধাতব ধর্ম। যে মৌলের পরমাণু যত সহজে ইলেকট্রন ত্যাগ করতে পারবে, সেই মৌলের ধাতব ধর্ম তত বেশি। যেমন K ধাতুর ১টি e- ত্যাগ করে K+-এ পরিণত হওয়ার ধর্মকে K এর ধাতব ধর্ম বলে।
লিথিয়াম (Li) একটি ধাতু। কারণ- এর ইলেকট্রন বিন্যাস হতে পাই,
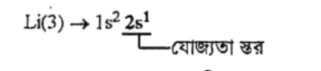
Li এর যোজ্যতা স্তরের 1টি e- ত্যাগ করে Li+-এ পরিণত হয়।
Li→ Li++e-
যে সকল মৌল এক বা একাধিক ইলেকট্রন গ্রহণ করে ঋণাত্মক আয়নে পরিণত হয়, তাদেরকে বলা হয় অধাতু। অধাতুর কয়েকটি বৈশিষ্ট্য হলো-
১. এসব মৌল চকচকে নয়
২. আঘাত করলে ধাতব শব্দ হয় না
৩. তাপ ও বিদ্যুৎ পরিবাহী নয়।
জানা আছে, যে সকল মৌল এক বা একাধিক ইলেকট্রন গ্রহণ করে ঋণাত্মক আয়নে পরিণত হয়, তাদেরকে বলে অধাতু। ক্লোরিন (CI) মৌলটি অধাতু। কারণ CI একটি ইলেকট্রন গ্রহণ করে CI- এ পরিণত হয়। অর্থাৎ, Cl + e- → Cl-
জানা আছে, যে সকল মৌল কোনো কোনো সময় ইলেকট্রন ত্যাগ করে এবং কোনো কোনো সময় ইলেকট্রন গ্রহণ করে তাদেরকে বলে অপধাতু। Si মৌলটি কোনো সময় ইলেকট্রন ত্যাগ করে তথা ধাতুর মতো আচরণ করে আবার কোনো সময় ইলেকট্রন গ্রহণ করে তথা অধাতুর মতো আচরণ করে। তাই বলা যায় সিলিকন (Si) একটি অপধাতু বা অর্ধধাতু
একই পর্যায়ে বাম থেকে ডানে গেলে-
১. পরমাণুর আকার হ্রাস পায়।
২. আয়নিকরণ শক্তি বৃদ্ধি পায়।
৩. ইলেকট্রন আসক্তি বৃদ্ধি পায়।
৪. তড়িৎ ঋণাত্মকতা বৃদ্ধি পায়।
৫. ধাতব বৈশিষ্ট্য হ্রাস পায়।
পর্যায় সারণির একই গ্রুপে উপর থেকে নিচের দিকে মৌলের-
১. আয়নিকরণ শক্তির হ্রাস পায়।
২. তড়িৎ ঋণাত্মকতা হ্রাস পায়।
৩. ইলেকট্রন আসক্তি হ্রাস পায়।
৪. অধাতব বৈশিষ্ট্য হ্রাস পায়।
৫. পারমাণবিক আকার বৃদ্ধি পায়।
পরমাণুর ইলেকট্রন বিন্যাসে যখন নতুন একটি শেল বা ইলেকট্রন স্তর যুক্ত হয়। তখন তার আকার বৃদ্ধি পায়। কারণ একই গ্রুপে উপর থেকে নিচে নামলে নতুন একটি করে শক্তিস্তর যুক্ত হয়। ফলে পরমাণুর আকার বৃদ্ধি পায়।
একই পর্যায়ে বাম থেকে ডানে গেলে শক্তিস্তর সংখ্যা একই থাকে, কিন্তু একটি করে ইলেকট্রন বৃদ্ধি পায়। ফলে তারা ধনাত্মক নিউক্লিয়াসকে আরও বেশি আকর্ষণ করে এবং সংকুচিত হয়। তাই পরমাণুর আকার হ্রাস পায়।
CI ও Ar এর মধ্যে Ar এর আকার ছোট। কারণ CI মৌল দুটি ৩য় পর্যায়ের ভিন্ন গ্রুপে অবস্থিত। একই পর্যায়ের বাম থেকে ডানে পারমাণবিক আকার ক্রমান্বয়ে হ্রাস পায়। কারণ বাম থেকে ডানে যোজ্যতা স্তর বৃদ্ধি পায়। ফলে আগত ইলেকট্রনের প্রতি নিউক্লিয়াসের আকর্ষণ বৃদ্ধি পায় এবং পরমাণুর আকার ছোট হয়। Ar(18) পরমাণু CI(17) এর ডানে অবস্থিত হওয়ায় Ar আকার ছোট হয়।
Na এর গঠন বিন্যাস পর্যালোচনা করলে দেখা যায় যে এর বিন্যাস্ 2, 8, 1। এর সর্ববহিঃস্থ কক্ষপথে একটি মাত্র ইলেকট্রন এবং তিনটি কক্ষপথ বিদ্যমান।

আবার যখন Na তার সর্বশেষ শক্তিস্তরের ইলেকট্রন ত্যাগ করে Na+ আয়নে পরিণত হয় তখন তার বিন্যাস দাঁড়ায় 2. ৪। ইলেকট্রন ত্যাগের মাধ্যমে এর শক্তিস্তর দুটিতে পরিণত হয়। ফলে Na+ এর আকার ছোট হয়ে আসে। তাই Na অপেক্ষা Na+এর আকার ছোট।
Mg ও Mg2+ আয়নের ইলেকট্রন বিন্যাস-
দেখা যাচ্ছে, Mg এর ইলেকট্রন বিন্যাস তিনটি স্তরে বিন্যস্ত হলেও
Mg2+ আয়নের ইলেকট্রন বিন্যাস দুটি স্তরে বিন্যস্ত। তাছাড়া Mg2+ আয়নের ক্ষেত্রে অধিক প্রোটন (12) কম ইলেকট্রন (10) কে অধিক শক্তিতে আকর্ষণ করে রাখে বলে আকার ছোট হয়।
একই গ্রুপে উপর থেকে নিচের দিকে গেলে পারমাণবিক সংখ্যার বৃদ্ধি সাথে সাথে নতুন শক্তি স্তরের সৃষ্টি হয়। ফলে নিউক্লিয়াস থেকে সর্বশেষ শক্তিস্তরের ইলেকট্রনের দূরত্ব বৃদ্ধি পেতে থাকে। যার ফলে নিউক্লিয়াস ও সর্বশেষ ইলেকট্রনের মধ্যবর্তী আকর্ষণ বল কমতে থাকে। ফলে সর্বশেষ শক্তি স্তর থেকে ইলেকট্রন অপসারণ করতে কম তাপের প্রয়োজন হয়। যার ফলে একই গ্রুপে উপর থেকে নিচের দিকে গেলে গলনাঙ্কের মান কমতে থাকে।
গ্যাসীয় অবস্থায় কোনো মৌলের এক মোল গ্যাসীয় পরমাণু থেকে এক মোল ইলেকট্রন অপসারণ করে এক মোল ধনাত্মক আয়নে পরিণত করতে যে শক্তির প্রয়োজন হয়, তাকে ঐ মৌলের আয়নিকরণ শক্তি বলা হয়। আয়নিকরণ শক্তি একটি পর্যায়বৃত্ত ধর্ম। একই পর্যায়ে পারমাণবিক ব্যাসার্ধ কমলে আয়নিকরণ শক্তির মান বাড়ে। আবার পর্যায়ের ডানদিকে পারমাণবিক ব্যাসার্ধ কম বলে আয়নিকরণ শক্তির মান বেশি।
ইলেকট্রন আসক্তি একটি পর্যায়বৃত্ত ধর্ম। একই পর্যায়ের বামের মৌলের পারমাণবিক ব্যাসার্ধ বেশি এবং ডানের মৌলের পারমাণবিক ব্যাসার্ধ কম। পারমাণবিক ব্যাসার্ধ কমলে ইলেকট্রন আসক্তির মান বাড়ে এবং পারমাণবিক ব্যাসার্ধ বাড়লে ইলেকট্রন আসক্তির মান কমে। এ যেমন ৩য় পর্যায়ের সর্ববামের মৌল Na এবং সর্বডানের মৌলCl , CI এর আকার ছোট বলে এর ইলেকট্রন আসক্তি সবচেয়ে বেশি।
জানা আছে, একই পর্যায়ের যত বাম থেকে ডানে যাওয়া যায় পরমাণুর আকার তত ক্ষুদ্র হয় এবং ইলেকট্রন আসক্তির মান তত বৃদ্ধি পায়। Na ও CI পর্যায় সারণির ৩য় পর্যায়ের মৌল। Na সর্ববামে ও CI সর্বডানে অবস্থিত হওয়ায় Na অপেক্ষা C এর ইলেকট্রন আসক্তি বেশি।
F ও CI এর সর্বশেষ শক্তিস্তরে ইলেকট্রন সংখ্যা 7 কিন্তু 'F এর সর্বশেষ ইলেকট্রনগুলো ২য় শক্তিস্তরে এবং CI এর ইলেকট্রনগুলো ৩য় শক্তিস্তরে থাকে। F এর আকার ছোট হওয়ায় ২য় শক্তিস্তরে ইলেকট্রন মেঘের ঘনত্ব বেশি। ফলে নতুন ইলেকট্রন আগমনে বিকর্ষণ বৃদ্ধি পায়। তাই C' এর ইলেকট্রন আসক্তির মান F এর তুলনায় বেশি।
Na, Mg, Al, Si এর মৌলগুলো পর্যায় সারণির ১নং পর্যায়ের মৌল। এই মৌলগুলোর মধ্যে Na এর পারমাণবিক ব্যাসার্ধের মান সবচেয়ে বেশি এজন্য সোডিয়াম এর ইলেকট্রন আসক্তির মান সবচেয়ে কম। আবার, Si এর পারমাণবিক ব্যাসার্ধের মান সবচেয়ে কম সেজন্য এর ইলেকট্রন আসক্তির মান সবচেয়ে বেশি।
দুটি পরমাণু যখন সমযোজী কন্ধনে আবদ্ধ হয়ে অণুতে পরিণত হয়, তখন অণুর পরমাণুগুলো বন্ধনের ইলেকট্রন দুটিকে নিজের দিকে আকর্ষণ করে; এই আকর্ষণকে বলা হয় তড়িৎ ঋণাত্মকতা। সাধারণত কোনো মৌলের পরমাণুর আকার ছোট হলে তড়িৎ ঋণাত্মকতার মান বেশি হয় এবং কোনো মৌলের পরমাণুর আকার বড় হলে তড়িৎ ঋণাত্মকতার মান কম হয়।
তড়িৎ ঋণাত্মকতা একটি পর্যায়বৃত্ত ধর্ম। জানা আছে, একই পর্যায়ের রামের মৌলের পারমাণবিক ব্যাসার্ধ বেশি এবং ডানের মৌলের পারমাণবিক ব্যাসার্ধ কম। আর পারমাণবিক ব্যাসার্ধ কমলে তড়িৎ ঋণাত্মকতার মান বাড়ে এবং পারমাণবিক ব্যাসার্ধ বাড়লে তড়িৎ ঋণাত্মকতার মান কমে। উদাহরণস্বরূপ, ৩য় পর্যায়ের সর্ববামের মৌল Na এর আকার সবচেয়ে বড় বলে তড়িৎ ঋণাত্মকতার মান সবচেয়ে কম। আবার এই পর্যায়ের সর্বডানের মৌল CI এর আকার সবচেয়ে ছোট বলে তড়িৎ ঋণাত্মকতার মান সবচেয়ে বেশি।
একই পর্যায়ের যত বাম থেকে ডানে যাওয়া যায় মৌলের আকার তত কমে, শেয়ারকৃত ইলেকট্রনের প্রতি আকর্ষণ বৃদ্ধি পায় ফলে তড়িৎ ঋণাত্মকতা বৃদ্ধি পায়। P ও CI একই পর্যায়ের মৌল এবং CI ডানে অবস্থিত হওয়ায় CI এর আকার ছোট তাই তড়িৎ ঋণাত্মকতা বেশি। অর্থাৎ CI অপেক্ষা P এর তড়িৎ ঋণাত্মকতা কম।
পর্যায় সারণির নং গ্রুপের Li, Na, K, Rb, Cs ও Fr এই 6টি মৌলকে ক্ষার ধাতু বলে। । নং গ্রুপের এই মৌলগুলো ইলেকট্রন ত্যাগ করতে পারে বলে এদেরকে ধাতু বলা হয়। আর এ ধাতুগুলো পানিতে দ্রবীভূত হয়ে হাইড্রোজেন গ্যাস এবং ক্ষার তৈরি করে বলে এরা ক্ষার ধাতু।
ইলেকট্রন বিন্যাস অনুসারে, এটি গ্রুপ-1-এ অবস্থিত। কারণ কোনো পরমাণুর যোজ্যতাস্তরে কেবল s orbital থাকলে এবং পূর্বের শক্তিস্তরে d orbital না থাকলে যোজ্যতা স্তরের মোট ইলেকট্রন সংখ্যা গ্রুপ ! নির্দেশ করে। যেহেতু K এর যোজ্যতা স্তরে 1টি e- আছে, সেহেতু এটি গ্রুপ-1 নং এর মৌল।
পর্যায় সারণিতে গ্রুপ-1 এ অবস্থিত মৌলসমূহ যথা: Li, Na, K, Rb, Cs এবং Fr কে ক্ষার" বলা হয়। কারণ এরা প্রত্যেকেই পানির সাথে বিক্রিয়া করে হাইড্রোলে গ্যাস ও ক্ষার তৈরি করে। যেমন,
Na গ্রুপ-1 এর মৌল এবং পানির সাথে বিক্রিয়া করে তীব্র ক্ষারীয় NaOH যৌগ উৎপন্ন করে।
বিক্রিয়া: 2Na + 2H2O→2NaOH + H2
আবার NaOH অম্লের অম্লত্বকে বিনষ্ট করতে পারে এবং বিক্রিয়ায় লবণ ও পানি উৎপন্ন করে।
NaOH + HCl NaCl + H2O
রুডিয়াম (Rb) কে ক্ষারধাতু বলা হয়। কারণ এটি গ্রুপ-1 এ অবস্থিত মৌল এবং পানির সাথে বিক্রিয়া করে তীব্র ক্ষার (RbOH) তৈরি করে।
বিক্রিয়া :
গ্রুপ-2 এ অবস্থিত Be থেকে শুরু করে Ra পর্যন্ত মৌলসমূহকে মৃৎক্ষার ধাতু বলা হয়। এদের ধর্ম অনেকটা ক্ষার ধাতুর মতোই। এদের অক্সাইডসমূহ পানিতে ক্ষারীয় দ্রবণ তৈরি করে। এরাও সর্ববহিঃস্থ শক্তিস্তরের ২টি ইলেকট্রন প্রদান করে আয়নিক যৌগ (লবণ) তৈরি করে। এ মৌলসমূহ বিভিন্ন যৌগ হিসেবে মাটিতে থাকে।
পর্যায় সারণির গ্রুপ-2 এর মৌলসমূহকে মৃৎক্ষার ধাতু বলা হয়। এদের ২টি বৈশিষ্ট্য নিচে উল্লেখ করা হলো-(i) এসব ধাতু পানির সাথে বিক্রিয়ায় ক্ষার উৎপন্ন করে, তাই এদের অক্সাইড ক্ষারীয়।
(ii) এদেরকে মাটির উপাদানরূপে পাওয়া যায় এবং অধাতব মৌলের সাথে আয়নিক যৌগ গঠন করে।
পর্যায় সারণির ২নং গ্রুপের Be, Mg, Ca, Sr, Ba, Ra এই ৬টি ধাতুকে বলা হয় মৃৎক্ষার ধাতু। পৃথিবীর উপরিভাগের মাটির আবরণ হলো ভূ-ত্বক। ভূ-ত্বকে বিভিন্ন ধাতু যৌগরূপে বিদ্যমান। ম্যাগনেশিয়াম (Mg) কে মাটির নিচে যৌগ রূপে পাওয়া যায় বলেই Mg কে মৃৎক্ষার ধাতু বলে। Mg মাটিতে MgO রূপে বিদ্যমান থাকে।
বেরিলিয়ামকে (Be)-কে মৃৎক্ষার ধাতু বলা হয়; এর কারণ হলো এটি গ্রুপ-2 এর মৌল এবং এদের অক্সাইডসমূহ পানিতে ক্ষারীয় দ্রবণ তৈরি করে। এছাড়া মৌলটি বিভিন্ন যৌগ হিসেবে মাটিতে থাকে।
বিক্রিয়া:
ক্যালসিয়ামকে (Ca)-কে মৃৎক্ষার ধাতু বলা হয়; এর কারণ হলো এটি গ্রুপ-2 এর মৌল এবং এদের অক্সাইডসমূহ পানিতে ক্ষারীয় দ্রবণ তৈরি করে। এছাড়া মৌলটি বিভিন্ন যৌগ হিসেবে মাটিতে থাকে।
বিক্রিয়া: Ca + 2H2O → Ca(OH)2 + H2(g)
সোনা, রুপা প্রভৃতি ধাতু তুলনামূলকভাবে কম সক্রিয় হওয়ায় এদেরকে অন্য কোনো মৌলের সাথে যুক্ত হতে দেখা যায় না। এমনকি এরা সাধারণ ঘনমাত্রার এসিড বা' ক্ষার দ্বারাও আক্রান্ত হয় না। এসব ধাতুর মাঝে স্থায়ী উজ্জ্বলতা বর্তমান থাকে এবং এদেরকে ধাতব মুদ্রা হিসেবে যথেষ্ট ব্যবহার করা হয়। এজন্যই সোনা, রূপা প্রভৃতি ধাতুকে অভিজাত ধাতু হিসেবে অভিহিত করা হয়।
গ্রুপ-17 এর F, Cl, Br, L, At ও Ts কে হ্যালোজেন বলা হয়। কারণ হ্যালোজেন এর অর্থ লবণ উৎপাদনকারী এবং এর মূল উৎস সামুদ্রিক লবণ। হ্যালোজেন মৌলগুলোর সাথে ধাতু যুক্ত হয়ে লবণ গঠন করে। যেমন- Na ধাতু হ্যালোজেন মৌল CI এর সাথে যুক্ত হয়ে NaCl লবণ গঠন করে। Na + Cl2→ 2NaCl
হ্যালোজেন মানে লবণ উৎপাদনকারী। এর মূল উৎস সামুদ্রিক লবণ। হ্যালোজেন মৌলগুলোর সাথে ধাতু যুক্ত হয়ে লবণ গঠিত হয়। যেমন F এর সাথে Na ধাতু যুক্ত হয়ে সোডিয়াম ফ্লোরাইড লবণ রা খাদ্য লবণ (NaF) গঠিত হয়। এজন্যই ফ্লোরিন (F) কে হ্যালোজেন বলা হয়।
নিষ্ক্রিয় গ্যাসের ইলেকট্রন বিন্যাস (……..ns2 np6 )হতে দেখা যায় এদের সর্ববহিঃস্থ স্তর অষ্টকপূর্ণ অবস্থায় থাকে। ফলে এরা ইলেকট্রন আদান-প্রদান বা শেয়ার করতে আগ্রহ প্রকাশ করে না এবং কোনো মৌলের সাথে রাসায়নিকভাবে যুক্ত হতে পারে না। তাই নিষ্ক্রিয় গ্যাসসমূহ সক্রিয় নয়।
পর্যায় সারণির গ্রুপ নং 18-এ অবস্থিত মৌলসমূহকে (Ne, Ar, Kr....…)নিষ্ক্রিয় মৌল বলা হয়। এদের সর্ববহিঃস্থ শক্তিস্তরে প্রয়োজনীয় সংখ্যক ইলেকট্রন দ্বারা অষ্টকপূর্ণ (ns2 np6) থাকায় এরা ইলেকট্রন আদান-প্রদান বা শেয়ারের মাধ্যমে যৌগ গঠনে সাধারণত আগ্রহ প্রকাশ করে না। এ কারণেই নিষ্ক্রিয় গ্যাসগুলো সাধারণত নিষ্ক্রিয় হয়।
হিলিয়ামের ইলেকট্রন বিন্যাস He (2) = 1s 2 অর্থাৎ 1s অরবিটাল ইলেকট্রন দ্বারা পূর্ণ থাকে। ১ম পর্যায়ের অন্য কোনো - অরবিটাল না থাকায়-এবং অরবিটাল ইলেকট্রন দ্বারা পূর্ণ থাকায় হিলিয়াম মৌলটি অন্য কোনো মৌল এমনকি আরেকটি হিলিয়ামের সাথে যুক্ত হতে পারে না। ইলেকট্রন দান বা গ্রহণ এবং শেয়ারের 'মাধ্যমে যৌগ গঠন করতে পারে না বলে এটি নিষ্ক্রিয় গ্যাস।
10X এর ইলেকট্রন বিন্যাস (1s2 2s22p6)-এ সর্ববহিঃস্থ স্তরে ইলেকট্রন দ্বারা অষ্টক পূর্ণ থাকে, যা অত্যন্ত সুস্থিত। এ সুস্থিত ইলেকট্রন বিন্যাস ভাঙতে অনেক শক্তির প্রয়োজন। তাই X তথা Ne স্বাভাবিক অবস্থায় কোনো মৌলের সাথে যুক্ত হয় না। অর্থাৎ বহিঃস্থ স্তরের সুবিন্যস্ত ইলেকট্রন বিন্যাসের কারণে উক্ত মৌলটি নিষ্ক্রিয় হয়।
আর্গন (Ar) নিষ্ক্রিয় গ্যাস। কারণ, 18Ar এর (1s2 2s22p6 3s6 3s2 3p6) সর্ববহিঃস্থ স্তরে ইলেকট্রন দ্বারা অষ্টক পূর্ণ থাকে, যা অত্যন্ত সুস্থিত। এ সুস্থিত ইলেকট্রন বিন্যাস ভাঙতে অনেক শক্তির প্রয়োজন। তাই Ar স্বাভাবিক তাবস্থায় কোনো মৌলের সাথে যুক্ত হয় না। অর্থাৎ বহিঃস্থ স্তরের সুবিন্যস্ত ইলেকট্রন বিন্যাসের কারণে Ar নিষ্ক্রিয় হয়।
ক্রিপ্টন এর ইলেকট্রন বিন্যাস-
দেখা যাচ্ছে, যোজ্যতা স্তরে ৪টি ইলেকট্রন থাকে অর্থাৎ অষ্টকপূর্ণ। এজন্য এটি অন্য কোনো মৌলের সাথে বিক্রিয়া করে না। অর্থাৎ বহিঃস্থ স্তরের সুবিন্যস্ত ইলেকট্রন বিন্যাসের কারণে Kr নিষ্ক্রিয় মৌল।
পর্যায় সারণির যেসব এ ব্লকভুক্ত মৌলের সর্বশেষ স্তরের d অরবিটাল ইলেকট্রন দ্বারা আংশিকভাবে (d1-9) পূর্ণ থাকে তাদেরকে অবস্থান্তর মৌল বলে। যেমন- Cr, Ni, Cu ইত্যাদি অবস্থান্তর মৌল। অবস্থান্তর মৌলসমূহের নিজস্ব বর্ণ আছে, এরা পরিবর্তনশীল যোজনী প্রদর্শন করে এবং প্রভাবক হিসাবে কাজ করতে পারে।
অবস্থান্তর মৌলের ২টি বৈশিষ্ট্য নিম্নরূপ:
১. অবস্থান্তর মৌলসমূহ পরিবর্তনশীল যোজনী প্রদর্শন করে।
২. অবস্থান্তর মৌলসমূহ রঙিন ও জটিল যৌগ গঠন করে।
যেসব ধাতব মৌলের সুস্থিত আয়নের -অরবিটাল আংশিকভাবে ইলেকট্রন দ্বারা পূর্ণ থাকে, সেগুলোকে অবস্থান্তর মৌল বলা হয়।
Cu এর ইলেকট্রন বিন্যাস নিম্নরূপ-
Cu এর সুস্থিত আয়নের ইলেকট্রন বিন্যাস লক্ষ করলে দেখা যায় d-অরবিটাল আংশিকভাবে পূর্ণ রয়েছে। তাই Cu কে অবস্থান্তর মৌল বলা হয়।
যে সকল d-ব্লক মৌলের স্থায়ী আয়নে d-অরবিটালের ইলেকট্রন বিন্যাস d1-9 হয় তাদেরকে অবস্থান্তর মৌল বলা হয়। এক্ষেত্রে Zn এর স্থায়ী আয়ন Zn2+ এর ইলেকট্রন বিন্যাস হলো Zn2+(30) = 1s2 2s2 2p6 3s2 3p6 3d10 4sº যেহেতু এ অরবিটালের ইলেকট্রন বিন্যাস d1-9নয়, তাই Zn কে অবস্থান্তর মৌল বলা হয় না।
পর্যায় সারণির যেসব ঐ ব্লকভুক্ত মৌলের সর্বশেষ স্তরের d অরবিটাল ইলেকট্রন দ্বারা আংশিকভাবে (d1-9) পূর্ণ থাকে তাদেরকে অবস্থান্তর মৌল বলে। যেমন- Cr, Ni, Cu ইত্যাদি অবস্থান্তর -মৌল। অবস্থান্তর মৌলসমূহের নিজস্ব বর্ণ আছে, এরা পরিবর্তনশীল যোজনী প্রদর্শন করে এবং প্রভাবক হিসাবে কাজ করতে পারে।
অবস্থান্তর মৌলের ২টি বৈশিষ্ট্য নিম্নরূপ:
১. অবস্থান্তর মৌলসমূহ পরিবর্তনশীল যোজনী প্রদর্শন করে।
২. অবস্থান্তর মৌলসমূহ রঙিন ও জটিল যৌগ গঠন করে।
যেসব ধাতব মৌলের সুস্থিত আয়নের d-অরবিটাল আংশিকভাবে ইলেকট্রন দ্বারা পূর্ণ থাকে, সেগুলোকে অবস্থান্তর মৌল বলা হয়।
Cu এর ইলেকট্রন বিন্যাস নিম্নরূপ-
Cu এর সুস্থিত আয়নের ইলেকট্রন বিন্যাস লক্ষ করলে দেখা যায় d-অরবিটাল আংশিকভাবে পূর্ণ রয়েছে। তাই Cu কে অবস্থান্তর মৌল বলা হয়।
যে সকল d-বুক মৌলের স্থায়ী আয়নে d-অরবিটালের ইলেকট্রন বিন্যাস d1-9 হয় তাদেরকে অবস্থান্তর মৌল বলা হয়। এক্ষেত্রে Zn এর স্থায়ী আয়ন Zn2+ এর ইলেকট্রন বিন্যাস হলো
যেহেতু d অরবিটালের ইলেকট্রন বিন্যাস d1-9 নয়, তাই Zn কে অবস্থান্তর মৌল বলা হয় না।
যে সকল এ-ব্লক মৌলের স্থায়ী আয়নের ইলেকট্রন বিন্যাস করলে এ অরবিটালে ইলেকট্রন সংখ্যা 1-9টি হয় তাদেরকে অবস্থান্তর মৌল বলে। আয়রন তথা Fe এর একটি স্থায়ী আয়ন হচ্ছে Fe+2। এর ইলেকট্রন বিন্যাস করলে d অরবিটালে ইলেকট্রন সংখ্যা 6টি (যা, 1-9 এর মধ্যে) হয়। তাই Fe কে অবস্থান্তর মৌল বলা হয়।
যেমন-26Fe2+ --1s2 2s2 2p6 3s2 3p6 3d6 4s2
যে সকল মৌলের সুস্থিত আয়নে এ-অরবিটাল ইলেকট্রন দ্বারা পূর্ণ বা শূন্য থাকলে তারা d-ব্লক মৌল হওয়া সত্ত্বেও অবস্থান্তর মৌল নয়। Sc(21) এর ইলেকট্রন বিন্যাস-
Sc(21) = 1s2 2s2 2p6 3s2 3p6 3d1 4s2
সুস্থিত আয়নে ইলেকট্রন বিন্যাস :
Sc3+(21) = 1s2 2s2 2p6 3s2 3p6 3d0 4s0
দেখা যাচ্ছে, Sc এর সুস্থিত আয়নে 3d অরবিটালে কোনো e- নেই।
কাজেই Sc মৌলটি d ব্লকভুক্ত হলেও অবস্থান্তর নয়।
যে সকল এ-ব্লক মৌলের ইলেকট্রন বিন্যাসে d-অরবিটাল ইলেকট্রন দ্বারা আংশিকভাবে (d1-9) পূর্ণ থাকে তাদেরকে অবস্থান্তর মৌল বলে। যে সকল মৌলের সুস্থিত আয়নে এ-অরবিটাল ইলেকট্রন দ্বারা পূর্ণ বা শূন্য থাকলে তারা এ-ব্লক মৌল হওয়া সত্ত্বেও অবস্থান্তর মৌল নয়। যেমন Sc3+ (21)= …….3d° এবং Zn2+ =.....3d104s0মৌল দুটি d-ব্লক মৌল হওয়া সত্ত্বেও অবস্থান্তর নয়। তাই বলা যায়, সকল d-ব্লক মৌলই অবস্থান্তর মৌল নয়।
আধুনিক পর্যায়সারণিটিতে তথা 7টি পর্যায় ও 1৪টি গ্রুপ নিয়ে গঠিত পর্যায় সারণিতে বেশ কিছু ফাঁকা ঘর ছিল। ঐ ফাঁকা ঘরের মৌলের ধর্ম কীরূপ হবে তা মৌলগুলো আবিষ্কারের পূর্বেই পর্যায় সারণি থেকে ধারণা পাওয়া গিয়েছিল। মৌলগুলো আবিষ্কারের পর পরবর্তীতে মৌলগুলোর ভবিষ্যৎদ্বাণী মিলে গিয়েছিলো। এক্ষেত্রে to পর্যায় সারণির ভূমিকাই ছিলো মুখ্য।
রসায়ন পাঠ সহজীকরণে পর্যায় সারণির ২টি সুবিধা হলো-
১. প্রতিটি গ্রুপের সাধারণ ধর্ম জানলে 11৪টি মৌলের ভৌত ও রাসায়নিক ধর্ম সম্বন্ধে ধারণা লাভ করা যায়।
২. পর্যায় সারণি সম্পর্কে ভালোভাবে ধারণা থাকলে বিভিন্ন মৌল দ্বারা গঠিত যৌগের ধর্ম সম্পর্কেও ধারণা লাভ করা যায়।
গবেষণার ক্ষেত্রে পর্যায় সারণির অসামান্য অবদান রয়েছে। যেমন কোনো বিজ্ঞানী বিশেষ প্রয়োজনে নতুন কোনো পদার্থ আবিষ্কার করতে চাইলেন। এক্ষেত্রে তাঁকে পর্যায় সারণি থেকেই ধারণা নিতে হবে যে, নতুন পদার্থটির ধর্ম কেমন হবে এবং নতুন পদার্থ তৈরিতে কী কী মৌলের প্রয়োজন হবে তা সবই পর্যায় সারণি থেকে ধারণা পাওয়া সম্ভব।
CI2 ও Br2 একই ধরনের বিক্রিয়া প্রদর্শন করে। কারণ মৌল দুটি একই গ্রুপ-17 এর অন্তর্ভুক্ত। এ গ্রুপের মৌলগুলো হ্যালোজেন নামে পরিচিত। এরা ধাতুর সাথে যুক্ত হয়ে ধাতুর হ্যালাইড(KCI, KBr) গঠন করে। যেমন,
আবার হাইড্রোজেন (H2) এর সাথে যুক্ত হয়ে হাইড্রাসিড গঠন করে।
সুতরাং Br2 ও Cl2 একই ধরনের বিক্রিয়া প্রদর্শন করে।
হ্যালোজেন গ্রুপের মৌলগুলো হলো- F2, Cl2, Br2 12 । এ মৌলগুলোর সাথে হাইড্রোজেন গ্যাসের বিক্রিয়া নিম্নরূপ-
ধাতুর যেসব অক্সাইড পৃথক পৃথকভাবে এসিড ও ক্ষারকের সাথে বিক্রিয়া করে প্রতিক্ষেত্রে লবণ ও পানি উৎপন্ন করে তাদেরকে উভধর্মী অক্সাইড বলে।
AI2O3 একটি উভধর্মী অক্সাইড। কারণ এটি এসিড যেমন HCI এবং ক্ষার NaOH এর সাথে পৃথকভাবে বিক্রিয়া করে লবণ ও পানি উৎপন্ন করে।
ক্ষারকরূপে
এসিডরূপে
ধাতুর অক্সাইড পানির সাথে বিক্রিয়া করে ধাতুর হাইড্রোক্সাইড উৎপন্ন করে এবং এসিডের সাথে বিক্রিয়া করে লবণ ও পানি উৎপন্ন করে-
বিক্রিয়া:
তাই ধাতুর অক্সাইড ক্ষারধর্মী।
প্রায় একই ধরনের ধর্মবিশিষ্ট মৌলসমূহকে একই শ্রেণিভুক্ত করে আবিষ্কৃত সব মৌলকে স্থান দিয়ে মৌলসমূহের যে সারণি বর্তমানে প্রচলিত তাই পর্যায় সারণি।
ম্যান্ডেলিফের পর্যায় সূত্রটি হলো:
"মৌলসমূহের ভৌত ও রাসায়নিক ধর্মাবলি তাদের পারমাণবিক ভর বৃদ্ধির সাথে পর্যায়ক্রমে আবর্তিত হয়।"
পারমাণবিক ভর অনুসারে তিনটি করে মৌলকে সাজালে দ্বিতীয় মৌলের পারমাণবিক ভর প্রথম ও তৃতীয় মৌলের পারমাণবিক ভরের যোগফলের অর্ধেক বা তার কাছাকাছি, যাকে ডোবেরাইনারের ত্রয়ীসূত্র বলা হয়।
মৌলগুলোকে তাদের পারমাণবিক ভর অনুযায়ী সাজালে প্রতি অষ্টম মৌলসমূহের ধর্মের মিল দেখা যায়, যা পর্যায় সারণির 'অষ্টক তত্ত্ব' নামে পরিচিত।
নিউল্যান্ডের অষ্টক সূত্রটি হচ্ছে "মৌলসমূহকে যদি পারমাণবিক ভরের ছোট থেকে বড় অনুযায়ী সাজানো যায়, তবে যেকোনো পর্যায়ের ১ম একটি মৌলের ধর্ম তার অষ্টম মৌলের ধর্মের সাথে মিলে যায়"।
IUPAC এর পূর্ণরূপ: International Union of Pure and
Applied Chemistry |
পারমাণবিক সংখ্যার আবিষ্কারক ইলেন বিজ্ঞানী হেনরি মোসলে।
পর্যায় সারণির বাম থেকে ডান পর্যন্ত বিস্তৃত সারিগুলোকে পর্যায় বলে।
আধুনিক পর্যায় সূত্রটি হলো- বিভিন্ন মৌলের ভৌত ও রাসায়নিক ধর্মাবলি তাদের পারমাণবিক সংখ্যা বৃদ্ধি অনুসারে পর্যায়ক্রমে আবর্তিত হয়।
সংশোধিত পর্যায় সূত্র হলো- মৌলসমূহের ভৌত ও রাসায়নিক ধর্মাবলি তাদের পারমাণবিক সংখ্যা অনুযায়ী আবর্তিত হয়।
আর্সেনিকের পারমাণবিক সংখ্যা 33।
Rb ধাতুর অবস্থান গ্রুপ-।-এ।
গ্যাসীয় অবস্থায় কোনো মৌলের এক মোল গ্যাসীয় পরমাণু থেকে এক মোল ইলেকট্রন অপসারণ করে এক মোল ধনাত্মক আয়নে পরিণত করতে যে শক্তির প্রয়োজন হয়, তাকে ঐ মৌলের আয়নিকরণ শক্তি বলে
দুটি পরমাণু যখন সমযোজী বন্ধনে আবদ্ধ হয়ে অণুতে পরিণত হয় তখন অণুর পরমাণুগুলো বন্ধনের ইলেকট্রন দুটিকে নিজের দিকে আকর্ষণ করে, এই আকর্ষণকে তড়িৎ ঋণাত্মকতা বলে।
গ্যাসীয় অবস্থায় কোনো মৌলের এক মৌল গ্যাসীয় পরমাণুতে এক মোল ইলেকট্রন প্রবেশ করিয়ে এক মৌল ঋণাত্মক আয়নে পরিণত করতে যে শক্তি নির্গত হয়, তাকে ঐ মৌলের ইলেকট্রন আসক্তি বলে।
পর্যায় সারণিতে অবস্থিত মৌলগুলোর কিছু ধর্ম যেমন, ধাতব ধর্ম, অধাতব ধর্ম, পরমাণুর আকার, আয়নিকরণ শক্তি, তড়িৎ ঋণাত্মকতা ইত্যাদি ধর্মসমূহকে পর্যায়বৃত্ত ধর্ম বলে।
পর্যায় সারণির গ্রুপ 11 নং এর 4টি মৌল (Cu, Ag, Au, Rg) এর মধ্যে ১ম ওটি মৌল (Cu, Ag, Ag) কে মুদ্রা ধাতু বলে।
পর্যায় সারণির গ্রুপ 11 নং এর 4টি মৌল (Cu, Ag, Au, Rg) এর মধ্যে ১ম ওটি মৌল (Cu, Ag, Ag) কে মুদ্রা ধাতু বলে।
যেসব মৌলের স্থিতিশীলতা আয়নের ইলেকট্রন বিন্যাসে d অরবিটাল আংশিক পূর্ণ থাকে অর্থাৎ d1-9 হয় তাদেকে অবস্থান্তর মৌল বলে।
পর্যায় সারণির গ্রুপ-17 এর 6টি মৌল (F, Cl, Br, 1, At ও Ts) কে হ্যালোজেন বলে।
পর্যায় সারণির গ্রুপ-1 এর অন্তর্ভুক্ত 6টি মৌল Li, Na, K, Rb, Cs ও Fr কে ক্ষার ধাতু বলা হয়।
হ্যালোজেন এর অর্থ হলো লবণ উৎপাদনকারী, সারণির গ্রুপ-117 এর 6টি মৌলসমূহ F, Cl, Br, I, At ও Ts।
পর্যায় সারণির গ্রুপ ।৪ এ অবস্থিত He, Ne, Ar, Kr, Xe, Rn এই 6 টি গ্যাসীয় মৌলকে নিষ্ক্রিয় গ্যাস বলে।
হ্যালোজেনসমূহের মূল উৎস সামুদ্রিক লবণ।
মুদ্রা ধাতুগুলো (Cu, Ag, Au) পর্যায় সারণির গ্রুপ-11-তে অবস্থিত।
যে সকল মৌলের পারমাণবিক সংখ্যা 89 থেকে 103 পর্যন্ত এ রকম 15টি মৌলকে অ্যাকটিনাইড় মৌল বলা হয়।
যে সকল মৌল এক বা একাধিক ইলেকট্রন ত্যাগ করে ধনাত্মক আয়নে পরিণত হয় তাদেরকে ধাতু বলে।
যে সকল মৌল এক বা একাধিক ইলেকট্রন গ্রহণ করে ঋণাত্মক আয়নে পরিণত হয় তাদেরকে অধাতু বলে।
একটি অভিজাত ধাতু হলো- রূপা (Ag)।
ধাতুর অক্সাইডসমূহ ক্ষারধর্মী।
ক্ষার ধাতুর সাথে পানির বিক্রিয়ায় হাইড্রোজেন গ্যাস ও ক্ষার দ্রবণ তৈরি হয়।
রাসায়নিকভাবে সদৃশ প্রতি ১টি মৌল শ্রেণির মাঝের মৌলটির পারমাণবিক ভর মোটামুটিভাবে অপর মৌল দুটির পারমাণবিক ভরের গড় হয়- এটিই ডোবেরাইনার ত্রয়ী সূত্র। উদাহরণ, লিথিয়াম (7) ও পটাসিয়াম (39) এর পারমাণবিক ভরের গড় সোডিয়াম (23) এর পারমাণবিক ভরের প্রায় সমান।
Sc(21) এর ইলেকট্রন বিন্যাস-
Sc(21) Is2 2s2 2p0 3s2 3p6 3d1 4s2
পর্যায় নির্ণয় : ইলেকট্রন বিন্যাস চারটি স্তরে বিন্যস্ত হওয়ায় এটি ৪র্থ পর্যায়ের মৌল।
গ্রুপ নির্ণয় : সর্বশেষ ইলেকট্রন এ অরবিটালের প্রবেশ করায় (n-1)d ও ns অরবিটালের মোট ইলেকট্রন গ্রুপ নির্দেশ করে। অর্থাৎ 1+2=
3 নং গ্রুপে Sc মৌলটি অবস্থিত।
15 পারমাণবিক সংখ্যাবিশিষ্ট মোল P। কোনো মৌলের সর্ববহিঃস্থ শেলের ইলেকট্রন সংখ্যা অনুসারে তার গ্রুপ এবং শেলের স্তরের সংখ্যা অনুসারে পর্যায় নির্ধারণ করা হয়। ফসফরাস (15) এর ইলেকট্রন বিন্যাস 2, 8, 5। এর শেল সংখ্যা ১টি এবং সর্ববহঃস্থ স্তরে ইলেকট্রন সংখ্যা 5টি। সুতরাং ফসফরাস ৩য় পর্যায়ের 5 + 10 = 15 নং গ্রুপে অবস্থান করবে।
20 পারমাণবিক সংখ্যাবিশিষ্ট মৌলের ইলেকট্রন বিন্যার্স
নিম্নরূপ- 1s22s2 2p6 3s2 3p64s2
ইলেকট্রন বিন্যাস অনুযায়ী, ইলেকট্রনগুলো চারটি শক্তিস্তরে বিন্যস্ত।
কাজেই মৌলটির অবস্থান হবে চতুর্থ পর্যায়ে।
আবার, সর্ববহিঃস্থ শক্তিস্তরে ইলেকট্রন সংখ্যা 2 ।
অতএব, মৌলটির গ্রুপ সংখ্যা হবে 2 ।
ইলেকট্রন বিন্যাসের মাধ্যমে কোন মৌলাটর কত নম্বর পর্যায় ও কত নম্বর গ্রুপ তা নির্ণয় করা যায়। পারমাণবিক ভর দ্বারা পর্যায় সারণিতে মৌলের অবস্থান নির্ণয় করলে K (পা: ভর 39) ও Ar (পা: ভর 40) সহ অনেক মৌলের ক্ষেত্রে সমস্যা দেখা যায়। কিন্তু ইলেকট্রন বিন্যাস দ্বারা মৌলের অবস্থান নির্ণয় করলে সে সমস্যা দূর হয়।
এজন্য ইলেকট্রন বিন্যাসই পর্যায় সারণির মূল ভিত্তি।
হিলিয়ামকে গ্রুপ-18 তে রাখা হয়। কারণ He এর ইলেকট্রন বিন্যাস He(2) = 1s2। He এর সর্বশেষ কক্ষপথ ইলেকট্রন দ্বারা পূর্ণ থাকে। এজন্য এটি অপর কোনো মৌলের সাথে ইলেকট্রন গ্রহণ, 'বর্জন বা শেয়ার করে না। অর্থাৎ নিষ্ক্রিয় অবস্থায় থাকে। আবার 18 নং গ্রুপ হচ্ছে নিষ্ক্রিয় মৌলসমূহের গ্রুপ। এক্ষেত্রে মৌলগুলোর ইলেকট্রন বিন্যাসে সর্ববহিঃস্থ স্তর ইলেকট্রন দ্বারা অষ্টক পূর্ণ, যা স্থিতিশীল'। যার জন্য অন্য মৌলের সাথে e-শেয়ার বা আদান-প্রদান করে না। অর্থাৎ, নিষ্ক্রিয় অবস্থায় থাকে। তাই He কে নিষ্ক্রিয় গ্যাসের সাথে গ্রুপ-18 তে রাখা হয়।
হিলিয়াম (He) এর ইলেকট্রন বিন্যাস 1s2। অর্থাৎ হিলিয়ামের (He) সর্বশেষ কক্ষপথে ২টি ইলেকট্রন রয়েছে। তাই স্বাভাবিকভাবে Hc এর অবস্থান পর্যায় সারণিতে দ্বিতীয় গ্রুপে মৃৎক্ষার ধাতুদের সাথে হওয়া উচিত। He এর সর্বশেষ কক্ষপথ ইলেকট্রন দ্বারা পূর্ণ থাকায় He গ্রুপ-2 এর মৌলসমূহের মত সক্রিয়তা, ধাতব বৈশিষ্ট্য প্রদর্শন করে না। সর্বোপরি, মৃৎক্ষার ধাতুদের সাথে ইলেকট্রন বিন্যাস ব্যতীত বৈশিষ্ট্যগত কোন মিল না থাকায় He কে গ্রুপ-2 এ না রেখে শূন্য (0) গ্রুপে রাখা হয়েছে।
H কে গ্রুপ-1 এ স্থান দেওয়া হয়। কারণ গ্রুপ-। এর মৌলগুলোর যোজ্যতা স্তরে। টি মাত্র ইলেকট্রন থাকে। H(1)= 1s1 পরমাণুর যোজ্যতা স্তরেও ১টি মাত্র ইলেকট্রন থাকে। গ্রুপ-। এর মৌলগুলোর যোজনী-1, 1 এর যোজনীও 1। গ্রুপ-1 এর মৌলগুলো হ্যালোজেনের সাথে ধাতব হ্যালাইড (MX) গঠন করে, মও হ্যালোজেনের সাথে HX যৌগ গঠন করতে পারে। অর্থাৎ গ্রুপ-। এর বৈশিষ্ট্য H এর সাথে মিল থাকায় H কে গ্রুপ-। এ স্থান দেওয়া হয়েছে।
একই পর্যায়ে যতই বাম হতে ডানে যাওয়া যায়, পরমাণুর আকার ততই হ্রাস পেতে থাকে। তাই সর্ববহিঃস্থ স্তরের ইলেকট্রন এর প্রতি আকর্ষণও তত বাড়তে থাকে। ফলে ইলেকট্রন অপসারণ করতে অধিক শক্তি প্রয়োজন হয়। সুতরাং, একই পর্যায়ে যতই বাম হতে ডানে যাওয়া যায় আয়নিকরণ শক্তির মান ততই বাড়তে থাকে। অন্যদিকে, একই গ্রুপে উপর হতে নিচের দিকে মৌলের আয়নিকরণ শক্তি হ্রাস পায়। কারণ, পর্যায় সারণির একই গ্রুপ বা শ্রেণিতে উপর হতে নিচের দিকে মৌলসমূহের পারমাণবিক সংখ্যা অর্থাৎ প্রোটন সংখ্যা বৃদ্ধি পাওয়ার সঙ্গে সঙ্গে পরমাণুর ইলেকট্রনের শক্তিস্তর সংখ্যা বৃদ্ধি পায়। ফলে পরমাণুর আকার অর্থাৎ পারমাণবিক ব্যাসার্ধ বৃদ্ধি পায়। এতে বহিঃস্থ শক্তিস্তরের ইলেকট্রনের উপর নিউক্লিয়াসের আকর্ষণ শক্তি হ্রাস পায়; অর্থাৎ কম শক্তি ব্যয় করে ইলেকট্রনকে অপসারণ করা যায়। এজন্য আয়নিকরণ শক্তি হ্রাস পায়। সুতরাং, আয়নিকরণ শক্তি একটি পর্যায়বৃত্ত ধর্ম।
সমযোজী যৌগের শেয়ারকৃত ইলেকট্রনযুগলকে 'নিজের দিকে আকর্ষণের ক্ষমতাকে মৌলের তড়িৎ ঋণাত্মকতা বলে। এই আকর্ষণের ক্ষমতা পরমাণুর আকারের উপর নির্ভর করে। পরমাণুর আকার যত 1 ছোট হবে আকর্ষণ তত বেশি হবে, তড়িৎ ঋণাত্মকতাও তত বেশি হবে। পর্যায় সারণিতে একই পর্যায়ের বাম থেকে ডানে পরমাণুর । আকার হ্রাস পায়, ফলে তড়িৎ ঋণাত্মকতা বাড়ে। আবার একই গ্রুপের উপর থেকে নিচে পরমাণুর আকার বৃদ্ধি পাওয়াতে তড়িৎ ঋণাত্মকতা হ্রাস পায়। সুতরাং, বলা যায় তড়িৎ ঋণাত্মকতা একটি পর্যায়বৃত্ত ধর্ম।
Ca ও Ca2+ এর মধ্যে Ca এর আকার বড়। কারণ Ca পরমাণুতে 20টি প্রোটন ও 20টি ইলেকট্রন আছে কিন্তু Ca2+ আয়নে 20টি প্রোটন ও 1৪টি ইলেকট্রন আছে। Ca2+ আয়নের ক্ষেত্রে 20টি প্রোটন ১৪টি ইলেকট্রনকে খুব দৃঢ়ভাবে নিউক্লিয়াসের সাথে আবদ্ধ করে রাখে বলে Ca2+ আয়নের আকার ছোট হয়। Ca এর ক্ষেত্রে 20টি প্রোটন 20টি ইলেকট্রনকে তুলনামূলক কম শক্তিতে আকৃষ্ট করে রাখে। এজন্য Ca এর আকার বড় হয়। অন্যভাবেও বলা যায়, ক্যাটায়নের আকার অপেক্ষা নিরপেক্ষ পরমাণুর আকার সাধারণত বড় হয়।
F এবং Ne এর মধ্যে F আয়নের আকার বড়। কারণ F আয়নে 9টি প্রোটন ও 10টি ইলেকট্রন থাকায় নিউক্লিয়াস' কর্তৃক বহিঃস্থ স্তরের অধিক সংখ্যক ইলেকট্রনের প্রতি আকর্ষণ কমে যায়। ফলে পরমাণুর আকার বড় হয়। পক্ষান্তরে Ne পরমাণুতে 10টি ইলেকট্রন ও 10টি প্রোটন থাকায় বহিঃস্তরে তুলনামূলক কম ইলেকট্রন থাকায় ইলেকট্রনের প্রতি নিউক্লিয়াসের আকর্ষণ অধিক হয়। ফলে পরমাণুর আকার ক্ষুদ্র হয়। এজন্য F আয়নের আকার (147 pm), যা Nc পরমাণুর আকার (38 pm) এর তুলনায় অনেক বড়।
ফ্লোরিন (F) ও ক্লোরিন (CI) এর ইলেকট্রন বিন্যাস নিম্নরূপ:
1F ও CI এর সর্বশেষ শক্তিস্তরে ইলেকট্রন সংখ্যা 7 কিন্তু F এর সর্বশেষ ইলেকট্রনগুলো ২য় শক্তিস্তরে এবং CI এর ইলেকট্রনগুলো ৩য় শক্তিস্তরে থাকে। F এর আকার ছোট হওয়ায় ২য় শক্তিস্তরে ইলেকট্রন মেঘের ঘনত্ব বেশি। ফলে নতুন ইলেকট্রন আগমনে বিকর্ষণ বৃদ্ধি - পায়। তাই F এর ইলেকট্রন আসক্তির মান CI এর তুলনায় কম।
Rb কে ক্ষারধাতু বলা হয়। কারণ এটি গ্রুপ-1 এ অবস্থিত মৌল এবং পানির সাথে বিক্রিয়া করে তীব্র ক্ষার (RbOH) তৈরি করে।
বিক্রিয়া :
পটাসিয়াম (K) কে ক্ষার ধাতু বলা 'হয়। কারণ পটাসিয়াম গ্রুপ-1 এর মৌল এবং পানির সাথে বিক্রিয়া করে তীব্র ক্ষারীয় KOH যৌগ উৎপন্ন করে।
বিক্রিয়া:
আবার KOH অম্লের অম্লত্বকে বিনষ্ট করতে পারে এবং বিক্রিয়ায় লবণ ও পানি উৎপন্ন করে।
তাই পটাসিয়ামকে ক্ষার ধাতু বলা হয়।
ক্যালসিয়ামকে (Ca)-কে মৃৎক্ষার ধাতু বলা হয়; এর কারণ হলো এটি গ্রুপ-2 এর মৌল এবং এদের অক্সাইডসমূহ পানিতে ক্ষারীয় দ্রষণ তৈরি করে। এছাড়া মৌলটি বিভিন্ন যৌগ. হিসেবে মাটিতে থাকে।
বিক্রিয়া :
Cu কে মুদ্রা ধাতু বলা হয়। কারণ প্রাচীনকালে Cu ধাতু দ্বারা মুদ্রা তৈরি হতো. এবং ব্যবসা-বাণিজ্য ও লেনদেনের মাধ্যম হিসাবে Cu ধাতুর মুদ্রা ব্যবহার করা হতো। এজন্য Cu কে মুদ্রা ধাতু বলে।
হ্যালোজেন মানে লবণ উৎপাদনকারী। এর মূল উৎস সামুদ্রিক লবণ। হ্যালোজেন মৌলগুলোর সাথে ধাতু যুক্ত হয়ে লবণ গঠিত হয়। যেমন CI এর সাথে Na ধাতু যুক্ত হয়ে সোডিয়াম ক্লোরাইড লবণ বা খাদ্য লবণ (NaCl) গঠিত হয়। এজন্যই ক্লোরিন (CI) কে হ্যালোজেন বলা হয়।
আর্গন (Ar) নিষ্ক্রিয় গ্যাস। কারণ, 18Ar এর (1s2 2s2 2p6 3s23p6) সর্ববহিঃস্থ স্তরে ইলেকট্রন দ্বারা অষ্টক পূর্ণ থাকে, যা অত্যন্ত সুস্থিত। এ সুস্থিত ইলেকট্রন বিন্যাস ভাঙতে অনেক শক্তির প্রয়োজন। তাই Ar স্বাভাবিক অবস্থায় কোনো মৌলের সাথে যুক্ত হয় না। অর্থাৎ বহিঃস্থ স্তরের সুবিন্যস্ত ইলেকট্রন বিন্যাসের কারণে Ar নিষ্ক্রিয় হয়।
নিয়ন (Ne) নিষ্ক্রিয় গ্যাস। কারণ, 10Ne এর ইলেকট্রন বিন্যাস (1s2 2s2 2p6)-এ সর্ববহিঃস্থ স্তরে ইলেকট্রন দ্বারা অষ্টক পূর্ণ থাকে, যা অত্যন্ত সুস্থিত। এ' সুস্থিত ইলেকট্রন বিন্যাস ভাঙতে অনেক শক্তির প্রয়োজন। তাই Ne স্বাভাবিক অবস্থায় কোনো মৌলের সাথে যুক্ত হয় না। অর্থাৎ বহিঃস্প স্তরের সুবিন্যস্ত ইলেকট্রন বিন্যাসের কারণে Ne নিষ্ক্রিয় হয়।
হিলিয়াম একটি নিষ্ক্রিয় গ্যাস। কারণ হিলিয়ামের ইলেকট্রন বিন্যাস He (2) = 1s2 অর্থাৎ ইলেকট্রন বিন্যাসে Is অরবিটাল ইলেকট্রন দ্বারা পূর্ণ থাকে। ১ম পর্যায়ের ক্ষেত্রে অন্য কোনো অরবিটাল না থাকায় এবং ও অরবিটাল ইলেকট্রন দ্বারা পূর্ণ থাকায় হিলিয়াম মৌলটি অন্য কোনো মৌল এমনকি আরেকটি হিলিয়ামের সাথে যুক্ত হতে পারে না। ইলেকট্রন দান বা গ্রহণ এবং শেয়ারের মাধ্যমে যৌগ গঠন করতে পারে না বলে এটি নিষ্ক্রিয় গ্যাস।
পর্যায় সারণিতে গ্রুপ-3 থেকে গ্রুপ-।। পর্যন্ত অবস্থিত মৌলসমূহকে অবস্থান্তর মৌল বলে। অন্যভাবে বলা যায়, যেসব d ব্লকভুক্ত মৌলের সর্বশেষ স্তরের এ অরবিটাল ইলেকট্রন দ্বারা আংশিকভাবে (d1-9) পূর্ণ থাকে তাদেরকে অবস্থান্তর মৌল বলে। অবস্থান্তর মৌলসমূহের নিজস্ব বর্ণ আছে, এরা পরিবর্তনশীল যোজনী প্রদর্শন করে এবং প্রভাবক হিসাবে কাজ করতে পারে।
Zn অবস্থান্তর মৌল নয়। কারণ জানা আছে, যে সকল এ-ব্লক মৌলের স্থায়ী আয়নে d-অরবিটালের ইলেকট্রন বিন্যাস d1-9হয় তাদেরকে অবস্থান্তর মৌল বলা হয়। এক্ষেত্রে Zn এর স্থায়ী আয়ন Zn2+ এর ইলেকট্রন বিন্যাস হলো Zn2+ (30) = 1s2 2s2 2p6 3s2 3p6 3d10 4s°
যেহেতু d অরবিটালের ইলেকট্রন বিন্যাস d1-9 নয় তাই Zn কে অবস্থান্তর মৌল বলা হয় না।
Cu অবস্থান্তর মৌল। কারণ জানা আছে, যেসব ধাতব মৌলের সুস্থিত আয়নের -অরবিটাল আংশিকভাবে ইলেকট্রন দ্বারা পূর্ণ থাকে, সেগুলোকে অবস্থান্তর মৌল বলা হয়। Cu এর ইলেকট্রন বিন্যাস নিম্নরূপ-
Cu এর সুস্থিত আয়নের ইলেকট্রন বিন্যাস লক্ষ করলে দেখা যায় d-অরবিটাল আংশিকভাবে পূর্ণ রয়েছে। তাই Cu কে অবস্থান্তর মৌল বলা হয়।
F2ও Cl2 একই ধরনের বিক্রিয়া প্রদর্শন করে। কারণ মৌল দুটি একই গ্রুপ-17 এর অন্তর্ভুক্ত। এ গ্রুপের মৌলগুলো হ্যালোজেন নামে পরিচিত। এরা ধাতুর সাথে যুক্ত হয়ে ধাতুর হ্যালাইড (NaF, NaCl ) গঠন করে। যেমন,
আবার হাইড্রোজেন (H2) এর সাথে যুক্ত হয়ে হাইড্রাসিড গঠন করে।
সুতরাং F2 ও Cl2একই ধরনের বিক্রিয়া প্রদর্শন করে।
2016 সাল পর্যন্ত পৃথিবীতে মোট 118টি মৌলিক পদার্থ আবিষ্কৃত হয়েছে। রসায়ন অধ্যয়ন ও গবেষণার জন্য সব কয়টি মৌলের ভৌত ও রাসায়নিক ধর্ম সম্পর্কে ধারণা থাকা প্রয়োজন। মৌলিক পদার্থগুলোর মধ্যে কিছু মৌলিক পদার্থ একই রকম ধর্ম প্রদর্শন করে। যে সকল মৌলিক পদার্থ একই রকম ধর্ম প্রদর্শন করে তাদেরকে একই গ্রুপে রেখে সমগ্র মৌলিক পদার্থের জন্য একটি ছক তৈরি করার চেষ্টা দীর্ঘদিন থেকেই চলছিল। কয়েক শত বছর ধরে বিভিন্ন বিজ্ঞানীর প্রচেষ্টা, অনেক পরিবর্তন, পরিবর্ধনের ফলে আমরা মৌলগুলো সাজানোর এই ছকটি পেয়েছি, যেটা পর্যায় সারণি বা Periodic table নামে পরিচিত। এ পর্যায় সারণি রসায়নের জগতে বিজ্ঞানীদের এক অসামান্য অবদান। এ পর্যায় সারণি এবং তার বৈশিষ্ট্য সম্পর্কে কারও ভালো ধারণা থাকলে শুধু এই 118টি মৌলের বিভিন্ন ধর্ম নয় বরং এ সকল মৌল দ্বারা গঠিত অসংখ্য যৌগের ধর্মাবলি সম্পর্কে সাধারণ ধারণা জন্মে। এই অধ্যায়ে পর্যায় সারণি এবং পর্যায় সারণিতে অবস্থিত মৌলসমূহের বিভিন্ন ধর্ম ও বৈশিষ্ট্য সম্পর্কে একটি সাধারণ ধারণা দেওয়ার চেষ্টা করা হয়েছে।
এ অধ্যায় পাঠ শেষে আমরা -
- পর্যায় সারণি বিকাশের পটভূমি বর্ণনা করতে পারব।
- মৌলের সর্ববহিঃস্তর শক্তিস্তরের ইলেকট্রন বিন্যাসের সাথে পর্যায় সারণির প্রধান গ্রুপগুলোর সম্পর্ক নির্ণয় করতে পারব (প্রথম 30টি মৌল)।
- একটি মৌলের পর্যায় শনার করতে পারব।
- পর্যায় সারণিতে কোনো মৌলের অবস্থান জেনে এর ভৌত ও রাসায়নিক ধর্ম সম্পর্কে ধারণা করতে পারব।
- মৌলসমূহের বিশেষ নামকরণের কারণ বলতে পারব।
- পর্যায় সারণির গুরুত্ব ব্যাখ্যা করতে পারব।
- পর্যায় সারণির একই গ্রুপের মৌল দ্বারা গঠিত যৌগের একই ধরনের ধর্ম প্রদর্শন করতে গাঁৱৰ ।
- পরীক্ষণের সময় কাচের যন্ত্রপাতির সঠিক ব্যবহার করতে পারব।
- পরীক্ষণ কাজে সতর্কতা অবলম্বন করতে পারব।
- পর্যায় সারণি অনুসরণ করে মৌলসমূহের ধর্ম অনুমানে আগ্রহ প্রদর্শন করতে পারব।
Related Question
View Allরাসায়নিকভাবে সদৃশ প্রতি ৩টি মৌলের মধ্যে মাঝের মৌলটির পারমাণবিক ভর মোটামুটিভাবে অপর মৌল দুটির পারমাণবিক ভরের গড় হয়- এটিই ডোবেরাইনার ত্রয়ী সূত্র।
বেরিয়াম (Ba) মৌলটি গ্রুপ-২ এ অবস্থিত। এর অক্সাইড পানিতে ক্ষারীয় দ্রবণ তৈরি করে। এর সর্ববহিঃস্ত স্তরের দুটি ইলেকট্রন অধাতুকে দান করে আয়নিক যৌগ (লবণ) তৈরি করে। এটি বিভিন্ন যৌগ হিসেবে মাটিতে থাকে। তাই বেরিয়াম (Ba) কে মৃৎক্ষার ধাতু বলা হয়।
ক্ষার
প্রদত্ত উদ্দীপকে সোডিয়াম (Na), ম্যাগনেসিয়াম (Mg), ফ্লোরিন (চ), ক্লোরিন (CI) এবং ব্রোমিন (Br) এই পাঁচটি মৌল অবস্থিত। এদের মধ্য Na, Mg ও CI মৌলত্রয় পর্যায় সারণির তৃতীয় পর্যায়ে এবং F, CI ও Br মৌলত্রয় পর্যায় সারণির 17 নং গ্রুপে অবস্থিত।
আমরা জানি, পর্যায় সারণির যে কোনো পর্যায়ে যতই বামদিক থেকে ডানদিকে যাওয়া যায় অর্থাৎ পারমাণবিক সংখ্যা যতই বাড়ে পরমাণুর আকার ততই হ্রাস পায়। অতএব উদ্দীপকের Na, Mg ও CI এর মধ্যে Na এর আকার সবচেয়ে বড় এবং CI এর আকার সবচেয়ে ছোট। এদের আকারের ক্রম হলো Na > Mg > Cl । Na এর পারমাণবিক ব্যাসার্ধ 0.154 nm এবং CI এর পারমাণবিক ব্যাসার্ধ 0.099 nm।
আবার একই গ্রুপের মৌলসমূহের বেলায় উপর থেকে নিচের দিকে গেলে পরমাণুর ইলেকট্রনের জন্য নতুন কক্ষপথ বা শক্তিস্তর যুক্ত হয়।
ফলে পারমাণবিক ব্যাসার্ধ বৃদ্ধি পায়। F, CI ও Br মৌলগুলোর মধ্যে F একই গ্রুপের সবচেয়ে উপরে এবং Br সবচেয়ে নিচে অবস্থিত। অতএব, এদের আকারের ক্রম হলো F < Cl < Br Br এর পারমাণবিক ব্যাসার্ধ হলো 0.144nm |
উপরোক্ত আলোচনা হতে দেখা যায়, Na ও Br উভয়ের আকারই CI থেকে বড়। অর্থাৎ এদের ক্রম হলো- Na > Cl < Br কিন্তু Na ও Br এর পারমাণবিক ব্যাসার্ধ যথাক্রমে 0.154 nm ও 0.114 nm । সুতরাং উদ্দীপকের মৌলগুলোর মধে Na এর আকার সবচেয়ে বড়।
গ্যাসীয় অবস্থায় কোনো মৌলের এক মোল গ্যাসীয় পরমাণুতে এক মোল ইলেকট্রন প্রবেশ করিয়ে এক মোল ঋণাত্মক আয়নে পরিণত করতে যে পরিমাণ শক্তি নির্গত হয় তাকে ঐ মৌলের ইলেকট্রন আসক্তি বলে।
উদ্দীপকের পর্যায়ের মৌলগুলো যথাক্রমে Na, Mg ও Cl
পর্যায় সারণির একই পর্যায়ে মৌলগুলোর জন্য বাম দিক থেকে ডান দিকে ইলেকট্রন আসক্তি ক্রমশ বৃদ্ধি পায়। কারণ বাম থেকে ডান দিকে পারমাণবিক সংখ্যা। ক্রমশ বৃদ্ধি পায়। ফলে নিউক্লিয়াসের প্রোটনের সংখ্যা বৃদ্ধি তথা ধনাত্মক চার্জ বৃদ্ধি পায় কিন্তু নতুন কোনো শক্তিস্তর সৃষ্টি না হওয়ায় নিউক্লিয়াস থেকে ইলেকট্রনের দূরত্ব তেমন বৃদ্ধি পায় না। ফলে ধনাত্মক চার্জের ঘনত্ব বৃদ্ধি পায়। তাই অধিক আকর্ষণের জন্য মৌলগুলোের ইলেকট্রন আসক্তি বৃদ্ধি পায়।
এক্ষেত্রে উদ্দীপকের পর্যায়ের সর্ববামের মৌল Na এর আকার সবচেয়ে বড় এবং সর্বডানের মৌল Cl এর আকার সবচেয়ে ছোট। অতএব এ পর্যায়ের মৌলের আকারের ক্রম হলো Na > Mg > ........>Cl আবার, আমরা জানি মৌলের পারমাণবিক ব্যাসার্ধ অর্থাৎ আকার বৃদ্ধি পেলে ইলেকট্রন আসক্তি হ্রাস পায় এবং আকার হ্রাস পেলে ইলেকট্রন আসক্তি বৃদ্ধি পায়। সুতরাং উদ্দীপকের পর্যায়ের মৌলগুলোের ইলেকট্রন আসক্তির ক্রম হবে Na < Mg<..........
মৌলসমূহের ভৌত ও রাসায়নিক ধর্মাবলি তাদের পারমাণবিক সংখ্যা অনুযায়ী পর্যায়ক্রমে আবর্তিত হয়।
উদ্দীপকের B মৌলটি পর্যায় সারণির চতুর্থ পর্যায়ের গ্রুপ-২ এ অবস্থিত। কাজেই মৌলটি হতে ক্যালসিয়াম (Ca)।
যে সকল ধাতু মাটিতে যৌগ হিসেবে পাওয়া যায় এবং পানির সাথে বিক্রিয়া করে ক্ষার তৈরি করে তাদেরকে মৃৎক্ষার ধাতু বলা হয়। বৈশিষ্ট্য অনুসারে গ্রুপ-2 এর মৌলসমূহকে মৃৎক্ষার ধাতু বলে। ক্যালসিয়াম (Ca) পর্যায় সারণির দ্বিতীয় গ্রুপে অবস্থিত একটি মৌল। মৌলটি মূলত মাটিতে পাওয়া যায় এবং পানির সাথে বিক্রিয়া করে Ca(OH)2 গঠন করে। তাই ক্যালসিয়াম (Ca) কে মৃৎক্ষার ধাতু বলা হয়।
১ ক্লিকে প্রশ্ন, শীট, সাজেশন ও
অনলাইন পরীক্ষা তৈরির সফটওয়্যার!
শুধু প্রশ্ন সিলেক্ট করুন — প্রশ্নপত্র অটোমেটিক তৈরি!



