সোনা মৌলিক পদার্থ।
যে পদার্থকে ভাঙলে সেই পদার্থ ছাড়া অন্য কোনো পদার্থ পাওয়া যায় না মৌলিক পদার্থ বলে।
প্রতিটি পদার্থ অসংখ্য ক্ষুদ্র এবং অবিভাজ্য কণার সমন্বয়ে গঠিত' এটি বিজ্ঞানী জন ডাল্টন এর মতবাদ ।
দার্শনিক ডেমোক্রিটাস গ্রিস এর দার্শনিক ছিলেন।
সর্বপ্রথম 'এটম' নামকরণ করেন দার্শনিক ডেমোক্রিটাস।
এ পর্যন্ত 118 টি মৌল আবিষ্কৃত হয়েছে ।
প্রকৃতিতে প্রাপ্ত মৌলের সংখ্যা 98 টি।
আমাদের শরীরে মোট 26 ধরনের মৌল রয়েছে ।
গবেষণাগারে আবিষ্কৃত মৌলের সংখ্যা 20টি।
গবেষণাগারে আবিষ্কৃত মৌলকে কৃত্রিম মৌল বলে ।
রাসায়নিক বিশ্লেষণের মাধ্যমে পানিকে ভাঙা হয়।
পানিকে বিশ্লেষণ করলে হাইড্রোজেন ও অক্সিজেন মৌল পাওয়া যায় ।
যে পদার্থকে ভাঙলে দুই বা ততোধিক মৌল পাওয়া যায় তাকে যৌগিক পদার্থ বলে।
যৌগের মধ্যে মৌলসমূহের সংখ্যার অনুপাত একই।
পানিতে হাইড্রোজেন ও অক্সিজেনের পরমাণুর সংখ্যার অনুপাত 2:1 ।
পানি সাধারণ তাপমাত্রায় তরল অবস্থায় থাকে।
ক্যালসিয়াম, কার্বন ও অক্সিজেনের সমন্বয় গঠিত যৌগ CaCO3বা চক ।
চক যৌগিক পদার্থ।
নাইট্রোজেন, ফসফরাস মৌলিক পদার্থ।
বরফ যৌগিক পদার্থ।
লোহাকে ভাঙলে লোহা (Fe) পদার্থের পরমাণু পাওয়া যাবে ।
পানির গঠনকারী মৌলসমূহ সাধারণ তাপমাত্রায় গ্যাসীয় অবস্থায় থাকে।
পানির ভাঙনকে রাসায়নিক বিশ্লেষণ বুঝায় ।
মৌলিক পদার্থের ক্ষুদ্রতম কণাকে পরমাণু বলে।
নাইট্রোজেন পরমাণুতে নাইট্রোজেন মৌলের ধর্ম বিদ্যমান ।
অক্সিজেন অণুর সংকেত O2।
অণুর ক্ষুদ্রতম কণাকে পরমাণু বলে।
মৌলিক বা যৌগিক পদার্থের ক্ষুদ্রতম কণাকে অণু বলে।
রাসায়নিক বিক্রিয়ায় অংশগ্রহণের পূর্বে পরমাণুতে বিশিষ্ট হয়।
পৃথিবীতে অণুর সংখ্যা অসংখ্য।
মৌলিক পদার্থের ক্ষুদ্রতম কণাকে পরমাণু বলে।
নিষ্ক্রিয় গ্যাসের পরমাণু স্বাধীনভাবে থাকতে পারে।
কার্বন ডাই অক্সাইড অণুর সংকেত CO2
ভিন্ন ভিন্ন মৌলের পরমাণু পরস্পর যুক্ত হলে তাকে যৌগিক অণু বলে।
একই মৌলের পরমাণু পরস্পর যুক্ত হলে তাকে মৌলের অণু বলে।
O2 মৌলের অণু ।
NO2 যৌগিক অণু ।
নাইট্রোজেন পরমাণুর স্থায়িত্ব অস্থায়ী।
CO2 অণুর স্থায়িত্ব স্থায়ী।
হাইড্রোজেনের প্রতীক H ।
মৌলের ইংরেজি বা ল্যাটিন নামের সংক্ষিপ্ত রূপকে প্রতীক বলে।
ক্যালসিয়ামের প্রতীক Ca
ক্যাডমিয়ামের প্রতীক Cd ।
কপারের ল্যাটিন নাম Cuprum ।
সিলভারের ল্যাটিন নাম Argentum ।
এন্টিমনির ল্যাটিন নাম Stibium ।
গোল্ডের ল্যাটিন নাম ও প্রতীক Aurum (Au)।
মারকারির ল্যাটিন নাম ও প্রতীক Hydrugyrum (Hg)।
টাংস্টেনের প্রতীক (W) মৌলের ল্যাটিন নাম থেকে নেয়া হয়েছে।
কোবাল্টের প্রতীক (Co) মৌলের ইংরেজি নাম থেকে নেয়া হয়েছে।
প্রকৃতিতে প্রাপ্ত সব মৌলিক পদার্থের প্রতীক এক বা দুই অক্ষরের হয় ।
সোডিয়ামের প্রতীক ও ল্যাটিন নাম প্রতীক Na, ল্যাটিন নাম Natrium।
পানির সংকেত H2O ।
রাসায়নিক সংকেত রাসায়নিক উপাদানসমূহের আনুপাতিক তথ্য প্রকাশ করে।
রাসায়নিক সংকেত রাসায়নিক গঠন প্রকাশ করা হয় ।
অ্যামোনিয়ার সংকেত NH3 ।
সালফিউরিক এসিডের সংকেত H2SO4 ।
পরমাণু ইলেকট্রন, প্রোটন ও নিউট্রন দিয়ে তৈরি ।
পরমাণুর স্থায়ী কণিকা ৩টি।
পরমাণুর কেন্দ্রকে নিউক্লিয়াস বলে।
পরমাণুর ইলেকট্রন কণিকা নিউক্লিয়াসকে ঘিরে ঘুরতে থাকে ।
পরমাণুর কেন্দ্রে প্রোটন ও নিউট্রন কণিকা থাকে ।
পরমাণুর ঋণাত্মক চার্জযুক্ত কণিকা ইলেকট্রন।
ইলেকট্রনের আধান
একটি ইলেকট্রনের প্রকৃত ভর
ইলেকট্রনের আপেক্ষিক আধান -1 ধরা হয়।
প্রোটন ও নিউট্রনের তুলনায় ইলেকট্রন ভর 1840 গুণ কম।
ইলেকট্রনের আপেক্ষিক ভর শূন্য ।
পরমাণুর ধনাত্মক চার্জযুক্ত কণিকা প্রোটন।
প্রোটনের আধান কুলম্ব।
একটি প্রোটনের প্রকৃত ভর
প্রোটনের আপেক্ষিক ভর 1
পরমাণুতে প্রোটনের অবস্থান নিউক্লিয়াসে।
পরমাণুর চার্জ নিরপেক্ষ কণিকা নিউট্রন।
হাইড্রোজেন মৌলের পরমাণুতে নিউট্রন নেই।
আধান নিরপেক্ষ কণিকার প্রকৃত ভর
প্রোটনের সংকেত H
পরমাণুর প্রোটন ও নিউট্রন কণিকার আপেক্ষিক ভর সমান ।
পরমাণুর ইলেকট্রনের অবস্থান কক্ষপথে ।
পরমাণুর প্রোটন সংখ্যাকে পারমাণবিক সংখ্যা বলে।
প্রত্যেক পরমাণুর চার্জ চার্জ নিরপেক্ষ।
কোনো পরমাণুর প্রোটন ও নিউট্রনের মোট সংখ্যাকে ভর সংখ্যা বলে ।
সোডিয়ামের ভর সংখ্যা 23।
সোডিয়ামের প্রোটন সংখ্যা 11 ।
ভর সংখ্যাকে A দিয়ে প্রকাশ করা হয়।
আর্গনের পারমাণবিক সংখ্যা 18 ।
সংকেতটিতে নিউট্রন সংখ্যা 20 ।
প্রতীকটিতে এ দ্বারা ভর সংখ্যা বুঝায় ।
প্রতীকটিতে নিউট্রন সংখ্যা A-Z ।
Al এর Z = 13 এবং A = 27 হলে নিউট্রন সংখ্যা 14 ।
একটি মৌলের পরমাণুর প্রতীক C (কার্বন) যার ইলেকট্রন প্রোটন, নিউট্রন সংখ্যা সমান ।
পরমাণুর ভর সংখ্যাকে নিউক্লিয়ন সংখ্যা বলা যায় ।
নিরপেক্ষ পরমাণুর ইলেকট্রন ও প্রোটন কণিকার সংখ্যা সমান ।
পরমাণুর ভেতরে বেশিরভাগ জায়গাই ফাঁকা
কোনো পরমাণুর পারমাণবিক সংখ্যা 9 হলে পরমাণুটি ফ্লোরিন (F)।
পরমাণুর প্রোটন ও ইলেকট্রন সংখ্যা সমান হলে পরমাণু চার্জ শূন্য।
রাদারফোর্ড 1911 সালে পরমাণুর মডেল প্রদান করেন ।
প্রোটন ও নিউট্রন পরমাণুর ভরকে পরমাণুর ভর হিসেবে বিবেচনা হয়।
সামগ্রিকভাবে পরমাণুর চার্জ শূন্য।
পরমাণুর নিউক্লিয়াসের প্রতি ইলেকট্রন কেন্দ্রমুখী আকর্ষণ বল অনুভব করে।
সোলার সিস্টেম এটম মডেল বিজ্ঞানী রাদারফোর্ড প্রদান করেন ।
সর্বপ্রথম নিউক্লিয়াস সম্পর্কে ধারণা দেন বিজ্ঞানী রাদারফোর্ড।
রাদারফোর্ডের পরমাণু মডেল সর্বপ্রথম নিউক্লিয়াস সম্পর্কে ধারণা দেয়া হয়।
ম্যাক্সওয়েলের তত্ত্বানুসারে রাদারফোর্ডের মডেলের ইলেকট্রন নিউক্লিয়াসে পতিত হবে।
রাদারফোর্ডের পরমাণু মডেল একটি ইলেকট্রন বিশিষ্ট পরমাণুর ক্ষেত্রে প্রযোজ্য।
রাদারফোর্ডের পরমাণু মডেলের ত্রুটিগুলো সংশোধন করেন বিজ্ঞানী নীলস্ বোর ।
বিজ্ঞানী ম্যাক্সওয়েল এর তত্ত্বানুসারে রাদারফোর্ডের পরমাণু মডেল সঠিক নয়।
অনুমোদিত কক্ষপথ বা অরবিট সম্পর্কে ধারণা দেন বিজ্ঞানী নীলস্ বোর।
পরমাণুতে ইলেকট্রন নিউক্লিয়াস কে কেন্দ্র করে নির্দিষ্ট কক্ষপথে ক্রমাগত ঘুরছে ।
স্থির কক্ষপথকে n দ্বারা প্রকাশ করা হয়।
পরমাণুর প্রায় সমস্ত ভর নিউক্লিয়াসে কেন্দ্রীভূত থাকে ।
পরমাণুতে নিউক্লিয়াস ও ইলেকট্রনের মধ্যে বিরাজমান দুই প্রকার বলের মান পরস্পর সমান ও বিপরীতমুখী।
চার্জযুক্ত কণার বৃত্তাকার পথে আবর্তন ও ক্রমাগত শক্তি বিকিরণের ধারণা প্রবর্তন করেন ম্যাক্সওয়েল।
1913 সালে বিজ্ঞানী নীলস বোর তার বিখ্যাত পরমাণু মডেল প্রদান করেন।
বোর মডেল অনুসারে শক্তিস্তরে ইলেকট্রনের কৌণিক ভরবেগ নির্ণয়ের সমীকরণ ।
প্ল্যাংক ধ্রুবক h এর মান
ইলেকট্রন নিম্ন শক্তিস্তর থেকে উচ্চ শক্তিস্তরে যাওয়ার সময় শক্তি শোষণ ঘটবে।
আলোর বেগ
শোষিত বা বিকিরিত শক্তির কম্পাঙ্কের একক S-1 বা HZ (হার্জ)
শোষিত বা বিকিরিত শক্তির তরঙ্গ দৈর্ঘ্যের একক m (মিটার)।
শক্তিস্তরের আকার বৃত্তাকার।
বৃত্তাকার শক্তিস্তরের ধারণা দেন নীলস্ বোর।
পরমাণুতে ইলেকট্রনের শোষিত বা বিকিরিত শক্তির পরিমাণ নির্ণয়ের সমীকরণ ।
প্রতিটি প্রধান শক্তিস্তরে সর্বোচ্চ ইলেকট্রন ধারণ ক্ষমতা 2n2
সোডিয়ামের M শেলে 1 টি ইলেকট্রন বিদ্যমান ।
সিলিকনের L শেলে ৪ টি ইলেকট্রন বিদ্যমান।
পরমাণুর ৩য় শক্তিস্তর (M) এর সর্বোচ্চ ইলেকট্রন ধারণ ক্ষমতা 18 টি।
পরমাণুর ৪র্থ শক্তিস্তর (N) এর সর্বোচ্চ ইলেকট্রন ধারণ ক্ষমতা ৩২ টি।
অ্যালুমিনিয়ামে M শেলে 3টি ইলেকট্রন বিদ্যমান।
পরমাণুর উপশক্তিস্তরগুলোকে অরবিটাল বলা হয়।
উপশক্তিস্তরকে/ দ্বারা চিহ্নিত করা হয়।
n = 3 হলে উপশক্তিস্তর 3 টি।
n = 4./= 1 হলে অরবিটাল 4f হবে।
পরমাণুর p উপস্তরে সর্বোচ্চ ইলেকট্রন ধারণ ক্ষমতা 6 টি।
পরমাণুর K শেলের উপস্তর সংখ্যা 1 টি।
পরমাণুর N শেলে সর্বোচ্চ 32 টি ইলেকট্রন থাকতে পারে ।
সোডিয়াম পরমাণুর ইলেকট্রন 3টি স্তরে বিন্যস্ত ।
প্রতিটি অরবিটালে ইলেকট্রন সংখ্যা 2(2/+1)।
ক্লোরিন মৌলের M শেলে ইলেকট্রন সংখ্যা 7টি।
পটাসিয়ামের সর্বশেষ ইলেকট্রনটি 4 s উপস্তরে প্রবেশ করে।
অরবিটালগুলোর অর্থপূর্ণ বা সম্পূর্ণভাবে অবস্থায় পরমাণুর ইলেকট্রন বিন্যাস সুস্থিত হয় ।
ক্রোমিয়ামের 3d অরবিটালটি অর্ধপূর্ণ হওয়ায় ইলেকট্রন বিন্যাস সুস্থিত ।
স্ক্যান্ডিয়ামের 21 তম ইলেকট্রনটি 3d অরবিটালে প্রবেশ করে ।
আয়রন পরমাণুতে প্রোটন সংখ্যা 26।
অরবিটালের শক্তির ক্রম (n+I) মানের উপর নির্ভর করে ।
আইসোটোপ পরমাণুসমূহের প্রোটন কণার সংখ্যা সমান।
হাইড্রোজেনের 7টি আইসোটোপ রয়েছে ।
প্রকৃতিতে প্রাপ্ত হাইড্রোজেন আইসোটোপের সংখ্যা 3 টি।
প্রোটিয়ামের প্রতীক
প্রতীককে ডিউটেরিয়াম বলা হয় ।
প্রতীককে কী বলা হয় টিট্রিয়াম।
দুটি আইসোটোপের ক্ষেত্রে অসমান ভরসংখ্যা।
ট্রিটিয়ামের ভরসংখ্যা 3 ।
বিভিন্ন ভরসংখ্যাবিশিষ্ট একই মৌলের পরমাণুকে পরস্পরের আইসোটোপ বলা হয়।
এবং হাইড্রোজেন মৌলের আইসোটোপ।
হাইড্রোজেনের আইসোটোপগুলোর মধ্যে ল্যাবরেটরিতে প্রস্তুত করা হয় 4 টি।
প্রোটন সংখ্যা
কার্বন 12 আইসোটোপের পারমাণবিক ভরের অংশের ভর
কপারের পারমাণবিক ভর 63.5
ক্লোরিনের পারমাণবিক ভর 35.5 ।
ফ্লোরিনের একটি পরমাণুর ভর
অ্যালুমিনিয়ামের একটি পরমাণুর ভর ।
আপেক্ষিক পারমাণবিক ভর নির্ণয়ে কার্বন 12 আইসোটোপ মৌলের পরমাণুর পারমাণবিক ভরের সাথে তুলনা করা হয়।
কোনো মৌলের আপেক্ষিক পারমাণবিক ভর নির্ণয়ে পরমাণুর প্রকৃত ভর জানা অপরিহার্য।
আপেক্ষিক পারমাণবিক ভরের একক নেই।
আপেক্ষিক পারমাণবিক ভর মূলত দুটি ভরের অনুপাত।
হাইড্রোজেনের আপেক্ষিক পারমাণবিক ভর 1.008
অ্যালুমিনিয়াম মৌলের আপেক্ষিক পারমাণবিক ভর 27 ।
প্রকৃতিতে ক্লোরিনের ২টি আইসোটোপ আছে ।
প্রকৃতিতে প্রাপ্ত ক্লোরিনের দুটি আইসোটোপের প্রতীক ।
প্রকৃতিতে প্রাপ্ত এর শতকরা পরিমাণ 75% ।
প্রকৃতিতে কপারের আইসোটোপ আছে।
প্রকৃতিতে প্রাপ্ত কপারের দুটি আইসোটোপের প্রতীক
আপেক্ষিক আণবিক ভরকে সাধারণভাবে আণবিক ভর হিসেবে বিবেচনা করা হয়।
H2SO4এর আপেক্ষিক আণবিক ভর 98 ।
সালফার পরমাণুর আপেক্ষিক পারমাণবিক ভর 32 ।
অক্সিজেন পরমাণুর আপেক্ষিক পারমাণবিক ভর 16 ।
H2SO4 অণুতে মোট পরমাণুর সংখ্যা 7 টি।
O2 এর আপেক্ষিক আণবিক ভর 32 ।
যেসব আইসোটোপ হতে আলফা, বিটা, গামা রশ্মি নির্গত হয় তাদের তেজস্ক্রিয় আইসোটোপ বলে।
এখন পর্যন্ত 3000 এর অধিক সংখ্যক আইসোটোপ সম্বন্ধে জানা গেছে।
রোগাক্রান্ত স্থানের ছবি তুলতে টেকনিশিয়াম আইসোটোপ ব্যবহার করা হয় ।
তেজস্ক্রিয় আইসোটোপ টেকনিশিয়াম 99 এর লাইফটাইম 6 ঘণ্টা।
রোগাক্রান্ত স্থানের ছবি তুলতে Tc আইসোটোপ গামা রশ্মি নির্গত করে।
সর্বপ্রথম থাইরয়েড ক্যান্সার নিরাময়ে তেজস্ক্রিয় আইসোটোপ ব্যবহার করা হয় ।
থাইরয়েড ক্যান্সার নিরাময়ে রোগীকে আইসোটোপ সমৃদ্ধ দ্রবণ পান করানো হয় ।
থাইরয়েড ক্যান্সার নিরাময়ে ব্যবহৃত থেকে বিটা রশ্মি নির্গত হয় ।
ব্রেইন ক্যান্সার নিরাময়ে ইরিডিয়াম আইসোটোপ ব্যবহার করা হয়।
টিউমারের উপস্থিতি নির্ণয় ও নিরাময়ে আইসোটোপ ব্যবহার করা হয় ।
ক্যান্সারের কোষ কলাকে ধ্বংস করতে থেকে গামা রশ্মি নির্গত হয়।
রক্তের লিউকোমিয়া রোগের চিকিৎসায় আইসোটোপ ব্যবহার করা হয় এর সালফেট।
প্রয়োজনের অতিরিক্ত সার প্রয়োগের ক্ষতিকর দিক পরিবেশ দূষণ ।
তেজস্ক্রিয় আইসোটোপ ব্যবহার করে জমিতে নাইট্রোজেন ও ফসফরাস মৌলের উপস্থিতি জানা যায়।
উদ্ভিদ তেজস্ক্রিয় নাইট্রোজেন ও ফসফরাস মূল অঙ্গের মাধ্যমে গ্রহণ করে ।
গাইগার মুলার কাউন্টার যন্ত্র ব্যবহার করে উদ্ভিদে তেজস্ক্রিয় রশ্মি শনাক্ত ও পরিমাপ করা হয়।
ফসিল মমির বয়স নির্ধারণে C-14 আইসোটোপ ব্যবহার করা হয়।
ফলমূলের ব্যাকটেরিয়া ধ্বংসে আইসোটোপ নির্গত গামা রশ্মি ব্যবহৃত হয় ।
উন্নতমানের ফসল পেতে তেজস্ক্রিয় রশ্মি দ্বারা উদ্ভিদের কোষের জিনগত পরিবর্তন ঘটানো হয়।
1986 সালে রাশিয়ার চেরোনোবিলে পারমাণবিক বিদ্যুৎকেন্দ্র দুর্ঘটনা ঘটেছিল।
বাংলাদেশ সরকার পাবনা জেলার রূপপুরে পারমাণবিক বিদ্যুৎকেন্দ্র স্থাপন করছে
পাবনা জেলার পারমাণবিক বিদ্যুৎকেন্দ্র হতে দুই হাজার চারশত মেগাওয়াট বিদ্যুৎ উৎপাদনের আশা করা হচ্ছে ।
২য় বিশ্বযুদ্ধে জাপানের হিরোশিমা ও নাগাসাকিতে পারমাণবিক বোমার বিস্ফোরণ ঘটেছিল।
যে পদার্থকে ভাঙলে ঐ পদার্থ ছাড়া অন্য কোনো পদার্থ পাওয়া যায় না, তাকে মৌলিক পদার্থ বা মৌল বলে। এ মৌলিক পদার্থের উদাহরণসমূহ হচ্ছে: নাইট্রোজেন (N), ফসফরাস (P), কার্বন (C), অক্সিজেন (০), হিলিয়াম (He), ক্যালসিয়াম (Ca), আর্গন (Ar), সালফার (S) ইত্যাদি। এ পর্যন্ত 11৪টি মৌল আবিষ্কৃত হয়েছে।
যে সকল পদার্থকে ভাঙলে বা রাসায়নিকভাবে বিশ্লেষণ করলে দুই বা ততোধিক মৌল পাওয়া যায় তাদেরকে যৌগিক পদার্থ বলে।
উদাহরণস্বরূপ: লেখার চক (CaCO3) কে রাসায়নিকভাবে বিশ্লেষণ করলে ক্যালসিয়াম (Ca), কার্বন (C) ও অক্সিজেন (০) ইত্যাদি একাধিক মৌলিক পদার্থ যায়। এক্ষেত্রে CaCO3হচ্ছে তাই যৌগিক পদার্থ।
দুই বা দুইয়ের অধিক সংখ্যক পরমাণু পরস্পরের সাথে রাসায়নিক বন্ধন এর মাধ্যমে যুক্ত থাকলে তাকে অণু বলে। অন্যদিকে, পরমাণুর সংজ্ঞা: পরমাণু হলো মৌলিক পদার্থের ক্ষুদ্রতম কণা, যার মধ্যে মৌলের গুণাগুণ বিদ্যমান।
অণু ও পরমাণুর মধ্যে দুইটি পার্থক্য নিম্নরূপ
| অণু | পরমাণু |
| ১. মৌলিক ও যৌগিক পদার্থের বৈশিষ্ট্য রক্ষাকারী ক্ষুদ্রতম কণা। | ১. কেবলমাত্র মৌলিক পদার্থের বৈশিষ্ট্য রক্ষাকারী ক্ষুদ্রতম কণা। |
| ২. অণু রাসায়নিক বিক্রিয়ায় সরাসরি অংশগ্রহণ করতে পারে না। | ২. পরমাণু সরাসরি রাসায়নিক বিক্রিয়ায় অংশগ্রহণ করতে পারে। |
মৌলিক অণু একই মৌলের একাধিক পরমাণু পরস্পরের সাথে যুক্ত হলে তাকে মৌলিক অণু বলে। যেমন- N2, H2, O2 ইত্যাদি মৌলিক অণুর প্রত্যেকেই একই মৌলের একাধিক পরমাণুর সমন্বয়ে গঠিত।
যৌগিক অণু: ভিন্ন ভিন্ন মৌলের পরমাণু পরস্পর যুক্ত হলে তাকে যৌগিক অণু বলে। যেমন, CO2, NH3, H2O ইত্যাদি যৌগিক অণুর প্রত্যেকেই ভিন্ন মৌলের একাধিক পরমাণুর সমন্বয়ে গঠিত।
সালফার (S) হলো 16 পারমাণবিক সংখ্যাবিশিষ্ট একটি মৌল। এটি পর্যায়সারণির ৩য় পর্যায়ের গ্রুপ 16 এর মৌল। ১ হলো একটি পরমাণু। অপরদিকে, আটটি সালফার (S) পরমাণু একত্রিত হয়ে মুকুট আকৃতির একটি সালফার অণু S8 গঠন করে। S8 এর গঠন নিম্নরূপ-

কোনো মৌলের ইংরেজি বা ল্যাটিন নামের সংক্ষিপ্ত রূপকে প্রতীক বলা হয়। যেমন ক্যালসিয়াম মৌলের ইংরেজি নাম Calcium; এর সংক্ষিপ্ত প্রকাশ অর্থাৎ প্রতীক Ca। আবার পটাশিয়াম মৌলের ল্যাটিন নাম Kalium; এর সংক্ষিপ্ত প্রকাশ; অর্থাৎ, এর প্রতীক K। কোনো মৌলের এই প্রতীকসমূহ লিখতে কিছু নিয়ম অনুসরণ করতে হয়।
প্রতীক লেখার দুইটি নিয়ম নিম্নরূপ:
১. মৌলের ইংরেজি বা ল্যাটিন নামের প্রথম অক্ষর ইংরেজি বর্ণমালার বড় হাতের অক্ষর দ্বারা প্রতীক লেখা হয়।
২. যদি দুই বা দুইয়ের অধিক মৌলের ইংরেজি বা ল্যাটিন নামের প্রথম অক্ষর একই হয়, সেক্ষেত্রে একটি মৌলকে ১ম অক্ষর ইংরেজি বর্ণমালার বড় হাতের অক্ষর দ্বারা এবং অন্যগুলোর ক্ষেত্রে দুই অক্ষর দ্বারা প্রতীক লেখা হয়।
কোনো মৌল বা যৌগের অণুর সংক্ষিপ্তরূপকে সংকেত বলা হয়। যেমন হাইড্রোজেন অণুর সংকেত H₂। এর অর্থ হলো একটি হাইড্রোজেনের অণুতে দুইটি হাইড্রোজেনের পরমানু (H) রয়েছে। আবার অ্যামোনিয়া অণুর সংকেত NH3 । এর অর্থ হচ্ছে অ্যামোনিয়ার একটি অণুতে ১টি নাইট্রোজেন (N) ও ৩টি হাইড্রোজেন (H) পরমাণু রয়েছে।
প্রতীক ও সংকেতের মধ্যে দুইটি পার্থক্য নিম্নরূপ :
| প্রতীক | সংকেত |
| ১. প্রতীক শুধু মৌলিক পদার্থের জন্য লেখা হয়। | ১. সংকেত মৌলিক ও যৌগিক উভয় পদার্থের জন্য লেখা হয়। |
| ২. প্রতীক মৌলের একটি পরমাণুকে নির্দেশ করে। | ২.সংকেত পদার্থের একটি অণুকে নির্দেশ করে। |
১টি যৌগিক অণুর এবং ১টি মৌলিক অণুর সংকেত নিম্নরূপ-
| যৌগিক অণু | সংকেত |
| সালফিউরিক এসিড | H2SO4 |
| মৌলিক অণু | সংকেত |
| ব্রোমিন | Br2 |
একমাত্র H ব্যতীত সকল পদার্থের পরমাণু যে তিনটি কণা দ্বারা গঠিত, তাকে বলা হয় পরমাণুর সাংগঠনিক (fundamental) বা মৌলিক কণা। পরমাণুর এ ৩টি সাংগঠনিক কণা হচ্ছে- ১. ইলেকট্রন, ২. প্রোটন ও ৩. নিউট্রন। পরমাণুর কেন্দ্র বা নিউক্লিয়াসে থাকে প্রোটন ও নিউট্রন এবং নিউক্লিয়াসকে ঘিরে ঘূর্ণায়মান থাকে ইলেকট্রন।
ইলেকট্রন হলো পরমাণুর একটি মূল কণিকা, যা ঋণাত্মক আধানবিশিষ্ট। এর আধানের পরিমাণ কুলম্ব, ভর এর আপেক্ষিক আধান -1 এবং আপেক্ষিক ভর ০। একে e প্রতীক দ্বারা প্রকাশ করা হয়।
প্রোটন হলো পরমাণুর একটি মূল কণিকা, যার চার্জ বা আধান ধনাত্মক। এ আধানের পরিমাণকুলম্ব। এর একটি প্রোটনের ভর । এর আপেক্ষিক আধান ও ভর যথাক্রম +1 ও 1।একে p প্রতীক দ্বারা প্রকাশ করা হয়।
পরমাণুর স্থায়ী ৩টি সাংগঠনিক কণা হচ্ছে- ইলেকট্রন, প্রোটন ও নিউট্রন।
ইলেকট্রনের প্রকৃত ভর =
প্রোটনের প্রকৃত ভর =
নিউট্রনের প্রকৃত ভর =
স্থায়ী কণিকা তিনটির আধান:
ইলেকট্রনের আধান = 1.60 10-19 কুলম্ব (C)
প্রোটনের আধান = +1.60 10-19 কুলম্ব (C)
নিউট্রনের কোনো আধান নেই।
এটি আধান নিরপেক্ষ। অর্থাৎ, নিউট্রনের আপেক্ষিক আধান '0' ধরা হয়।
নিউট্রন হলো পরমাণুর আধান নিরপেক্ষ মূল কণিকা। এর ভর প্রোটনের ভরের চেয়ে সামান্য বেশি। এর আপেক্ষিক আধান 0, আপেক্ষিক ভর।। একে প্রতীক দ্বারা প্রকাশ করা হয়। H ব্যতীত সকল পরমাণুতেই নিউট্রন রয়েছে।
কোনো মৌলের নিউক্লিয়াসে অবস্থিত প্রোটন সংখ্যাকে পারমাণবিক সংখ্যা বলা হয়। অর্থাৎ উক্ত মৌলটির পারমাণবিক সংখ্যা 9। আর পারমাণবিক সংখ্যাই মৌলটির আসল পরিচয়। অর্থাৎ, পারমাণবিক সংখ্যা 9 হলে মৌলটি হবে ফ্লোরিন (F)।
কোনো মৌলের একটি পরমাণুর নিউক্লিয়াসে অবস্থিত প্রোটনের সংখ্যাই হচ্ছে ঐ মৌলের পারমাণবিক সংখ্যা। দেখা যাচ্ছে, X পরমাণুর নিউক্লিয়াসে মোট 12টি প্রোটন অবস্থিত। এজন্য X এর পারমাণবিক সংখ্যা 12। পরমাণুর পারমাণবিক সংখ্যা প্রতীকের নিচে বাম পাশে লেখা হয়। যেমন, 12X দ্বারা বুঝায় মৌলটি হচ্ছে Mg, যার পারমাণবিক সংখ্যা 12।
কোনো মৌলের একটি পরমাণুর নিউক্লিয়াসে অবস্থিত প্রোটনের সংখ্যাই হচ্ছে ঐ মৌলের পারমাণবিক সংখ্যা। সিলিকন (Si) এর পারমাণবিক সংখ্যা 14 বলতে বুঝায়, Si পরমাণুর নিউক্লিয়াসে '14টি প্রোটন আছে।
কোনো মৌলের একটি পরমাণুর নিউক্লিয়াসে অবস্থিত প্রোটনের সংখ্যাকে ঐ মৌলের পারমাণবিক সংখ্যা বলে। Al এর পারমাণবিক সংখ্যা 13. বলতে AI পরমাণুর নিউক্লিয়াসে 13টি প্রোটন আছে।
পরমাণু সামগ্রিকভাবে চার্জ শূন্য। কারণ পরমাণুর কেন্দ্রে নিউক্লিয়াসে ধনাত্মক চার্জযুক্ত যতগুলো প্রোটন থাকে ঠিক ততগুলো ঋণাত্মক চার্জযুক্ত ইলেকট্রন নিউক্লিয়াসের বাইরে পরমাণুতে অবস্থান করে। এ ধনাত্মক ও ঋণাত্মক চার্জ পরস্পরকে প্রশম করে দেয় বলে পরমাণু চার্জ শূন্য হয়ে যায়।
জানা আছে, পরমাণুর নিউক্লিয়াসকে কেন্দ্র করে বিভিন্ন কক্ষপথে ইলেকট্রন ঘূর্ণায়মান। কোনো পরমাণুর নিউক্লিয়াসে যে কয়টি প্রোটন থাকে, নিউক্লিয়াসের বাইরে সে কয়টি ইলেকট্রন থাকে। অর্থাৎ, Na পরমাণুর কেন্দ্রে 11 টি প্রোটন (P') থাকে এবং নিউক্লিয়াসের বাইরে 11টি থাকে। যেহেতু প্রোটন এবং ইলেকট্রনের চার্জ একে অপরের সমান ও বিপরীত চিহ্নের, তাই Na পরমাণুর - সামগ্রিকভাবে চার্জ শূন্য।
কোনো পরমাণুর নিউক্লিয়াসে উপস্থিত প্রোটন ও নিউট্রন সংখ্যার যোগফলকে ঐ পরমাণুর ভরসংখ্যা বলে। অর্থাৎ, ভরসংখ্যা হচ্ছে প্রোটন সংখ্যা ও নিউট্রন সংখ্যার সমষ্টি। Na এর ভরসংখ্যা 23 বলতে বুঝায়, Na পরমাণুর নিউক্লিয়াসে প্রোটন সংখ্যা 11 এবং নিউট্রন সংখ্যা (23-11) = 12, যাদের সমষ্টি (11+12) = 23 হচ্ছে এর ভর সংখ্যা।
মৌলের নিউক্লিয়ন সংখ্যা তথা ভরসংখ্যা থেকে প্রোটন সংখ্যা বাদ দিলেই উক্ত মৌলের নিউট্রন সংখ্যা পাওয়া যায়। যেমন-অ্যালুমিনিয়ামের প্রোটন সংখ্যা 13 এবং ভরসংখ্যা 27 সুতরাং, অ্যালুমিনিয়াম (Al) এর নিউট্রন সংখ্যা = ভরসংখ্যা প্রোটন সংখ্যা =27-13-14
পরমাণুর মধ্যে 1টি ইলেকট্রন যুক্ত হলে ঋণাত্মক আধানের সৃষ্টি হয়, অর্থাৎ আয়নে পরিণত হবে। আবার পরমাণুটির মধ্যে ২টি নিউট্রন যুক্ত হলে এর পারমাণবিক ভর আগের তুলনায় 2 বৃদ্ধি পাবে। অর্থাৎ পরমাণুটিথেকে অবস্থা প্রাপ্ত হবে। এক কথায়,এর পরিবর্তিত রূপ: ।
পরমাণুর মধ্যে 1টি ইলেকট্রন যুক্ত হলে ঋণাত্মক আধানের সৃষ্টি হয়, অর্থাৎ আয়নে পরিণত হবে। আবার পরমাণুটির মধ্যে ২টি নিউট্রন যুক্ত হলে এর পারমাণবিক ভর আগের তুলনায় 2 বৃদ্ধি পাবে। অর্থাৎ পরমাণুটি থেকে অবস্থা প্রাপ্ত হবে। এক কথায়,এর পরিবর্তিত রূপ:
বলতে বুঝায় ম্যাগনেসিয়াম (Mg) মৌলটির :
(i) প্রোটন সংখ্যা = 12
(ii) ইলেকট্রন সংখ্যা = (12-2) = 10
(iii) নিউট্রন সংখ্যা = (24-12) = 12
(iv) ভরসংখ্যা = 24
(v) পারমাণবিক সংখ্যা তথা প্রোটন সংখ্যা যেহেতু 12, তাই মৌলটি ম্যাগনেসিয়াম (Mg)|
বলতে বুঝায়-
i. মৌলটির প্রোটন সংখ্যা = 17
ii. মৌলটির ইলেকট্রন সংখ্যা = 18
iii. মৌলটির নিউট্রন সংখ্যা 35-17-18
iv. মৌলটির পারমাণবিক সংখ্যা = 17
v. মৌলটির পারমাণবিক ভর = 35
পরমাণুর ভর ও পারমাণবিক ভরের মধ্যে ২টি পার্থখ্য নিম্নরূপ-
| পরমাণুর ভর | পারমাণবিক ভর |
| ১. পরমাণুর ডর বলতে কোনো মৌলের একটি পরমাণুর ভরকে বোঝায়। এর একক g। | ১. পারমাণবিক ভর বলতে যেকোনো মৌলের একটি পরমাণুর ভর এবং 1টি কার্বন-12 আইসোটোপের ভরের অংশের অনুপাতকে বোঝায়। |
| ২. পরমাণুর ভর =মৌলের গ্রাম পারমাণবিক ভর/অ্যাভোগেড্রো সংখ্যা | =মৌলের একটি পরমাণুর ভর/একটি কার্বন 12 আইসোটোপের ভরের অংশ |
পারমাণবিক সংখ্যা ও ভর সংখ্যার মধ্যে ২টি পার্থক্য নিম্নরূপ :
| পারমাণবিক সংখ্যা | ভর সংখ্যা |
| ১. কোনো মৌলের কেন্দ্রে অবস্থিত মোট প্রোটন সংখ্যাকে ঐ মৌলের পারমাণবিক সংখ্যা বলে। | ১. মৌলের কেন্দ্রে অবস্থিত প্রোটন ,নিউট্রনের মোট সংখ্যাকে পারমাণবিক ভরসংখ্যা বা নিউক্লিয়ন সংখ্যা বলে। |
| ২. পারমাণবিক সংখ্যাকে Z দ্বারা প্রকাশ করা হয়। | ২. ভর সংখ্যাকে A দ্বারা প্রকাশ করলে, A = Z + n; n = নিউট্রন সংখ্যা। |
সংকেতটির K দ্বারা পটাশিয়াম মৌলকে বুঝায়। সংকেতটির বামপাশে উপরের দিকে 39 দ্বারা পটাশিয়ামের (K) ভরসংখ্যাকে বুঝানো হয়েছে। আর বাম পাশের নিচের দিকের 19 দ্বারা K এর পারমাণবিক সংখ্যাকে বুঝানো হয়েছে। আবার ডানপাশের উপরের '+' চিহ্ন দ্বারা একটি ইলেকট্রন ত্যাগ করে একক ধনাত্মক চার্জযুক্ত K+ সৃষ্টি করাকে বুঝানো হয়েছে। অর্থাৎ, K এর ইলেকট্রন সংখ্যা = (19-1)=18
রাদারফোর্ড পরমাণু মডেলের দুইটি সীমাবদ্ধতা নিম্নরূপ:
১. সৌরজগতের গ্রহগুলো চার্জহীন কিন্তু ইলেকট্রন ঋণাত্মক চার্জযুক্ত।
২. বর্ণালি রেখার কোনো ধারণা এ মডেলে নেই।
সৌরজগতে সূর্যকে কেন্দ্র করে বিভিন্ন কক্ষপথে যেমন গ্রহগুলো ঘুরে, তেমনি, পরমাণু মডেলে নিউক্লিয়াসকে কেন্দ্র করে বিভিন্ন কক্ষপথে ইলেকট্রন ঘুরছে। অর্থাৎ, রাদারফোর্ডের পরমাণু মডেলকে সৌরজগতের সাথে তুলনা করা হয়েছে বলে এ মডেলটিকে সোলার সিস্টেম মডেল বা সৌর মডেল বলা হয়।
বোর পরমাণু মডেলের দুইটি সীমাবদ্ধতা নিম্নরূপ:
১. বোর পরমাণু মডেলের সাহায্যে একাধিক ইলেকট্রন বিশিষ্ট পরমাণুর পারমাণবিক বর্ণালি ব্যাখ্যা করা যায় না।
২. বোর পরমাণুর মডেল অনুসারে পরমাণুতে শুধু বৃত্তাকার কক্ষপথ বিদ্যমান। কিন্তু পরে প্রমাণিত হয়েছে পরমাণুতে ইলেকট্রন শুধু বৃত্তাকার কক্ষপথেই নয়, উপবৃত্তাকার কক্ষপথেও ঘুরে।
জানা আছে, প্রধান শক্তিস্তরে ইলেকট্রন ঘূর্ণনের সময় কোনো শক্তি শোষণ বা বিকিরণ করে না। তবে ইলেকট্রন যখন নিম্ন শক্তিস্তর থেকে উচ্চ শক্তিস্তরে যায় তখন শক্তি শোষণ করে। আবার, ইলেকট্রন যখন উচ্চ শক্তিস্তর থেকে নিম্ন শক্তিস্তর-এ যায় তখন শক্তির বিকিরণ হয়। ইলেকট্রন উচ্চ শক্তিস্তর থেকে নিম্ন শক্তিস্তরে যাবার সময় যে আলো বিকিরণ করে তাকে প্রিজমের মধ্যদিয়ে puss করালে পারমাণবিক বর্ণালি(atomicspectra) সৃষ্টি হয়।
অরবিট ও অরবিটালের মধ্যে দুইটি পার্থক্য নিম্নরূপ
| অরবিট | অরবিটাল |
| ১. পরমাণুর যেসব স্থির কক্ষপথে ইলেকট্রনগুলো নিউক্লিয়াসকে কেন্দ্র করে আবর্তন করে তাদেরকে অরবিট বলে। | নিউক্লিয়াসের চতুর্দিকে যে অঞ্চলে আবর্তনশীল ও নির্দিষ্ট শক্তিযুক্ত ইলেকট্রন মেঘের সর্বাধিক প্রাপ্তির সম্ভাবনা থাকে, তাকে অরবিটাল বলে। |
| ২. 'অরবিট' শব্দটির উৎস হচ্ছে বোর প্রদত্ত হাইড্রোজেন পরমাণুর গঠন সংক্রান্ত মতবাদ। | 'অরবিটাল' শব্দটির উৎস হচ্ছে কোয়ান্টাম বল বিদ্যা। |
বিভিন্ন শেলে সর্বোচ্চ ইলেকট্রন ধারণ ক্ষমতার সূত্র 2n2 (যেখানে n = 1, 2, 3 ,4...) । সূত্রানুসারে-
K শেলে ধারণ ক্ষমতা = টি
L শেলে সর্বোচ্চ ইলেকট্রন ধারণ ক্ষমতা = টি
M শেলে সর্বোচ্চ ইলেকট্রন ধারণা ক্ষমতা = টি
N শেলে সর্বোচ্চ ইলেকট্রন ধারণ ক্ষমতা = = 32 টি
উপস্তরগুলোকে s, p, d, f' নামে আখ্যায়িত করা হয়।
s উপশক্তিস্তরে সর্বোচ্চ ইলেকট্রন ধারণ ক্ষমতা ২টি।
p উপশক্তিস্তরে সর্বোচ্চ ইলেকট্রন ধারণ ক্ষমতা 6টি।
d উপশক্তিস্তরে সর্বোচ্চ ইলেকট্রন ধারণ ক্ষমতা 10টি।
ঐ উপশক্তিস্তরে সর্বোচ্চ ইলেকট্রন ধারণ ক্ষমতা 14টি।
N শেল হলো চতুর্থ শক্তিস্তর। N শেলের উপস্তর হলো 4টি।
যথা- 4s, 4p, 4d ও 4f
4s উপস্তরে ইলেকট্রন ধারণ ক্ষমতা ২টি।
4p উপস্তরে ইলেকট্রন ধারণ ক্ষমতা 6টি।
4d উপস্তরে ইলেকট্রন ধারণ ক্ষমতা 10টি।
4f উপস্তরে ইলেকট্রন ধারণ ক্ষমতা 14টি।
M শেল হলো তৃতীয় প্রধান শক্তিস্তর। M শেলের উপস্তরগুলো
3টি। যথা: 3s, 3p, 3d 1
3s উপস্তরে ইলেকট্রন ধারণ ক্ষমতা 2টি
3p উপস্তরে ইলেকট্রন ধারণ ক্ষমতা 6টি
3d উপস্তরে ইলেকট্রন ধারণ ক্ষমতা 10টি
পরমাণুতে ইলেকট্রন ইলেকট্রন বিন্যাসের ৩টি নীতি রয়েছে।
যেমন- ১. পাওলির বর্জন নীতি,
২. আউফ-বাউ নীতি,
৩. হুন্ডস এর সূত্র।
তৃতীয় শক্তিস্তরে f অরবিটাল অসম্ভব। কারণ তৃতীয় শক্তিস্তরের জন্য n = 3 এবং/= 0, 1, 2 । জানা আছে/ এর মান 0, 1 ও 2 এর জন্য s, p ও d অরবিটাল সম্ভব হয়। তাই ৩য় শক্তিস্তরে f orbital নেই তথা অসম্ভব।
দ্বিতীয় প্রধান শক্তিস্তরে এ অরবিটাল থাকে না। কারণ দ্বিতীয় প্রধান শক্তিস্তরের জন্য n = 2 সেক্ষেত্রে: উপশক্তিস্তর I = 0 । আমরা জানি,/ এর মান ০ ও। এর জন্য S ও p'অরবিটাল অসম্ভব। এজন্য 2d অরবিটাল দ্বিতীয় প্রধান শক্তিস্তরে থাকে না।
দুটি অরবিটালের মধ্যে যার (n+1) এর মান কম, তার শক্তিও কম হয়।
2p অরবিটালের জন্য: n = 2 এবং l = 1
∴ (n' + 1) = 2 + 1 = 3
2s অরবিটালের জন্য n = 2 এবং/=0
∴ (n + l) = 2 + 0 = 2
দেখা যাচ্ছে যে, 2p ও 2s এর মধ্যে 2s এর (n+1) এর মান কম, তাই 2s এর শক্তিও কম।
দুটি অরবিটালের মধ্যে কোনটি নিম্নশক্তির আর কোনটি উচ্চশক্তির তা (n + /) এর মানের ওপর নির্ভর করে। যার (n + /) এর মান কম সেটি নিম্নশক্তির অরবিটাল। 3p ও 3d অরবিটালের জন্য (n + /) এর মান নিম্নরূপ 3p অরবিটালে: n=3,/=1 ∴ n + /= 3 + 1 = 4
3d অরবিটালে : n = 3, /= 2 ∴ n + / = 3 + 2 = 5
দেখা যাচ্ছে যে, 3p এর ক্ষেত্রে (n + /) এর মান কম। তাই 3p অরবিটালের শক্তি 3d অপেক্ষা কম।
অরবিটালের শক্তি নির্ধারণ করা হয় (n + /) এর মান হিসাব করে। যে অরবিটালের (n + /) এর মান বেশি সেটির শক্তি বেশি।
4s অরবিটালের ক্ষেত্রে== n + /= 4 + 0 = 4
3d অরবিটালের ক্ষেত্রে = n + / = 3 + 2 = 5
যেহেতু 4s অরবিটালের (n + 1) এর মান কম, সেহেতু এর শক্তি কম।
2d ও 3f অরবিটাল অসম্ভব। কারণ 2d অরবিটালের ক্ষেত্রে, n = 2, /= 0, 1/ এর মান 0,1 এর জন্য s ও p অরবিটাল সম্ভব। তাই 2d অসম্ভব। আবার, 3f অরবিটালের ক্ষেত্রে, n = 3, /= 0, 1, 2 / এর মান 0; 1, 2 এর জন্য s, p, d অরবিটাল সম্ভব। এজন্য 31 অরবিটাল অসম্ভব।
দুটি অরবিটালের মধ্যে যার (n+/) এর মান কম সেটি নিম্নশক্তির অরবিটাল। 3d এবং 4s অরবিটালের জন্য (n+/) এর মান নিম্নরূপ :
3d অরবিটালে: n = 3, /= 2 ∴ n + 1 = 3 + 2 = 5
4s অরবিটালে: n=4, s = 0 ∴ n + / = 4 + 0 = 4
সুতরাং 3d এর চেয়ে 4s অরবিটালের শক্তি কম (4s < 3d) হওয়ায় পটাসিয়ামের 19তম ইলেকট্রন 3d অরবিটালে না গিয়ে 4s অরবিটালে স্থান গ্রহণ করে। ফলে K(19) এর ইলেকট্রন বিন্যাস হয়-
K(19)→ 1s22s22p63s23p64s1 |
29X (29) → 1s2 2s2 2p6 3s2 3p6 3d10 4s1 এখানে, মৌলটির ইলেকট্রন বিন্যাসে d9 এর পরিবর্তে d১০ হয়েছে কারণ d১০ হলো পূর্ণ। যেহেতু d9এর পরিবর্তে d10 পূর্ণ। তাই স্থিতিশীলতা লাভের জন্য 4s² অরবিটাল থেকে একটি ইলেকট্রন লাফ দিয়ে 3d অরবিটালে চলে আসে। তাই মৌলটির ইলেকট্রন বিন্যাস সাধারণ নিয়মে না হয়ে ব্যতিক্রমশীলতা প্রদর্শন করে।
ইলেকট্রন বিন্যাস থেকে দেখা যাচ্ছে, আয়নের d অরবিটাল ইলেকট্রন দ্বারা অর্ধপূর্ণ থাকে বলে Fe3+ আয়নটি সুস্থিত।
সাধারণ নিয়মে এর ইলেকট্রন বিন্যাস 3d4 4s2 হওয়ার কথা। কিন্তু অর্ধপূর্ণ অরবিটাল অধিক স্থিতিশীল হওয়ার কারণে স্থিতিশীলতা অর্জনের জন্য বহিঃস্থ 4s2 থেকে। টি e 3d-এ স্থানান্তরিত হয়ে অর্ধপূর্ণ 3d' ইলেকট্রন বিন্যাস হয়। তাই Cr এর ইলেকট্রন বিন্যাস সাধারণ নিয়মে হয় না তথা ব্যতিক্রম হয়।
একই মৌলের যেসব পরমাণুর প্রোটন সংখ্যা সমান কিন্তু ভরসংখ্যা ভিন্ন তাদেরকে পরস্পরের বলা হয় আইসোটোপ। যেমন-হাইড্রোজেন মৌলের তিনটি আইসোটোপ হলো- প্রোটিয়াম ,.-ডিউটেরিয়াম ও ট্রিটিয়াম যাদের প্রোটন সংখ্যা একই (1) কিন্তু ভরসংখ্যা যথাক্রমে 1, 2ও ও।
একই মৌলের পারমাণবিক সংখ্যা অর্থাৎ, প্রোটন সংখ্যা নির্দিষ্ট ও অপরিবর্তনীয়। কিন্তু ভরসংখ্যা ভিন্ন হতে পারে যেমন-হাইড্রোজেনের প্রোটন সংখ্যা 1। কিন্তু হাইড্রোজেনের তিনটি আইসোটোপ আছে যেমন হাইড্রোজেন, ডিউটেরিয়াম ও ট্রিটিয়াম যাদের ভরসংখ্যা যথাক্রমে 1, 2 ও ও। যেহেতু প্রোটন ও নিউট্রন সংখ্যার যোগফল ভরসংখ্যা, সেহেতু তাদের নিউট্রন সংখ্যা যথাক্রমে 0,1ও 2টি।
আমরা জানি, যে সকল পরমাণুর প্রোটন সংখ্যা একই কিন্তু ভরসংখ্যা ভিন্ন তাদেরকে পরস্পরের আইসোটোপ বলে। প্রোটিয়াম ডিউটেরিয়াম ও ট্রিটিয়াম প্রতিটি পরমাণুরই প্রোটন সংখ্যা অভিন্ন কিন্তু ভর সংখ্যা ভিন্ন। এ কারণে প্রোটিয়াম, ডিউটেরিয়াম ও ট্রিটিয়াম পরস্পরের আইসোটোপ।
এবং পরস্পর আইসোটোপ। জানা আছে, যে সব পরমাণুর প্রোটন সংখ্যা একই কিন্তু ভর সংখ্যা ও নিউট্রন সংখ্যা ভিন্ন তাদেরকে পরস্পর আইসোটোপ বলে । ও পরমাণুদ্বয়ের প্রোটন সংখ্যা 1 । এদের ভরসংখ্যা ভিন্ন (1ও 3) এবং নিউট্রন সংখ্যা ভিন্ন (0, 2)। এজন্য ও পরস্পরের আইসোটোপ।
আইসোটোপ ও আইসোবারের মধ্যে পার্থক্য নিম্নরূপ-
| আইসোটোপ | আইসোবার |
| ১. যেসব পরমাণুর প্রোটন সংখ্যা সমান, কিন্তু ভর সংখ্যা ভিন্ন হয়, সেসব পরমাণুকে পরস্পরের আইসোটোপ বলে | ১. যেসব পরমাণুর ভর সংখ্যা অর্থাৎ নিউক্লিয়াসে প্রোটন ও নিউট্রনের মোট সংখ্যা সমান হয়, কিন্তু প্রোটন সংখ্যা ভিন্ন হয়, তাদেরকে আইসোবার বলে |
| ২. একই মৌলের পরমাণু। | ২. ভিন্ন ভিন্ন মৌলের পরমাণু। |
যেসব মৌলের পরমাণুর পারমাণবিক সংখ্যা সমান কিন্তু ভরসংখ্যা ভিন্ন তাদেরকে পরস্পরের আইসোটোপ বলা হয়। মৌলদ্বয়ের পারমাণবিক সংখ্যা সমান (6) কিন্তু ভরসংখ্যা যথাক্রমে 12 ও 13 অর্থাৎ ভিন্ন। কাজেই এরা পরস্পরের আইসোটোপ
14C আইসোটোপ জীবাশ্ম, মমি, উল্কাপিণ্ড ইত্যাদি থেকে আরম্ভ করে পৃথিবীর বয়স নির্ধারণে ব্যবহৃত হয়। জীবিত উদ্ভিদ বা প্রাণিদেহে যতটুকু আইসোটোপ ক্ষয় হয় ঠিক ততটুকু আবার সৃষ্টি হয় বলে জীবিত অবস্থায় আইসোটোপের পরিবর্তন হয় না। তবে মৃত অবস্থায় আইসোটোপ সৃষ্টি বন্ধ হয়ে যায়। ফলে ক্ষয়প্রাপ্ত তেজস্ক্রিয় আইসোটোপের পরিমাণ দেখে মৃতের বয়স নির্ধারণ করা যায়।
একটি মৌলের যেকোনো পরমাণুর পারমাণবিক সংখ্যা নির্দিষ্ট ও অপরিবর্তনীয়। কিন্তু পরমাণুর নিউক্লিয়াসে উপস্থিত নিউট্রন সংখ্যার তারতম্যের কারণে একই মৌলের পরমাণুগুলোর ভরসংখ্যা পরিবর্তিত হয়। এভাবেই' একই পারমাণবিক সংখ্যাবিশিষ্ট মৌলের ভিন্ন ভরসংখ্যা বিশিষ্ট পরমাণু পাওয়া যায়। যেমন- হাইড্রোজেন মৌলের একই পারমাণবিক সংখ্যা (1) কিন্তু ভিন্ন ভরসংখ্যা বিশিষ্ট (1, 2, 3) তিনটি আইসোটোপ পাওয়া যায়।
কোনো মৌলের একটি পরমাণুর ভরকে প্রমাণ হিসেবে ধরে তার সাপেক্ষে অপর কোনো মৌলের একটি পরমাণু কতগুণ ভারী এই আপেক্ষিক রাশিকে সংশ্লিষ্ট মৌলের আপেক্ষিক পারমাণবিক ভর বলা হয়। ক্লোরিনের আপেক্ষিক পারমাণবিক ভর 35.5 বলতে বোঝায় যে ক্লোরিনের একটি পরমাণুর ভর হাইড্রোজেনের একটি পরমাণুর ভরের 35.5 গুণ (হাইড্রোজেন স্কেল অনুসারে)।
কোনো মৌলের একটি পরমাণুর ভরকে প্রমাণ হিসেবে ধরে তার সাপেক্ষে অপর কোনো মৌলের একটি পরমাণু কতগুণ ভারী এই আপেক্ষিক রাশিকে সংশ্লিষ্ট মৌলের আপেক্ষিক পারমাণবিক ভর বলা হয়। F-এর আপেক্ষিক পারমাণবিক ভর 19 বলতে বোঝায় যে, F একটি পরমাণুর ভর হাইড্রোজেনের একটি পরমাণুর ভরের 19 গুণ (হাইড্রোজেন স্কেল অনুসারে)।,
কোনো মৌলের একটি পরমাণুর ভরকে প্রমাণ হিসেবে ধরে তার সাপেক্ষে অপর কোনো মৌলের একটি পরমাণু কতগুণ ভারী এই আপেক্ষিক রাশিকে সংশ্লিষ্ট মৌলের আপেক্ষিক পারমাণবিক ভর বলা হয়। নাইট্রোজেনের আপেক্ষিক পারমাণবিক ভর 14 বলতে বোঝায় যে, নাইট্রোজেনের একটি পরমাণুর ভর হাইড্রোজেনের একটি পরমাণুর ভরের 14 গুণ (হাইড্রোজেন স্কেল অনুসারে)।
কোনো মৌলের আপেক্ষিক পারমাণবিক ভরকে নিম্নরূপে প্রকাশ করা হয়-মৌলের আপেক্ষিক পারমাণবিক ভর
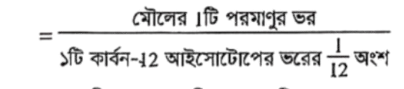
সুতরাং, দেখা যায়, আপেক্ষিক পারমাণবিক ভর দুটি পৃথক ভরের অনুপাত (kg/kg বা g/g)। তাই এর কোনো একক থাকে না।
কার্বনের আপেক্ষিক পারমাণবিক ভর 12 এবং অক্সিজেনের আপেক্ষিক পারমাণবিক ভর 16। যেহেতু CO2 অণুটি একটি কার্বন পরমাণু এবং ২টি অক্সিজেন পরমাণু নিয়ে গঠিত। সুতরাং, CO2 এর আপেক্ষিক আণবিক ভর হবে = 12 + (162) = 44 ।
অণুতে উপস্থিত H পরমাণুর সংখ্যা =2
S পরমাণুর সংখ্যা = 1
O পরমাণুর সংখ্যা = 4
আবার, H এর আপেক্ষিক পারমাণবিক ভর = 1
S এর আপেক্ষিক পারমাণবিক ভর 32
O এর আপেক্ষিক পারমাণবিক ভর= 16
সুতরাং এর আপেক্ষিক আণবিক ভর = 98 ।
HNO1 অণুস্থ H পরমাণুর সংখ্যা = 1
N পরমাণুর সংখ্যা = 1
O পরমাণুর সংখ্যা = 3
আবার, H এর আপেক্ষিক পারমাণবিক ভর =.।
N এর আপেক্ষিক পারমাণবিক ভর= 14
O এর আপেক্ষিক পারমাণবিক ভর = 16
সুতরাং, HNO3 এর আপেক্ষিক আণবিক ভর =
অর্থাৎ, HNO3 এর আপেক্ষিক আণবিক ভর = 63 ।
কিছু কছু আইসোটোপ রয়েছে, যাদের নিউক্লিয়াস স্বতঃস্ফূর্তভাবে (নিজে নিজেই) ভেঙে ৫ রশ্মি, ও রশ্মি, y রশ্মি ইত্যাদি নির্গত করে, তাদেরকে তেজস্ক্রিয় আইসোটোপ বলে। তেজস্ক্রিয় আইসোটোপ এর নিয়ন্ত্রিত ব্যবহার দিয়ে মানুষ অনেক কিছু করতে পারে। যেমন- চিকিৎসা ক্ষেত্রে, কৃষিক্ষেত্রে, বিদ্যুৎ উৎপাদনে তেজস্ক্রিয় আইসোটোপের ব্যাপক ব্যবহার রয়েছে।
চিকিৎসাক্ষেত্রে তেজস্ক্রিয় আইসোটোপের দুটি ব্যবহার হলো-
১. টিউমারের উপস্থিতি নির্ণয় ও নিরাময়ে তেজস্ক্রিয় আইসোটোপ ব্যবহার করা হয়।
২. রক্তের লিউকোমিয়া রোগের চিকিৎসায় 32P এর ফসফেট ব্যবহার করা হয়।
কৃষিক্ষেত্রে তেজস্ক্রিয় আইসোটোপের দুইটি প্রায়োগিক দিক হলো-
১. তেজস্ক্রিয় রশ্মি ব্যবহার করে কৃষিক্ষেত্রে নতুন নতুন উন্নত মানের বীজ উদ্ভাবন করা হচ্ছে এবং এর মাধ্যমে ফলনের মানের উন্নতি ও পরিমাণ বাড়ানো হচ্ছে।
২. তেজস্ক্রিয় 32Pযুক্ত ফসফেট দ্রবণ উদ্ভিদের মূলধারায় সূচিত করা হয়। গাইগার কাউন্টার ব্যবহার করে পুরো উদ্ভিদে এর চলাচল চিহ্নিত করে বিজ্ঞানীরা কী কৌশলে (mechanism) ফসফরাস ব্যবহার করে উদ্ভিদ বেড়ে উঠে তা জানতে পারেন।
তেজস্ক্রিয়তার দুইটি ক্ষতিকর দিক নিম্নরূপ-
১.. তেজস্ক্রিয় পদার্থ থেকে নির্গত বিভিন্ন রশ্মি ক্যান্সার সৃষ্টির বিশেষ কারণ।
২. সব ধরনের পারমাণবিক বোমায় তেজস্ক্রিয়তার ব্যবহার মানব জাতির অস্তিত্বের জন্য হুমকিস্বরূপ।
দুই বা দুইয়ের অধিক সংখ্যক পরমাণু পরস্পরের সাথে রাসায়নিক বন্ধন এর মাধ্যমে যুক্ত থাকলে তাকে অণু বলে।
পরমাণু হলো মৌলিক পদার্থের ক্ষুদ্রতম কণা যার মধ্যে মৌলের গুণাগুণ থাকে।
যে পদার্থকে ভাঙলে সেই পদার্থ ছাড়া অন্য কোনো পদার্থ পাওয়া যায় না তাকে মৌল বা মৌলিক পদার্থ বলে।
মানুষের শরীরে ২৬ ধরনের ভিন্ন ভিন্ন মৌল রয়েছে।
কোনো মৌলের ইংরেজি বা ল্যাটিন নামের সংক্ষিপ্ত রূপকে মৌলের প্রতীক বলে।
পটাশিয়ামের ল্যাটিন নাম হলো Kalium।
বক্সাইটের সংকেত হলো- Al2O3.2H2O।
সালফার অণুর সংকেত S৪।
ক্যালসিয়াম ফসফেটের সংকেত: Ca3(PO4)2 ।
লেড (Lead) মৌলের প্রতীক Pb ।
কোনো মৌলের একটি পরমাণুর নিউক্লিয়াসে উপস্থিত প্রোটনের সংখ্যাকে ঐ মৌলের পারমাণবিক সংখ্যা বলে।
আর্সেনিক (As) এর পারমাণবিক সংখ্যা 33 ।
কোনো পরমাণুর নিউক্লিয়াসে উপস্থিত প্রোটন ও নিউট্রন সংখ্যার যোগফলকে ঐ পরমাণুর ভরসংখ্যা বলা হয়।
একটি নিউট্রনের প্রকৃত ভর
পরমাণুর স্থায়ী কণিকাসমূহ হলো ইলেকট্রন, প্রোটন ও নিউট্রন।
একটি প্রোটনের ভর
একটি ইলেকট্রনের ভর ।
নিউট্রনের প্রকৃত আধান শূন্য (০)।
চার্জবিহীন মূল কণিকা নিউট্রন।
ইলেকট্রনের আধান কুলম্ব।
একই পারমাণবিক ভরবিশিষ্ট বিভিন্ন মৌলের পরমাণুকে পরস্পরের আইসোমার বলে।
পরমাণুর কেন্দ্রে প্রোটন ও নিউট্রন থাকে।
পরমাণুর কেন্দ্র বা নিউক্লিয়াস প্রোটন ও নিউট্রন দ্বারা গঠিত।
পারমাণবিক সংখ্যাকে Z এবং ভর সংখ্যাকে A দ্বারা চিহ্নিত করা হয়।
প্রোটন সংখ্যা তথা পারমাণবিক সংখ্যা পরমাণুর নিজস্ব সত্তা ও পরিচয় বহন করে।
পরমাণুর নিউট্রন কণা আধান নিরপেক্ষ হয়।
প্রোটনের আপেক্ষিক আধান +1 ।
নীল'স বোর 1913 সালে পরমাণু মডেল প্রদান করেন।
৫-কণা হলো দ্বি-ধনাত্মক হিলিয়াম নিউক্লিয়াস ।
আলফা কণা (a-কণা) বিচ্ছুরণ পরীক্ষার সিদ্ধান্তের ভিত্তিতে রাদারফোর্ড পরমাণুর মডেল প্রদান করেন।
ইলেকট্রন উচ্চ শক্তিস্তর থেকে নিম্ন শক্তিস্তরে যাবার সময় যে - আলো বিকিরণ করে তাকে প্রিজমের মধ্যদিয়ে প্রবেশ করালে সৃষ্ট - আলোক রশ্মিকে পারমাণবিক বর্ণালি (Atomic Spectra) বলে।
পরমাণুতে বিদ্যমান প্রতিটি প্রধান শক্তিস্তর কতকগুলো উপশক্তিস্তরে বিভক্ত থাকে যাদেরকে অর্বিটাল বলে।
পরমাণুর যে সকল স্থির কক্ষপথে ইলেকট্রনগুলো নিউক্লিয়াসকে কেন্দ্র করে আবর্তন করে তাদেরকে অরবিট বলে।
প্রতিটি প্রধান শন্তিস্তরের সর্বোচ্চ ইলেকট্রন ধারণ ক্ষমতা 2n2; যেখানে n = 1, 2, 3, 4 ইত্যাদি।
যে সকল পরমাণুর প্রোটন সংখ্যা সমান কিন্তু ভরসংখ্যা ও নিউট্রন সংখ্যা ভিন্ন তাদেরকে একে অপরের আইসোটোপ বলে।
হাইড্রোজেনের 7টি আইসোটোপ বিদ্যমান।
কোনো একটি পরমাণুর ভর এবং একটি কার্বন-12 পরমাণু ভরের অংশের অনুপাতকে ঐ মৌলের পারমাণবিক ভর বলে।
পর্যায় সারণিতে যে পারমাণবিক ভর লেখা আছে, তা মূলত গড় আপেক্ষিক, পারমাণবিক ভর; যেমন, 'Cu এর গড় আপেক্ষিক পারমাণবিক ভর 63.5 ।
প্রোটন ও নিউট্রনের আপেক্ষিক ভর সমান হয়।
আপেক্ষিক পারমাণবিক ভরের কোনো একক নেই।
কোনো পরমাণুর আইসোটোপ না থাকলে তার আপেক্ষিক পারমাণবিক ভর ও ভরসংখ্যা সমান হয়।
যে সকল আইসোটোপের নিউক্লিয়াস স্বতঃস্ফূর্তভাবে (নিজে নিজেই) ভেঙে আলফা রশ্মি, বিটা রশ্মি, গামা রশ্মি ইত্যাদি নির্গত করে তাদেরকে তেজস্ক্রিয় আইসোটোপ বলে।
পৃথিবীর বয়স নির্ধারণে কার্বন-14(C-14) আইসোটোপ ব্যবহৃত এটি একটি তেজস্ক্রিয় আইসোটোপ হয়।
তেজস্ক্রিয় মৌল থেকে তেজস্ক্রিয় রশ্মি নির্গমনের ঘটনাকে তেজস্ক্রিয়তা বলে।
বাংলাদেশের পাবনা জেলার রূপপুরে পারমাণবিক বিদ্যুৎকেন্দ্র স্থাপিত হতে যাচ্ছে।
থেকে গামা রশ্মি নির্গত হলে ভরবিশিষ্ট আইসোটোপ উৎপন্ন হয়।
গাইগার কাউন্টার একটি যন্ত্র, যার সাহায্যে তেজস্ক্রিয় মৌল থেকে বিকিরিত রশ্মি বা কণা শনাক্ত করা হয়।
থেকে নির্গত কোন রশ্মিটি ক্যান্সার কোষকে ধ্বংস করতে সক্ষম।
গামা (y) রশ্মি জীবন্ত কোষের ক্ষতি সাধন করতে পারে।
ব্রেইন ক্যান্সার নিরাময়ে ইরিডিয়াম আইসোটোপ ব্যবহার করা হয়।
Cl2 ও 2CI এর মধ্যে পার্থক্য নিম্নরূপ-
| Cl2 | 2CI |
| Cl2 হলো ক্লোরিন অণু। | 2CI হলো ক্লোরিনের দুটি বিচ্ছিন্ন পরমাণু। |
| দুটি CI পরমাণু রাসায়নিক বন্ধনের মাধ্যমে যুক্ত হয়ে Cl2 অণু গঠন করে। | 2CI কোনো রাসায়নিক বন্ধনের মাধ্যমে যুক্ত হয়ে অণু গঠন করেনি। |
পরমাণুর কেন্দ্রের নাম নিউক্লিয়াস। নিউক্লিয়াসের ভিতরে প্রোটন ও নিউট্রন এবং বাইরে ইলেকট্রন অবস্থান করে। যেহেতু আপেক্ষিকভাবে ইলেকট্রনের ভর শূন্য ধরা হয়, কাজেই নিউক্লিয়াসের ভিতরে অবস্থিত প্রোটন ও নিউট্রনের ভরই পরমাণুর ভর হিসাবে বিবেচনা করা হয়। অর্থাৎ পরমাণুর সমস্ত ভর নিউক্লিয়াসে কেন্দ্রীভূত।"
পরমাণুর নিউক্লিয়াস ধনাত্মক চার্জবিশিষ্ট। কারণ নিউক্লিয়াসের অভ্যন্তরে থাকে প্রোটন ও নিউট্রন। প্রোটনের চার্জ ধনাত্মক এবং তা অপরদিকে নিউট্রন চার্জহীন। যেহেতু নিউক্লিয়াসের অভ্যন্তরে কেবল প্রোটনের চার্জ থাকে এবং তা ধনাত্মক, সেহেতু পরমাণুর নিউক্লিয়াস ধনাত্মক চার্জবিশিষ্ট হয়।
বলতে বুঝায় সোডিয়াম (Na) মৌলটির,
(i) প্রোটন সংখ্যা = 11
(ii) ইলেকট্রন সংখ্যা = (11 - 1) = 10
(iii) নিউট্রন সংখ্যা = (23-11) = 12
(iv) ভরসংখ্যা = 23
(v) পারমাণবিক সংখ্যা তথা প্রোটন সংখ্যা যেহেতু 11, তাই মৌলটি সোডিয়াম (Na)।
কোনো মৌলের একটি পরমাণুর নিউক্লিয়াসে অবস্থিত প্রোটনের সংখ্যাকে ঐ মৌলের পারমাণবিক সংখ্যা বলে। একে Z দ্বারা প্রকাশ করা হয়। Mg পরমাণুর নিউক্লিয়াসে মোট 12টি প্রোটন অবস্থিত। এজন্য Mg এর পারমাণবিক সংখ্যা 12 । পরমাণুর পারমাণবিক সংখ্যা প্রতীকের নিচে বাম পাশে লেখা হয়। যেমন, 12Mg দ্বারা বুঝায় Mg এর পারমাণবিক সংখ্যা 12 ।
কোনো পরমাণুতে উপস্থিত প্রোটন ও নিউট্রন সংখ্যার যোগফলকে ঐ পরমাণুর ভরসংখ্যা বলে। অর্থাৎ ভরসংখ্যা হচ্ছে প্রোটন সংখ্যা ও নিউট্রন সংখ্যার সমষ্টি। Na এর ভরসংখ্যা 23 বলতে বুঝায়, Na পরমাণুর নিউক্লিয়াসে প্রোটন সংখ্যা 11 এবং নিউট্রন সংখ্যা (23-11) 12, যাদের সমষ্টি (11+12) = 23 হচ্ছে এর ভর সংখ্যা।
কোনো মৌলের একটি পরমাণুর ভরকে প্রমাণ হিসাবে ধরে তার সাপেক্ষে অপর কোনো মৌলের একটি পরমাণু কতগুণ ভারী এই আপেক্ষিক রাশিকে সংশ্লিষ্ট মৌলের পারমাণবিক ভর বলে। সালফারের পারমাণবিক ভর 32 এর অর্থ হলো সালফারের একটি পরমাণুর ভর হাইড্রোজেনের একটি পরমাণুর ভরের 32 গুণ (হাইড্রোজেন স্কেল অনুসারে)।
অক্সিজেন পরমাণুর প্রোটন সংখ্যা তথা পারমাণবিক সংখ্যা ৪ এবং ভরসংখ্যা অর্থাৎ প্রোটন ও নিউট্রনের মোট সংখ্যা 16। তাহলে এ অক্সিজেন পরমাণুটির নিউট্রন সংখ্যা হলো 16-8=8 । কাজেই হতে দুটি নিউট্রন সরালে পারমাণবিক সংখ্যা অপরিবর্তিত 8 থাকলেও ভরসংখ্যা 2 হ্রাস পেয়ে 14 হবে। তখন পরিবর্তিত অক্সিজেন পরমাণুর সংক্ষিপ্ত প্রকাশ হবে ।
| পারমাণবিক সংখ্যা (Z ) | ভরসংখ্যা (A) | ইলেকট্রন সংখ্যা | নিউট্রন সংখ্যা (A - Z) | |
| 14 | 28 | 14 | 14 | |
| 15 | 31 | 15 | 16 | |
| 8 | 17 | 8 | 9 | |
| 19 | 39 | 19 | 20 |
রাদারফোর্ড পরমাণু মডেলের সীমাবদ্ধতা নিম্নরূপ:
১. সৌরজগতের গ্রহগুলো চার্জহীন কিন্তু ইলেকট্রন ঋণাত্মক চার্জযুক্ত।
২. একাধিক ইলেকট্রন বিশিস্ট পরমাণুর ক্ষেত্রে এ মডেল ব্যাখ্যা দিতে পারে না।
৩. বর্ণালি রেখার কোনো ধারণা এ মডেলে নেই।
শক্তির উৎস থেকে মৌলের অসংখ্য পরমাণুর একই ইলেকট্রন বিভিন্ন পরিমাণে শক্তি শোষণ করে উদ্দীপিত অবস্থায় বিভিন্ন নির্দিষ্ট শক্তির উচ্চ শক্তিস্তরে লাফিয়ে চলে। পরে শক্তির উৎস সরিয়ে নিলে ঐ অসংখ্য হাইড্রোজেন পরমাণুর ইলেকট্রন শক্তি বিকিরণ করে একই নিম্ন শক্তিস্তরে ফিরে আসতে পারে। তখন বিভিন্ন রেখা বর্ণালির সৃষ্টি হয়ে থাকে।
পরমাণুর যে সকল স্থির কক্ষপথে ইলেকট্রনগুলো নিউক্লিয়াসকে কেন্দ্র করে আবর্তন করে তাদেরকে অরবিট বলে। প্রতিটি অরবিটে সর্বোচ্চ ইলেকট্রন থাকতে পারে 2n2সংখ্যক। যেখানে n = 1, 2, 3, 4…. ইত্যাদি। n = 1 হলে K শেল নির্দেশ করে। অনুরূপভাবে n = 2, 3, 4 ইত্যাদির জন্য L, M, N শেল নির্দেশ করে। আবার 2n2সূত্রানুযায়ী, K, L, M, N শেলে সর্বোচ্চ সংখ্যক ইলেকট্রন থাকতে পারে 2, 8, 18, 32 টি করে।
দুটি অরবিটালের মধ্যে যার (n+1) এর মান কম, তার শক্তিও কম হয়।
2p অরবিটালের জন্য: n = 2 এবং / = 1
∴ (n + 1) = 2 + 1 = 3
2s অরবিটালের জন্য: n = 2 এবং / = 0
∴ (n + l) = 2 + 0 = 2
দেখা যাচ্ছে যে, 2p ও 2s এর মধ্যে 2s এর (n+/) এর মান কম, তাই 2s এর শক্তিও কম।
আউফবাউ নীতি অনুসারে, ইলেকট্রন প্রথমে নিম্নশক্তির অরবিটাল এবং পরে উচ্চ শক্তির অরবিটালে গমন করে। দুটি অরবিটালের মধ্যে কোনটি নিম্নশক্তির আর কোনটি উচ্চশক্তির তা (n+1) এর মানের ওপর নির্ভর করে। যার (n + 1) এর মান কম সেটি নিম্নশক্তির অরবিটাল। 3p ও 3d অরবিটালের জন্য (n + 1) এর মান
নিম্নরূপ:
3p অরবিটালে: n = 3, /= 1 ∴ n + l = 3 + 1 = 4
3d অরবিটালে: n = 3 / = 2 ∴ n + /= 3 + 2 = 5
দেখা যাচ্ছে যে, 3d এর ক্ষেত্রে (n+1) এর মান বেশি। তাই 3d অরবিটালের শক্তি 3p অপেক্ষা বেশি।
৩য় শক্তিভরে। অরবিটাল নেই। কারণ ৩য় শক্তিস্তরের জন্য n = 3 এবং 1 = 0, 1, 2। জানা আছে, 1 এর মান 0,1ও 2 এর জন্য s, p ও d এ অরবিটাল সম্ভব হয়। তাই ৩য় শক্তিস্তরে f orbital নেই।
অরবিটালের শক্তি নির্ধারণ করা হয় (n + l) এর মান হিসাব করে। যে অরবিটালের (n + l) এর মান বেশি সেটির শক্তি বেশি।
4s অরবিটালের ক্ষেত্রে = n + l = 4 + 0 = 4
3d অরবিটালের ক্ষেত্রে = n + 1 = 3 + 2 = 5
যেহেতু 3d অরবিটালের (n + 1) এর মান বেশি, সেহেতু এর শক্তি বেশি।
অরবিটালের শক্তি নির্ধারণ করা হয় (n + I) এর মান হিসাব করে। যে অরবিটালের (n + 1) এর মান বেশি সেটির শক্তি বেশি।
6s অরবিটালে: n=6,/=0 ∴ n + / = 6 + 0 = 6
4d অরবিটালে: n=4,/ =2 ∴ n + I = 4 + 2 = 6
দেখা যাচ্ছে যে, 6s ও 4d অরবিটালের (n + 1) এর মান সমান। এক্ষেত্রে যে অরবিটালের। এর মান বেশি সেই অরবিটালের শক্তিও বেশি। আবার 4d এর n এর মান কম তাই এ অরবিটালের শক্তি কম।
অর্থাৎ 6s অরবিটালের শক্তি 4d অপেক্ষা বেশি।
সাধারণভাবে দেখা যায় যে, সমশক্তিসম্পন্ন অরবিটালসমূহ অর্ধপূর্ণ বা সম্পূর্ণ পূর্ণ হলে সে ইলেকট্রন বিন্যাস অধিকতর সুস্থিতি অর্জন করে। এক্ষেত্রে এবং d5 s1 ইলেকট্রন বিন্যাসবিশিষ্ট মৌল অধিকতর স্থায়ী হয় । কপার (Cu) এর ইলেকট্রন বিন্যাসে সুস্থিতির জন্য 3d94s2
এর 'পরিবর্তে 3d104s1 হয়। এজন্য কপারের ইলেকট্রন বিন্যাস সাধারণ নিয়ম মানে না।
যেসব পরমাণুর প্রোটন সংখ্যা সমান কিন্তু ভরসংখ্যা ও নিউট্রন সংখ্যা ভিন্ন হয়, যেসব পরমাণুকে পরস্পরের আইসোটোপ বলা হয়। যেহেতু, আইসোটোপগুলোর প্রোটন সংখ্যা সমান তাই, নিউট্রন সংখ্যার পার্থক্যের জন্যই ভরসংখ্যা ভিন্ন হয়ে থাকে। তাই, ভরসংখ্যার ভিন্নতা থেকেই আইসোটোপ নির্ধারণ করা যায়।
ডিউটেরিয়াম (H) হাইড্রোজেন (H) এর একটি আইসোটোপ।
নিচে তা ব্যাখ্যা করা হলো:
যেসব পরমাণুর প্রোটন সংখ্যা সমান কিন্তু ভরসংখ্যা ভিন্ন হয় সে সব পরমাণুকে পরস্পরের আইসোটোপ বলা হয়। ডিউটেরিয়াম ও হাইড্রোজেন উভয়ের প্রোটন সংখ্যা 1. অর্থাৎ সমান। আবার ভরসংখ্যা যথাক্রমে 2 এবং 1, অর্থাৎ ভিন্ন। যেহেতু তাদের প্রোটন সংখ্যা একই এবং ভরসংখ্যা ভিন্ন।
সুতরাং তারা পরস্পরের আইসোটোপ।
হাইড্রোজেনের দুটি পরমাণুকে নির্দেশ করে। পরমাণু দুটির ভর সংখ্যা ভিন্ন। আমরা জানি, একটি মৌলের যে কোনো পরমাণুর পারমাণবিক সংখ্যা নির্দিষ্ট ও অপরিবর্তনীয়। কিন্তু পরমাণুর নিউক্লিয়াসে উপস্থিত নিউট্রন সংখ্যার তারতম্যের কারণে ভর সংখ্যা আলাদা হয়। এবং পরমাণু দুটির পারমাণবিক সংখ্যা একই কিন্তু নিউট্রন সংখ্যা যথাক্রমে 0 ও 1 । এ কারণে পরমাণু দুটির ভর সংখ্যার ভিন্নতা দেখা যায়।
একই মৌলের যেসব পরমাণুর প্রোটন সংখ্যা সমান কিন্তু ভরসংখ্যা ভিন্ন তাদেরকে পরস্পরের আইসোটোপ বলা হয়। একই মৌলের এসব পরমাণু পর্যায় সারণিতে একই স্থানের জন্য নির্দিস্ট হওয়ায় এদেরকে আইসোটোপ নামকরণ করা হয়েছে। যেমন-হাইড্রোজেন মৌলের তিনটি আইসোটোপ হলো- প্রোটিয়াম ডিউটেরিয়াম ও ট্রিটিয়াম যাদের প্রোটন সংখ্যা একই ( 1 ) কিন্তু ভরসংখ্যা যথাক্রমে 1.2 ও 3।
যেসব মৌলের পরমাণুর পারমাণবিক সংখ্যা সমান কিন্তু ভরসংখ্যা ভিন্ন তাদেরকে পরস্পরের আইসোটোপ বলা হয়। মৌলদ্বয়ের পারমাণবিক সংখ্যা সমান (৪) কিন্তু ভরসংখ্যা যথাক্রমে 16 ও 1৪ অর্থাৎ ভিন্ন। কাজেই এরা পরস্পরের আইসোটোপ।
একটি মৌলের যেকোনো পরমাণুর পারমাণবিক সংখ্যা নির্দিষ্ট ও অপরিবর্তনীয়। কিন্তু পরমাণুর নিউক্লিয়াসে উপস্থিত নিউট্রন সংখ্যার তারতম্যের কারণে একই মৌলের পরমাণুগুলোর ভরসংখ্যা পরিবর্তিত হয়। এভাবেই একই পারমাণবিক সংখ্যাবিশিষ্ট মৌলের ভিন্ন ভরসংখ্যা বিশিষ্ট পরমাণু পাওয়া যায়। যেমন- হাইড্রোজেন মৌলের একই পারমাণবিক সংখ্যা (1) কিন্তু ভিন্ন ভরসংখ্যা বিশিষ্ট (1. 2, 3) তিনটি আইসোটোপ পাওয়া যায়।
পরমাণুর আপেক্ষিক পারমাণবিক ভর নির্ণয়ে কার্বন-12
আইসোটোপ ব্যবহারের সুবিধা হলো-
১. কার্বন-12 আইসোটোপ অত্যন্ত সহজলভ্য পদার্থ।
২. এ আইসোটোপ অধিক সংখ্যক যৌগ গঠনে অংশ নিতে পারে।
৩. হাইড্রোজেন, অক্সিজেন প্রভৃতি গ্যাসীয় মৌলের পরিবর্তে কার্বন কঠিন মৌল হওয়ায় এর সংরক্ষণ ও ব্যবহার অত্যন্ত সুবিধাজনক।
একই মৌলের পারমাণবিক সংখ্যা অর্থাৎ, প্রোটন সংখ্যা নির্দিষ্ট ও অপরিবর্তনীয়। কিন্তু ভরসংখ্যা ভিন্ন হতে পারে যেমন-হাইড্রোজেনের প্রোটন সংখ্যা।। কিন্তু হাইড্রোজেনের তিনটি আইসোটোপ আছে যেমন হাইড্রোজেন, ডিউটেরিয়াম ও ট্রিটিয়াম যাদের ভরসংখ্যা যথাক্রমে 1, 2 ও ও। যেহেতু প্রোটন ও নিউট্রন সংখ্যার যোগফল ভরসংখ্যা, সেহেতু তাদের নিউট্রন সংখ্যা যথাক্রমে 0,132 টি।
সুতরাং, একই পরমাণুর নিউক্লিয়াসের নিউট্রন সংখ্যা পরিবর্তনের কারণে ভরসংখ্যা পরিবর্তিত হয়।
কোনো মৌলিক বা যৌগিক পদার্থের অণুতে যে পরমাণুগুলো থাকে তাদের আপেক্ষিক পারমাণবিক ভর নিজ নিজ পরমাণু সংখ্যা দিয়ে গুণ করে যোগ করলে প্রাপ্ত যোগফলই হলো ঐ অণুর আপেক্ষিক আণবিক ভর। যেমন H₂O অণুতে উপস্থিত H এর আপেক্ষিক পরমাণবিক ভর 1.0 এবং পরমাণু সংখ্যা 2, O পরমাণুর আপেক্ষিক পারমাণবিক ভর 16 এবং পরমাণু সংখ্যা ।। সুতরাং H2O এর আপেক্ষিক আণবিক ভর =
জানা আছে, দুটি একই রকম রাশি অনুপাত আকারে থাকলে এর কোনো একক থাকে না। কোনো মৌলের আপেক্ষিক পারমাণবিক ভরকে নিম্নরূপে প্রকাশ করা হয়-মৌলের আপেক্ষিক পারমাণবিক ভর ।

সুতরাং, দেখা যায়, আপেক্ষিক পারমাণবিক ভর দুটি পৃথক ভরের অনুপাত (kg/kg বা g/g)। তাই এর কোনো একক্ থাকে না।
কোনো মৌলের একটি পরমাণুর ভরকে প্রমাণ হিসেবে ধরে তার সাপেক্ষে অপর কোনো মৌলের একটি পরমাণু কতগুণ ভারী এই আপেক্ষিক রাশিকে সংশ্লিষ্ট মৌলের আপেক্ষিক পারমাণবিক ভর বলা হয়। অক্সিজেনের আপেক্ষিক পারমাণবিক ভর 16 বলতে বোঝায় যে, অক্সিজেনের একটি পরমাণুর ভর হাইড্রোজেনের একটি পরমাণুর ভরের 16 গুণ (হাইড্রোজেন স্কেল অনুসারে)।
জানা আছে, কোনো মৌলিক বা যৌগিক পদার্থের অণুতে যে পরমাণুগুলো থাকে তাদের আপেক্ষিক পারমাণবিক ভরকে নিজ নিজ পরমাণু সংখ্যা দিয়ে গুণ করে যোগ করলে প্রাপ্ত যোগফলই হলো ঐ অণুর আণবিক ভর। নাইট্রোজেনের আণবিক ভর 28 বলতে বুঝায়, নাইট্রোজেন এর পারমাণবিক ভর (14 2)। কেননা নাইট্রোজেন একটি দ্বি-পরমাণুক গ্যাস (N2)।
এজন্য নাইট্রোজেনের আণবিক ভর = 14 2 = 28 ।
চিকিৎসা ক্ষেত্রে তেজস্ক্রিয় আইসোটোপ গুরুত্বপূর্ণ- নিচে তা ব্যাখ্যা করা হলো:
১. দেহের হাড় বেড়ে যাওয়া এবং কোথায় কেন ব্যথা হচ্ছে তা নির্ণয়ের জন্য Tc-99 m ব্যবহৃত হয়।
২. টিউমারের উপস্থিতি নির্ণয় এবং তা নিরাময়ে তেজস্ক্রিয় আইসোটোপ ব্যবহার করা হয়। থেকে নির্গত গামা রশ্মি ক্যান্সার কোষ কলা ধ্বংস করে।
৩. রক্তের লিউকোমিয়া রোগের চিকিৎসায় 32P এর ফসফেট ব্যবহার করা হয়।
৪. 131I থাইরয়েড গ্রন্থির কোষকলা বৃদ্ধি প্রতিহত করে।
সুতরাং এ থেকে বলা যায় যে, চিকিৎসা ক্ষেত্রে তেজস্ক্রিয় আইসোটোপ গুরুত্বপূর্ণ।
ফসফরাসের তেজস্ক্রিয় রশ্মি ব্যবহার করে কৃষিক্ষেত্রে নতুন নতুন উন্নত মানের বীজ উদ্ভাবন করা হচ্ছে এবং এর মাধ্যমে ফলনের মানের উন্নতি ও পরিমাণ বাড়ানো হচ্ছে। তেজস্ক্রিয় "p যুক্ত ফসফেট দ্রবণ উদ্ভিদের মূলধারায় সূচিত করা হয়। গাইগার কাউন্টার ব্যবহার করে পুরো উদ্ভিদে এর চলাচল চিহ্নিত করে কী কৌশলে উদ্ভিদ বেড়ে উঠে তা ফসফরাস ব্যবহার করে জানা যায়।
তেজস্ক্রিয়তা পদার্থের নিউক্লিয় ধর্ম। তেজস্ক্রিয়তা হলো কোনো পরমাণুর নিউক্লিয়াস থেকে স্বতঃস্ফূর্তভাবে বিভিন্ন রশ্মি (α, β, γ) নির্গমনের ঘটনা। অপরদিকে নিউক্লিয়ার ফিসন বিক্রিয়া হলো একটি বৃহৎ নিউক্লিয়াসকে নিউট্রন কণা দ্বারা আঘাত করে ক্ষুদ্র ক্ষুদ্র নিউক্লিয়াসে পরিণত হওয়ার প্রক্রিয়া। যেহেতু তেজস্ক্রিয়তার মাধ্যমে
পরমাণুর নিউক্লিয়াস থেকে বিভিন্ন রশ্মি নির্গমনের মাধ্যমে ক্ষুদ্র নিউক্লিয়াস যুক্ত পরমাণুতে পরিণত হয়, সেহেতু তেজস্ক্রিয়তা একটি নিউক্লিয়ার ফিসন বিক্রিয়া।
তেজস্ক্রিয় রশ্মি ব্যবহার করে কৃষিক্ষেত্রে নতুন নতুন উন্নত মানের বীজ উদ্ভাবন করা হচ্ছে এবং এর মাধ্যমে ফলনের মানের উন্নতি ও পরিমাণ বাড়ানো হচ্ছে। তেজস্ক্রিয় 32P যুক্ত ফসফেট দ্রবণ উদ্ভিদের মূলধারায় সূচিত করা হয়। গাইগার কাউন্টার ব্যবহার করে পুরো উদ্ভিদে এর চলাচল চিহ্নিত করে বিজ্ঞানীরা কী কৌশলে (mechanism) ফসফরাস ব্যবহার করে উদ্ভিদ বেড়ে উঠে তা জানতে পারেন।
তেজস্ক্রিয়তার ক্ষতিকর দিকগুলো নিম্নরূপ-
১. তেজস্ক্রিয় পদার্থ থেকে নির্গত বিভিন্ন রশ্মি ক্যান্সার সৃষ্টির বিশেষ কারণ।
২. কেমোথেরাপির তেজস্ক্রিয় পদার্থের ব্যবহারের দরুন মাথার চুল পড়ে যায়, বমি বমি ভাব হয় এবং আমাদের জন্য প্রয়োজনীয় ব্যাকটেরিয়ার মৃত্যুর কারণ হয়ে দাঁড়ায়।
৩. সব ধরনের পারমাণবিক বোমায় তেজস্ক্রিয়তার ব্যবহার মানব 'জাতির অস্তিত্বের জন্য হুমকিস্বরূপ।
Related Question
View Allকোন মৌলের একটি পরমাণুর নিউক্লিয়াসে যতটি প্রোটন থাকে সে সংখ্যাকে ঐ মৌলের পারমাণবিক সংখ্যা বলে।
এবং মৌল দুটির প্রোটন সংখ্যা বা পারমাণবিক সংখ্যা যথাক্রমে 29 ও 30 এবং ভরসংখ্যা যথাক্রমে 64 ও 64। অর্থাৎ নিউক্লিয়ন সংখ্যা একই। নিউক্লিয়ন সংখ্যা হলো প্রোটন ও নিউট্রন সংখ্যার যোগফল। আমরা জানি, নিউট্রন সংখ্যা = ভর সংখ্যা (A) – পারমাণবিক সংখ্যা (Z)
সুতরাং এর নিউট্রন সংখ্যা = 64-29 = 35
এর নিউট্রন সংখ্যা = 64 - 30 = 34
যেহেতু, মৌল দুটির পারমাণবিক সংখ্যা বা প্রোটন সংখ্যা ভিন্ন তাই পরমাণু দুটির নিউক্লিয়ন সংখ্যা সমান হলেও, নিউট্রন সংখ্যা ভিন্ন হবে।
ফরিদের আঁকা মডেলটি রাদারফোর্ড পরমাণু মডেলকে সমর্থন করে। মডেলটির স্বীকার্যসমূহ হলো-
i. পরমাণুর কেন্দ্রস্থলে একটি ধনাত্মক চার্জ বিশিষ্ট ভারী বস্তু বিদ্যমান। এই ভারী বস্তুকে পরমাণুর কেন্দ্র বা নিউক্লিয়াস বলা হয়। পরমাণুর মোট আয়তনের তুলনায় নিউক্লিয়াসের 'আয়তন অতি নগণ্য। নিউক্লিয়াসে পরমাণুর সমস্ত ধনাত্মক চার্জ ও প্রায় সমস্ত ভর কেন্দ্রীভূত।
ii. পরমাণু বিদ্যুৎ নিরপেক্ষ। অতএব নিউক্লিয়াসের ধনাত্মক চার্জযুক্ত প্রোটন সংখ্যার সমান সংখ্যক ঋণাত্মক চার্জযুক্ত ইলেকট্রন পরমাণুর নিউক্লিয়াসকে পরিবেষ্টিত করে রাখে।
iii. সৌরজগতের সূর্যের চারদিকে ঘূর্ণায়মান গ্রহসমূহের মতো পরমাণুর ইলেকট্রনগুলো নিউক্লিয়াসের চারদিকে অবিরাম ঘুরছে। ধনাত্মক চার্জ বিশিষ্ট নিউক্লিয়াস ও ঋণাত্মক চার্জ বিশিষ্ট ইলেকট্রনসমূহের পারস্পরিক স্থির বৈদ্যুতিক আকর্ষণজনিত কেন্দ্রমুখী বল এবং ঘূর্ণায়মান ইলেকট্রনের কেন্দ্র বহির্মুখী বল পরস্পর সমান।

চিত্র: রাদারফোর্ডের পরমাণু মডেল
উদ্দীপকে বিদ্যমান ফরিদের অঙ্কিত মডেল হল রাদারফোর্ডের পরমাণু মডেল। এটি বিশ্লেষণ করলে দেখা যায়, ইলেকট্রনগুলো সর্পিলাকারে ঘুরতে ঘুরতে নিউক্লিয়াসে পতিত হচ্ছে, তাই অঙ্কিত মডেলটি একটি অস্থায়ী পরমাণু মডেল।
ম্যাক্সওয়েলের তত্ত্বানুসারে কোন চার্জযুক্ত কণা কোনো বৃত্তাকার পথে ঘুরতে থাকলে তা ক্রমাগত শক্তি বিকিরণ করবে এবং তার আবর্তন কক্ষপথের ব্যাসার্ধ ধীরে ধীরে কমতে থাকবে। সুতরাং ইলেকট্রনসমূহ ক্রমশ শক্তি হারাতে হারাতে নিউক্লিয়াসে প্রবেশ করবে। ফলে মডেলটি অর্থাৎ পরমাণুর অস্তিত্ব বিলীন হয়ে যাবে।
অর্থাৎ, রাদারফোর্ডের পরমাণু মডেল ম্যাক্সওয়েলের তত্ত্ব অনুসারে পরমাণু স্থায়ী হবে না।
কোনো মৌলের পূর্ণ নামের সংক্ষিপ্ত প্রকাশকে ঐ মৌলের প্রতীক বলা হয়।
বর্ণালি হলো বিভিন্ন বর্ণের আলোর সমাবেশ। বোর পরমাণু মডেল অনুসারে পরমাণুর মধ্যে কোনো ইলেকট্রন যখন একটি নিম্নতর কক্ষপথ থেকে উচ্চতর কক্ষপথে স্থানান্তরিত হয় তখন নির্দিষ্ট পরিমাণ শক্তি শোষণ করে। আবার যখন উচ্চতর শক্তিস্তর থেকে নিম্নতর শক্তিস্তরে স্থানান্তরিত হয় তখন নির্দিষ্ট পরিমাণ শক্তি বিকিরণ করে। বিকিরিত শক্তি আলোক শক্তিরূপে আমাদের চোখে ধরা পড়ে। এ আলোক শক্তিকে বর্ণালি হিসাবে পাওয়া যায়। এভাবে পরমাণুতে বর্ণালির সৃষ্টি হয়।
১ ক্লিকে প্রশ্ন, শীট, সাজেশন ও
অনলাইন পরীক্ষা তৈরির সফটওয়্যার!
শুধু প্রশ্ন সিলেক্ট করুন — প্রশ্নপত্র অটোমেটিক তৈরি!



