আমাদের চারপার্শ্বে বিভিন্ন পদার্থ তাপ, চাপ কিংবা একে অন্যের সংস্পর্শে এসে পরিবর্তিত হয়। পদার্থের এ পরিবর্তন দুই ধরনের হয়- কখনো হয় ভৌত পরিবর্তন, কখনো বা রাসায়নিক পরিবর্তন। ভৌত পরিবর্তনে পদার্থের বিভিন্ন অবস্থার পরিবর্তন ঘটে; কিন্তু রাসায়নিক পরিবর্তনে সম্পূর্ণ ভিন্নধর্মী নতুন পদার্থে পরিণত হয়।
যদি কোনো পদার্থের অভ্যন্তরীণ রাসায়নিক গঠনের কোনো পরিবর্তন না ঘটে শুধু বাহ্যিক অবস্থার পরিবর্তন ঘটে তা হচ্ছে ভৌত পরিবর্তন (Physical Change)। যেমন- এক টুকরো কঠিন বরফ কক্ষ তাপমাত্রায় রাখলে তা পরিবেশ থেকে তাপ গ্রহণ করে তরলে এবং আরো তাপ প্রয়োগে জলীয় বাষ্পে পরিণত হয়। অর্থাৎ, তাপের প্রভাবে পানির ৩টি অবস্থার (কঠিন, তরল, বাষ্প) শুধু পরিবর্তন ঘটে, মূল গঠনের পরিবর্তন ঘটে না- এটাই ভৌত পরিবর্তন।
কঠিন বরফ, তরল পানি ও জলীয় বাষ্প এ তিনটি পদার্থের আণবিক সংকেত । অর্থাৎ, বরফ, পানি, জলীয় বাষ্প তিনটি পদার্থ একই। শুধু তাপের প্রভাবে পানি এর ৩টি অবস্থার পরিবর্তন ঘটে যেমন তাপের সংস্পর্শে কঠিন বরফ থেকে তরলে, তরল থেকে বাষ্পে পরিণত হয়- এটাই ভৌত পরিবর্তন।
ভৌত পরিবর্তনে পদার্থের বাহ্যিক বা ভৌত অবস্থারই পরিবর্তন ঘটে, আণবিক গঠনের পরিবর্তন ঘটে না। বাহ্যিক পরিবর্তনের কারণ সরিয়ে নিলেই বস্তু পূর্বাবস্থায় ফিরে আসে। এ পরিবর্তনে অণুর গঠনের পরিবর্তন ঘটে না বলে রাসায়নিক সংযুতিরও পরিবর্তন ঘটে না। এসব বৈশিষ্ট্যের কারণে ভৌত পরিবর্তন হয়ে থাকে।

-এটি একটি ভৌত পরিবর্তন। কেননা তাপের সংস্পর্শে পানি পদার্থের শুধু ৩টি অবস্থার পরিবর্তন ঘটেছে। এক্ষেত্রে তাপের প্রভাবে কঠিন বরফ থেকে তরল পানিতে, আবার তরল পানি থেকে জলীয় বাষ্পে পরিণত হয়েছে। অন্যদিকে তাপ অপসারণে জলীয় বাষ্প থেকে তরলে আবার তরল থেকে কঠিন বরফে পরিণত হয়েছে। অর্থাৎ ভৌত পরিবর্তন ঘটেছে।
যে পরিবর্তনের ফলে সম্পূর্ণ ভিন্ন ধর্মবিশিষ্ট নতুন পদার্থে পরিণত হয়, তা হচ্ছে রাসায়নিক পরিবর্তন, (Chemical Change) | যেমন মিথেন গ্যাসকে অক্সিজেনে পোড়ালে কার্বন ডাইঅক্সাইড গ্যাস, জলীয় বাষ্প এবং তাপশক্তি উৎপন্ন করে। এক্ষেত্রে উৎপন্ন পদার্থ কার্বন ডাইঅক্সাইড, জলীয় বাষ্পের বৈশিষ্ট্য বিক্রিয়ক মিথেন থেকে সম্পূর্ণ ভিন্নধর্মী। তাই এটি একটি রাসায়নিক পরিবর্তন।
রাসায়নিক পরিবর্তনের ২টি বৈশিষ্ট্য নিম্নরূপ-
১. রাসায়নিক পরিবর্তনে অবশ্যই তাপের উদগীরণ বা শোষণ ঘটে।
২. রাসায়নিক পরিবর্তনে ভিন্ন কোনো পরমাণুর সৃষ্টি বা কোনো পরমাণুর ধ্বংস হয় না।
ক্যালসিয়াম কার্বনেট ও হাইড্রোক্লোরিক এসিডের সাথে বিক্রিয়ায় সম্পূর্ণ ভিন্নধর্মী পদার্থ কার্বন ডাইঅক্সাইড ও পানি উৎপন্ন করে। তাই এটি রাসায়নিক পরিবর্তন।
বিক্রিয়া :
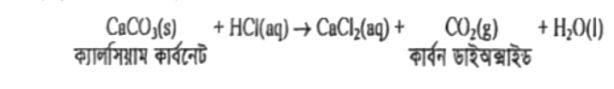
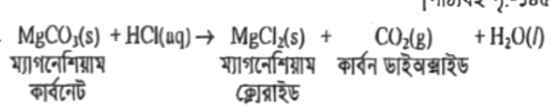
বিক্রিয়াটিতে বিক্রিয়ক থেকে সম্পূর্ণ ভিন্নধর্মী পদার্থ পদার্থ উৎপন্ন হয়েছে। তাই এটি রাসায়নিক পরিবর্তন।
ভৌত ও রাসায়নিক পরিবর্তনের মধ্যে ২টি পার্থক্য নিম্নরূপ
| ভৌত পরিবর্তন | রাসায়নিক পরিবর্তন |
| ১. ভৌত পরিবর্তনে পদার্থের অভ্যন্তরীণ রাসায়নিক গঠনের কোনো পরিবর্তন ঘটে না, শুধু বাহ্যিক অবস্থার পরিবর্তন ঘটে। | ১. রাসায়নিক পরিবর্তনে বিক্রিয়ক অণুর বন্ধন ভেঙে নতুন বন্ধন গড়ার মাধ্যমে সম্পূর্ণ ভিন্নধর্মী নতুন পদার্থ সৃষ্টি হয়। |
| ২. এটি অস্থায়ী পরিবর্তন। | ২. এটি স্থায়ী পরিবর্তন। |
মোম জ্বালালে তার কিছু অংশ শুধু ভৌত পরিবর্তনের মাধ্যমে গলে কঠিন অবস্থা হতে তরল অবস্থায় রূপান্তরিত হয় এবং ঠান্ডা হয়ে পুনরায় কঠিন অবস্থায় পরিণত হয়। একই সাথে মোমের কিছু অংশ অক্সিজেনের সাথে বিক্রিয়া করে কার্বন ডাইঅক্সাইড ও জলীয় বাষ্প উৎপন্ন করে। অর্থাৎ, মোম জ্বালানোর সময় ভৌত ও রাসায়নিক উভয় ধরনের পরিবর্তন ঘটে।
যে রাসায়নিক বিক্রিয়ায় বিক্রিয়ক পদার্থগুলো উৎপাদে পরিণত হয়, কিন্তু উৎপাদ পদার্থগুলো পুনরায় বিক্রিয়কে পরিণত হয় না তাকে বলা হয় একমুখী বিক্রিয়া। যেমন ক্যালসিয়াম কার্বনেট খোলা পাত্রে নিয়ে তাপ প্রয়োগ করলে তা তাপে বিয়োজিত হয়ে কঠিন চুন ও কার্বন ডাইঅক্সাইড গ্যাস উৎপন্ন করবে। এক্ষেত্রে অপসারিত হওয়ায়, উৎপাদ চুন থেকে কখনোই পাওয়া সম্ভব নয়। তাই এটি একমুখী বিক্রিয়া। এ বিক্রিয়ায় বিক্রিয়ক ও উৎপাদের মাঝে চিহ্ন
ব্যবহৃত হয়।
বিক্রিয়া :
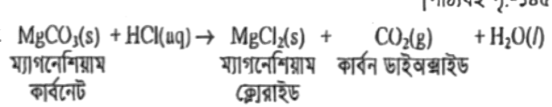
যে রাসায়নিক বিক্রিয়ায় বিক্রিয়ক পদার্থসমূহ বিক্রিয়া করে উৎপাদে পরিণত হয়; আবার উৎপাদ পদার্থগুলো বিক্রিয়া করে পুনরায় বিক্রিয়ক পদার্থে পরিণত হয়। সেটা হচ্ছে উভমুখী বিক্রিয়া। এ ধরনের বিক্রিয়ায় বিক্রিয়ক হতে উৎপাদ হওয়ার বিক্রিয়াকে সম্মুখমুখী বিক্রিয়া এবং উৎপাদ হতে বিক্রিয়কে পরিণত হওয়ার বিক্রিয়াকে বলা হয় পশ্চাৎমুখী বিক্রিয়া। এ ধরনের বিক্রিয়ায় বিক্রিয়ক ও উৎপাদের মধ্যে

বিক্রিয়াটি একটি উভমুখী বিক্রিয়া; কারণ বিক্রিয়াটিতে বিক্রিয় অ্যালকোহল ও এসিড পরস্পরের সাথে বিক্রিয়া করে এস্টার উৎপ করেছে। আবার উৎপাদ এস্টারের আর্দ্রবিশ্লেষণে অ্যালকোহল এসিড পাওয়া যায়।

দেখা যাচ্ছে, বিক্রিয়াটিতে হাইড্রোজেন (H) ও আয়োডিন পরস্পরের সাথে বিক্রিয়া করে হাইড্রোজেন আয়োডাইড (HI) উৎ করেছে। আবার উৎপাদ হাইড্রোজেন আয়োডাইড ভেঙে হাইড্রোজে ও আয়োডিনে পরিণত হয়। তাই এটি উভমুখী বিক্রিয়া।
যে রাসায়নিক বিক্রিয়ায় তাপ উৎপন্ন হয়, তাদেরকে বলা হয় তাপোৎপাদী বিক্রিয়া। যেমন: হতে উৎপাদনের সময় 92 kJ তাপ উৎপন্ন হয়। তাই এটি তাপোৎপাদী বিক্রিয়া। অর্থাৎ l
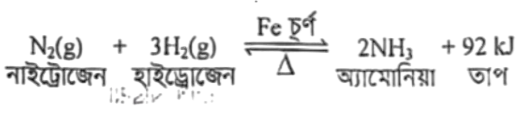
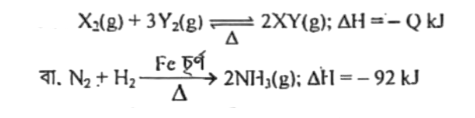
বিক্রিয়াটি একটি তাপোৎপাদী বিক্রিয়া। কেননা এ বিক্রিয়ায় ∆H এর মান খঋণাত্মক। বিক্রিয়ায় তাপ উৎপাদন হলে AIH এর মান ঋণাত্মক হয়। আর যে বিক্রিয়ায় তাপ উৎপন্ন হয়, সেটি তাপোৎপাদী বিক্রিয়া।
যে রাসায়নিক বিক্রিয়ায় তাপশক্তির শোষণ ঘটে, সেই রাসায়নিক বিক্রিয়া হচ্ছে তাপহারী বা তাপশোষী বিক্রিয়া। যেমন,। মোল ও.l মোল পরস্পরের সাথে বিক্রিয়া করে 2 মোল NO উৎপন্ন হওয়ার সময় 180 kJ তাপ শোষিত হয়। তাই এটি তাপশোষী বা তাপহারী বিক্রিয়া।
অর্থাৎ
বিক্রিয়াটি একটি উভমুখী, তাপহারী বিক্রিয়া। কেননা বিক্রিয়াটিতে বিক্রিয়ক ও উৎপাদের মাঝে '' উভমুখী চিহ্ন রয়েছে। আবার এ বিক্রিয়ায় ∆H এর মান ধনাত্মক। তাপহারী বা তাপশোষী বিক্রিয়ায় ∆H এর মান ধনাত্মক হয়। বিক্রিয়াটি সংঘটিত হতে 52 kJ তাপ শোষিত হয়েছে। তাই এটি তাপহারী বিক্রিয়া।
তাপোৎপাদী ও তাপহারী বিক্রিয়ার মধ্যে দুটি পার্থক্য হলো-
| তাপোৎপাদী বিক্রিয়া | তাপহারী বিক্রিয়া |
১. তাপোৎপাদী বিক্রিয়ায় সর্বদা তাপ উৎপন্ন হয়। ২. তাপোৎপাদী বিক্রিয়ার ১৪ এর মান ঋণাত্মক (-ve) হয়। | ১. তাপহারী বিক্রিয়ায় সর্বদা তাপ শোষিত হয়। ২. তাপহারী বিক্রিয়ার ∆H এর মান ধনাত্মক (+ve) হয়। |
রেডক্স (Redox) এর অর্থ জারণ-বিজারণ। অর্থাৎ যে রাসায়নিক বিক্রিয়ায় বিক্রিয়কসমূহের মধ্যে ইলেকট্রনের আদান-প্রদান তথা জারণ-বিজারণ ঘটে, 'তাকে বলা হয় রেডক্স বিক্রিয়া। Redox তথা জারণ-বিজারণ দুটি অর্ধাংশে বিভক্ত; যথা- জারণ অর্ধবিক্রিয়া ও বিজারণ অর্ধবিক্রিয়া।
Redox বিক্রিয়া তথা জারণ-বিজারণ বিক্রিয়ার যে অর্ধাংশে বিক্রিয়ক ইলেকট্রন ত্যাগ করে তা হচ্ছে জারণ অর্ধবিক্রিয়া। এক্ষেত্রে জারণ সংখ্যার বৃদ্ধি ঘটে। উদাহরণস্বরূপ:
জারণ অর্ধবিক্রিয়া :
ইলেকট্রন ত্যাগ, জারণ মান বৃদ্ধি+23 [জারণ বিক্রিয়া]
Redox বিক্রিয়া তথা জারণ-বিজারণ বিক্রিয়ার যে অর্ধাংশে একটি বিক্রিয়ক ইলেকট্রন গ্রহণ করে, তা হচ্ছে- বিজারণ অর্ধবিক্রিয়া।
এক্ষেত্রে জারণ-মানের হ্রাস ঘটে। উদাহরণস্বরূপ:
বিজারণ অর্ধবিক্রিয়া
ইলেকট্রন গ্রহণ; জারণ মান হ্রাস (01) [বিজারণ বিক্রিয়া]
জারণ-বিজারণ বিক্রিয়ায় যে বিক্রিয়কটি ইলেকট্রন গ্রহণ করে তা হচ্ছে জারক পদার্থ। যেমন-
বিক্রিয়াটিতে-
বিক্রিয়ক CI ইলেকট্রন গ্রহণ করেছে, তাই CI জারক পদার্থ।
জারণ-বিজারণ বিক্রিয়ায় যে বিক্রিয়কটি ইলেকট্রন ত্যাগ করে তা হচ্ছে বিজারক পদার্থ। যেমন-
বিক্রিয়াটিতে 'Mg বিক্রিয়ক ইলেকট্রন ত্যাগ করেছে। তাই Mg বিজারক পদার্থ।

জারক: জারণ ক্রিয়া যার উপস্থিতিতে ঘটে, সেটা জারক। তাই বিক্রিয়াটিতে জারক।
বিজারক : বিজারণ ক্রিয়া যার উপস্থিতিতে ঘটে, সেটা বিজারক; তাই K বিক্রিয়াটিতে বিজারক।
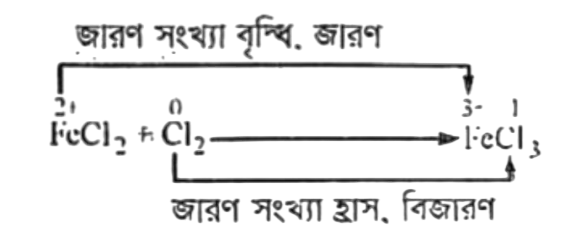
উপরিউক্ত বিক্রিয়াটিতে- বিক্রিয়ক তথা ইলেকট্রন ত্যাগ করেছে, তাই এটি বিজারক। অন্যদিকে, বিক্রিয়ক ইলেকট্রন গ্রহণ করেছে, তাই এটি জারক।
বিজারকসমূহ কোন বিক্রিয়ায় তড়িৎ ধনাত্মক মৌল বা মূলকের সংযোগ ঘটায়, ফলে ধনাত্মক মূলকের অনুপাত বৃদ্ধি পায় অথবা যৌগের অণু হতে তড়িৎ ঋণাত্মক মৌল বা মূলকের অপসারণ ঘটায়। ফলে ঋণাত্মক মূলকের অনুপাত হ্রাস পায়। এ জন্য বিজারকসমূহ জারিত হয়।
কার্বন একটি বিজারক, কারণ কপার অক্সাইড (CuO) এবং. কার্বনের বিক্রিয়ায় কপার ও কার্বন মনোক্সাইড উৎপন্ন হয়।
এ বিক্রিয়ার কপার অক্সাইড হতে তড়িৎ ঋণাত্মক অক্সিজেনের অপসারণ হয়েছে। সুতরাং কপার অক্সাইডের বিজারণ ঘটেছে। কার্বন এই বিজারণ ঘটিয়ে নিজে জারিত হয়ে কার্বন মনোক্সাইডে রূপান্তরিত হয়েছে। অর্থাৎ কার্বন বিজারক।
জারণ-বিজারণ বিক্রিয়ায় যে পরমাণু বা মূলক ইলেকট্রন বর্জন করে তাকে বিজারক বলে। একটি বিজারক। কারণ রাসায়নিক বিক্রিয়ায় - আয়ন ইলেকট্রন বর্জন করে গ্যাসে পরিণত হয়।
জারণ-বিজারণ বিক্রিয়ায় যে পরমাণু বা মূলক ইলেকট্রন বর্জন করে তাকে বিজারক বলে। একটি বিজারক। কারণ রাসায়নিক বিক্রিয়ায় আয়ন ইলেকট্রন বর্জন করে গ্যাসে পরিণত হয়।
জারণ-বিজারণ বিক্রিয়ায় যে বিক্রিয়ক ইলেকট্রন গ্রহণ করে, তাকে জারক বলে। প্রদত্ত হচ্ছে একটি জারক। কারণ এটি সর্বদা ।টি ইলেকট্রন গ্রহণ করে Na ধাতুতে পরিণত হয়। হতে ইলেকট্রন অপসারণ করতে অনেক শক্তির প্রয়োজন হয় বলে এটি হতে ইলেকট্রন ত্যাগ করা অসম্ভব। তাই এটি সর্বদা ইলেকট্রন গ্রহণ করে, অর্থাৎ এটি একটি জারক।
তড়িদদ্বার বিক্রিয়া জারণ-বিজারণ বিক্রিয়া। কারণ একটি তড়িৎ রাসায়নিক কোষ বা তড়িৎ বিশ্লেষ্য কোষ গঠনে দুটি তড়িদদ্বার যথা: অ্যানোড ও ক্যাথোড তড়িদদ্বার ব্যবহার করা হয়। অ্যানোড তড়িদদ্বারে জারণ বিক্রিয়া ঘটে এবং ক্যাথোড তড়িদ্রদ্বারে বিজারণ বিক্রিয়া ঘটে।অ্যানোড তড়িদদ্বার: জারণ-বিক্রিয়া)
ক্যাথোড তড়িদদ্বার: (বিজারণ-বিক্রিয়া)
সুতরাং, তড়িদদ্বার বিক্রিয়া জারণ-বিজারণ বিক্রিয়া।
অণু বা যৌগমূলকের মধ্যে অবস্থিত কোনো পরমাণুর ইলেকট্রন ত্যাগ করার প্রবণতাকে ধনাত্মক চিহ্নযুক্ত (+) সংখ্যা দ্বারা আবার কোনো পরমাণুর ইলেকট্রন গ্রহণ করার প্রবণতাকে ঋণাত্মক চিহ্ন (-) যুক্ত সংখ্যা দ্বারা প্রকাশ করা হয়; এই ধনাত্মক বা ঋণাত্মক চিহ্নযুক্ত সংখ্যাকেই বলা হয় জারণ সংখ্যা (Oxidation Number), যেমন; যৌগে এর জারণ মান + 2।
S এর জারণ সংখ্যা নির্ণয় :
ধরি, s এর জারণ সংখ্যা = x
তাহলে
বা,
বা
বা; 4x = 10
x =
সুতরাং S এর নির্ণেয় জারণ মান + 2.5।
সংশ্লিষ্ট বিক্রিয়া:
লবণ
উৎপন্ন লবণ- এর কেন্দ্রীয় S পরমাণুর জারণ মান = x (ধরি)
এখানে,
Na এর জারণ মান = + 1
0 = ,, ,, ,, = -2
বা,
বা,
x=+6
সুতরাং, এর কেন্দ্রীয় পরমাণুর জারণ সংখ্যা + 6।
পটাসিয়াম ডাইক্রোমেট, এর সংকেত
ধরি, কেন্দ্রীয় পরমাণু Cr এর জারণ সংখ্যা = x
আমরা জানি, K এর জারণ সংখ্যা = + 1
০ এর জারণ সংখ্যা =- 2
বা
এর জারণ সংখ্যা + 6.
পটাসিয়াম পারম্যাঙ্গানেট এর সংকেত । মনে করি যৌগের কেন্দ্রীয় পরমাণু Mn এর জারণ সংখ্যা x
তাহলে
অতএব, কেন্দ্রীয় পরমাণু Mn এর জারণ সংখ্যা + 7।
ধরি, , যৌগে Fe এর জারণ সংখ্যা = x
Ca এর জারণমান = + 2
০ এর জারণমান = - 2
বা,
বা
x = 6
সুতরাং, যৌগে Fe এর জারণমান + 6.
যৌগটির কেন্দ্রীয় পরমাণুর জারণ সংখ্যা নির্ণয় :
মনে করি যৌগের কেন্দ্রীয় পরমাণু Mn এর জারণ সংখ্যা x
তাহলে
অতএব, কেন্দ্রীয় পরমাণু Mn এর জারণ সংখ্যা + 7।
যৌগে কেন্দ্রীয় মৌল C।
H এর জারণ সংখ্যা +1 ও Cl এর জারণ সংখ্যা
ধরি, C এর জারণ সংখ্যা x.
বা,
ধরি, , যৌগে ১ এর জারণ সংখ্যা x ।
জানা আছে
এখানে
Na = + 1
S=x
O = - 2
বা,
বা,
বা, 4x = 10
জানা আছে, নিরপেক্ষ যৌগে পরমাণুসমূহের মোট জারণ সংখ্যা শূন্য (0) হয়। অর্থাৎ নিরপেক্ষ যৌগের জারণ সংখ্যা শূন্য হয়। যেহেতু HCI যৌগটি নিরপেক্ষ। তাই HCI যৌগের জারণ সংখ্যা শূন্য (0) হয়।
জানা আছে, যৌগস্থিত মৌলসমূহের জারণ সংখ্যার যোগফল শূন্য (0)।
ধরি, Mn এর জারণ মান = x
তাহলে
বা
x - 7 = 0
x = 7
সুতরাং যৌগে Mn এর জারণ মান + 7।
জানা আছে, নিরপেক্ষ যৌগে পরমাণুসমূহের মোট জারণ সংখ্যা শূন্য (0) হয়। অর্থাৎ নিরপেক্ষ যৌগ এর জারণ মান = 0। এখন, সুপার অক্সাইড যেমন এ ধরি Oএর জারণ মান x।
তাহলে
বা,
বা
সুতরাং, বলা যায়, সুপার অক্সাইডে অক্সিজেনের জারণ মান ।
ধরি, যৌগে C এর জারণ সংখ্যা = x
বা
এ, ৩ এর জারণ সংখ্যা= -2
ধরি, P এর জারণ সংখ্যা = x
সুতরাং
বা
বা
সুতরাং, এ P এর জারণ সংখ্যা +5 l
যোজনী ও জারণ সংখ্যার মধ্যে দুইটি বৈসাদৃশ্য নিম্নরূপ-
| যোজনী | জারণ সংখ্যা |
| ১. কোনো মৌলের যোজনী কখনো শূন্য হয় না। | ১. অন্যদিকে নিরপেক্ষ পরমাণু বা মুক্ত মৌলের জারণ সংখ্যা সবসময় শূন্য (০) হয়। |
| ২. যোজনী প্রকাশ করতে ধনাত্মক বা ঋণাত্মক চিহ্নের প্রয়োজন হয় না। | ২. অন্যদিকে জারণ সংখ্যা প্রকাশ করতে ধনাত্মক বা ঋণাত্মক চিহ্নের প্রয়োজন হয়। |
যোজনী ও জারণ সংখ্যা এক নয়, এর কারণ নিচে ব্যাখ্যা করা হলো:
১. যোজনীর কোনো ধনাত্মকতা বা ঋণাত্মকতা নেই। জারণ সংখ্যা ধনাত্মক ও ঋণাত্মক বা শূন্য হতে পারে।
২. মৌলের যোজনী সব সময় পূর্ণসংখ্যা। কিন্তু জারণ সংখ্যা ভগ্নাংশ' হতে পারে।।
সুতরাং, বলা যায়, জারণ সংখ্যা ও যোজনী একই বিষয় নয়।
যে রাসায়নিক বিক্রিয়ায় ইলেকট্রনের দান ঘটে তাকে জারণ বিক্রিয়া এবং যে রাসায়নিক বিক্রিয়ায় ইলেকট্রনের গ্রহণ ঘটে, তাকে বলে বিজারণ বিক্রিয়া। যেমন:
(জারণ বিক্রিয়া)
বিজারণ বিক্রিয়া)
এখানে Na এর জারণ ঘটেছে এবং CI এর বিজারণ ঘটেছে। রাসায়নিক বিক্রিয়ার জারণ যখনই ঘটবে সাথে সাথে সেখানে বিজারণও ঘটবে। অর্থাৎ জারণ-বিজারণ বিক্রিয়া যুগপৎভাবে তথা একই সাথে ঘটে।
যে জারণ-বিজারণ বিক্রিয়ায় দুই বা ততোধিক রাসায়নিক পদার্থ পরস্পরের সাথে যুক্ত হয়ে একটিমাত্র উৎপাদ উৎপন্ন করে তা হচ্ছে সংযোজন বিক্রিয়া (Addition Reaction)। যেমন: একাধিক বিক্রিয়ক তথা ফেরাস ক্লোরাইড ও ক্লোরিন পরস্পরের সাথে যুক্ত হয়ে একটিমাত্র উৎপাদ ফেরিক ক্লোরাইড উৎপন্ন করে। তাই এটি | সংযোজন বিক্রিয়া।
বিক্রিয়া:
সংযোজন বিক্রিয়া
প্রদত্ত বিক্রিয়া:

বিক্রিয়াটি একটি সংযোজন তথা সংশ্লেষণ বিক্রিয়া। কেননা দেখা যাচ্ছে, বিক্রিয়াটিতে একাধিক বিক্রিয়ক মৌল মিলে একটিমাত্র উৎপাদ তথা , যৌগ উৎপন্ন করেছে। তাই এটি সংযোজন বিক্রিয়া। আবার বিক্রিয়ক পদার্থ উভয়ই মৌলিক বলে এটি সংশ্লেষণ বিক্রিয়াও বটে।
যেসব সংযোজন বিক্রিয়ায় শুধু মৌলিক পদার্থ যুক্ত হয়ে যৌগ গঠন করে তাদেরকে বলা হয় সংশ্লেষণ বিক্রিয়া। যেমন, হাইড্রোজেন (H) ও ক্লোরিন (Cl) মৌলিক গ্যাস পরস্পরের সাথে সংযুক্ত হয়ে সংশ্লেষণ বিক্রিয়ার মাধ্যমে HCI এসিড উৎপন্ন করে। অর্থাৎ,
বিক্রিয়া:

প্রদত্ত রিক্রিয়াটি হলো:
কোনো রাসায়নিক বিক্রিয়ায় দুই বা ততোধিক মৌলিক পদার্থ যুক্ত হয়ে নতুন যৌগ গঠন করলে তাকে সংশ্লেষণ বিক্রিয়া বলে। প্রদত্ত বিক্রিয়াতে, দুইটি মৌলিক পদার্থ পরস্পরের সাথে বিক্রিয়া করে নতুন যৌগ নাইট্রিক অক্সাইড তৈরি করে। সুতরাং এটি সংশ্লেষণ বিক্রিয়া।
সংযোজন বিক্রিয়াতে দুই বা ততোধিক যৌগ বা মৌল যুক্ত হয়ে নতুন যৌগ উৎপন্ন হয়। যেমন- গ্যাস গ্যাসের সাথে বিক্রিয়া করে একটিমাত্র যৌগ HCI গ্যাস উৎপন্ন করে। অর্থাৎ,
আবার সংযোজন বিক্রিয়ায় একাধিক শুধু বিক্রিয়ক মৌল পরস্পরের সাথে যুক্ত হয়ে একটিমাত্র যৌগ উৎপন্ন করে। তাই বলা যায়, সকল সংশ্লেষণ বিক্রিয়াই সংযোজন বিক্রিয়া।
যে বিক্রিয়ায় একটি যৌগ ভেঙে একাধিক যৌগ বা মৌল উৎপন্ন হয়, তাকে বলা হয় বিয়োজন বিক্রিয়া। যেমন, ফসফরাস পেন্টাক্লোরাইডকে তাপ দিলে তা বিয়োজিত হয়ে ফসফরাস ট্রাইক্লোরাইড ও ক্লোরিন গ্যাস উৎপন্ন করে। তাই এটি বিয়োজন বিক্রিয়া!
বিক্রিয়া:
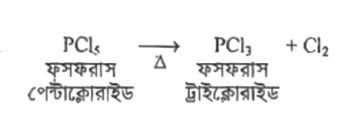
প্রদত্ত বিক্রিয়া:

উক্ত বিক্রিয়াটি একটি বিয়োজন বিক্রিয়া। কেননা বিক্রিয়ক যৌগ পানিকে তড়িৎ বিশ্লেষণ করলে একটি অণু ভেঙে একাধিক তথা দুটি অণু তে পরিণত হয়। তাই এটি বিয়োজন বিক্রিয়া।
প্রদত্ত বিক্রিয়া:

উক্ত বিক্রিয়াটি একটি বিয়োজন বিক্রিয়া। কেননা বিক্রিয়ক যৌগ পানিকে তড়িৎ বিশ্লেষণ করলে একটি অণু ভেঙে একাধিক তথা দুটি অণু তে পরিণত হয়। তাই এটি বিয়োজন বিক্রিয়া।
যে বিক্রিয়ায় অধিক সক্রিয় মৌল বা যৌগমূলক অপর কোনো কম সক্রিয় মৌল বা যৌগমূলককে প্রতিস্থাপন করে নতুন যৌগ উৎপন্ন হয়, সে বিক্রিয়াই হচ্ছে প্রতিস্থাপন বিক্রিয়া। যেমন- জিঙ্ক ধাতু সালফিউরিক এসিডের হাইড্রোজেনকে প্রতিস্থাপিত করে জিঙ্ক সালফেট ও হাইড্রোজেন গ্যাস উৎপন্ন করে। তাই এটি একটি প্রতিস্থাপন বিক্রিয়া।

প্রদত্ত বিক্রিয়া:
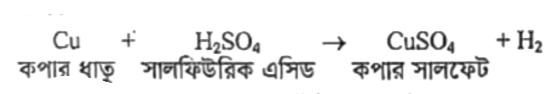
উপরিউক্ত বিক্রিয়াটি একটি প্রতিস্থাপন বিক্রিয়া। কেননা এক্ষেত্রে বিক্রিয়ক মৌল Cu ধাতু এর H কে প্রতিস্থাপিত করে কপার সালফেট ও হাইড্রোজেন গ্যাস, উৎপন্ন করেছে। তাই এটি একটি প্রতিস্থাপন বিক্রিয়া।
কোনো মৌল বা যৌগকে বাতাসের অক্সিজেনের উপস্থিতিতে 'পুড়িয়ে তার উপাদান মৌলের অক্সাইডে পরিণত করার প্রক্রিয়াকে বলা হয় দহন বিক্রিয়া (Combustion Reaction)। এ বিক্রিয়ায় সবসময় তাপ উৎপন্ন হয় এবং ইলেকট্রনের আদান-প্রদান ঘটে। যেমন: মিথেন বাতাসের অক্সিজেনের সাথে দহন বিক্রিয়ায় কার্বন ডাইঅক্সাইড গ্যাস ও পানি উৎপন্ন করে। তাই এটি দহন বিক্রিয়া।
বিক্রিয়া :

প্রদত্ত বিক্রিয়া:
বিক্রিয়াটি একটি দহন বিক্রিয়া। কেননা এক্ষেত্রে বিক্রিয়ক ধাতব মৌল ম্যাগনেশিয়াম (Mg) বাতাসের অক্সিজেন এর সাথে বিক্রিয়া করে ধাতব অক্সাইড (MgO) উৎপন্ন করেছে। তাই এটি দহন বিক্রিয়া।
কোনো মৌল বা যৌগকে বাতাসের অক্সিজেনের উপস্থিতিতে পুড়িয়ে তার উপাদান মৌলের অক্সাইডে পরিণত করার প্রক্রিয়াকে বলা হয় দহন বিক্রিয়া। দহন বিক্রিয়ায় সবসময় তাপ উৎপন্ন হয়। আবার, যে সকল রাসায়নিক বিক্রিয়ায় তাপ উৎপন্ন হয়, তাকে তাপ উৎপাদী বিক্রিয়া বলে। তাই বলা যায়, দহন বিক্রিয়া একটি তাপোৎপাদী বিক্রিয়া। যেমন,
বেনজিন
অর্থাৎ। মোল বেনজিনের সাথে যথেস্ট পরিমাণ অক্সিজেনের সম্পূর্ণ দহন করলে তাপ উৎপন্ন হয়।
যে সকল রাসায়নিক বিক্রিয়ায় ইলেকট্রনের আদান-প্রদান ঘটে না তথা জারণ সংখ্যার হ্রাস-বৃদ্ধি ঘটে না, সেসব বিক্রিয়াই হচ্ছে নন-রেডক্স বিক্রিয়া (Non-Redox)। যেমন প্রশমন বিক্রিয়া, অধঃক্ষেপণ বিক্রিয়ায় বিক্রিয়ক ও উৎপাদে জারণ সংখ্যার পরিবর্তন ঘটে না। তাই এসব বিক্রিয়া নন রেডক্স বিক্রিয়া।
বিক্রিয়া
বিক্রিয়াটিতে জারণ সংখ্যার মান অপরিবর্তিত থাকায় এটি নন-রেডক্স বিক্রিয়া।
প্রদত্ত বিক্রিয়া:
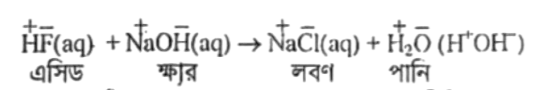
বিক্রিয়াটি একটি নন-রেডক্স তথা প্রশমন বিক্রিয়া। কেননা বিক্রিয়াটিতে জারণ মানের কোনো পরিবর্তন ঘটেনি তথা ইলেকট্রনের আদান-প্রদান ঘটেনি। তাই এটি নন-রেডক্স বিক্রিয়া। আবার বিক্রিয়াটিতে এসিড ও ক্ষার বিক্রিয়া করে লবণ ও পানি উৎপন্ন করায় এটি প্রশমন বিক্রিয়াও বটে।
একটি এসিড ও একটি ক্ষার পরস্পরের সাথে বিক্রিয়া করে প্রশমিত হয়ে লবণ ও পানি উৎপন্ন করার বিক্রিয়াকে বলা হয় প্রশমন বিক্রিয়া বা এসিড-ক্ষার বিক্রিয়া (Neutralization Reaction) যেমন, পরস্পরের সাথে বিক্রিয়া করে উৎপন্ন করায় এটি একটি প্রশমন বিক্রিয়া। অর্থাৎ,
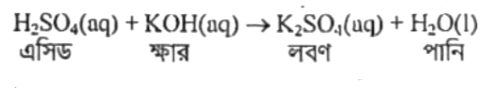
প্রদত্ত বিক্রিয়া:
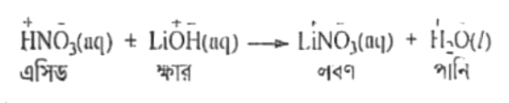
বিক্রিয়াটি একটি প্রশমন বিক্রিয়া তথা নন-রেডক্স বিক্রিয়া। কেননা দেখা যাচ্ছে, বিক্রিয়াটিতে বিক্রিয়ক এসিড ও ক্ষার (LiOH) পরস্পরের সাথে বিক্রিয়া করে লবণ ও পানি উৎপন্ন করেছে। তাই এটি প্রশমন বিক্রিয়া। আবার বিক্রিয়াটিতে বিক্রিয়ক ও উৎপাদের জারণ মানের কোনো পরিবর্তন ঘটেনি। তাই এটি নন-রেডক্স বিক্রিয়াও বটে।
রাসায়নিক বিক্রিয়ার দ্রবণে উপস্থিত যে সমস্ত আয়ন বিক্রিয়ায় অংশগ্রহণ করে না, তাকে বলা হয় দর্শক আয়ন। যেমন HCI ওKOH বিক্রিয়ার ক্ষেত্রে-
আয়নদ্বয় পরস্পরের সাথে বিক্রিয়া করে উৎপন্ন করে। কিন্তু NaCl জলীয় দ্রবণে আয়ন হিসেবে থাকে। এ আয়নদ্বয় বিক্রিয়ায় অংশগ্রহণ করে না বলে এরা দর্শক আয়ন।
যে সকল আয়ন বিক্রিয়ক ও উৎপাদে উপস্থিত থাকে কিন্তু বিক্রিয়ায় সরাসরি অংশগ্রহণ করে না তাদেরকে দর্শক আয়ন বলে। বিক্রিয়াটিতে বিক্রিয়ক ও উৎপাদ যৌগে আয়নের জারণ মানের কোনো পরিবর্তন ঘটেনি। অর্থাৎ এটি বিক্রিয়ায় সরাসরি অংশ নেয়নি। এজন্য এ বিক্রিয়ায় আয়ন হলো দর্শক আয়ন।
সাধারণত নন-রেডক্স বিক্রিয়ায় কোনো রকম ইলেকট্রনের স্থানান্তর ঘটে না। ফলে বিক্রিয়ক মৌলের জারণ সংখ্যারও কোনো পরিবর্তন ঘটে না। অর্থাৎ নন-রেডক্সক্স যেমন প্রশমন বিক্রিয়ায় জারণ মানের পরিবর্তন ঘটে না। তাই এ ধরনের বিক্রিয়ায় সাধারণত দর্শক আয়ন, উৎপন্ন হয়, যা জলীয় দ্রবণে উপস্থিত থাকে।
প্রশমন বিক্রিয়ায় এসিড ও ক্ষার পরস্পরের সাথে বিক্রিয়া করে লবণ ও পানি উৎপন্ন করে। এ বিক্রিয়ায় এসিড আয়ন, ক্ষার ' আয়ন সরবরাহ করে; যে আয়নদ্বয় পরস্পরের সাথে মিলে উৎপন্ন করে। এক্ষেত্রে উৎপন্ন করার জন্যই তাপ উৎপন্ন হয়। অর্থাৎ, প্রশমন বিক্রিয়ায় সর্বদাই তাপ উৎপন্ন হয়। আর এ বিক্রিয়ায় তাপ উৎপন্ন হয় বলেই প্রশমন বিক্রিয়াকে তাপ উৎপাদী বিক্রিয়া বলা হয়।
প্রশমন বিক্রিয়া বলতে বুঝায়, আয়নদ্বয় বিক্রিয়া করে উৎপন্ন করার বিক্রিয়া। এ ধরনের বিক্রিয়ায় সর্বদাই তাপ উৎপন্ন হয়। প্রশমন বিক্রিয়ায়। মোল পানি উৎপন্ন করতে যে পরিমাণ তাপ উৎপন্ন হয় তা হচ্ছে প্রশমন তাপ। যেমন, এসিড ও ক্ষার উভয়ই তীব্র হলে এই প্রশমন তাপের মান, ∆H = – 57.34 kJ |
যে বিক্রিয়ায় দ্রবণীয় বিক্রিয়ক পদার্থ বিক্রিয়া করে অদ্রবণীয় কঠিন উৎপাদে পরিণত হয়, তাকে বলা হয় অধঃক্ষেপণ বিক্রিয়া (Precipitation Reaction)। যেমন, সোডিয়াম ক্লোরাইডের জলীয় দ্রবণের মধ্যে সিলভার নাইট্রেটের জলীয় দ্রবণ যোগ করলে পরস্পরের সাথে বিক্রিয়া করে সিলভার ক্লোরাইডের অধঃক্ষেপ উৎপন্ন করে। তাই এটি অধঃক্ষেপণ বিক্রিয়া।
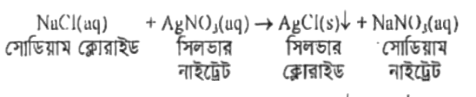
কোনো রাসায়নিক বিক্রিয়ায় বিক্রিয়ক হিসেবে পানি অন্য কোনো যৌগের সাথে বিক্রিয়া করে উৎপাদ উৎপন্ন করলে তাকে বলা আর্দ্র-বিশ্লেষণ বিক্রিয়া বা পানি বিশ্লেষণ বিক্রিয়া (Hydrolysis Reaction) যেমন বিক্রিয়াটিতে বিক্রিয়ক পানি হওয়ায় এটি আর্দ্র বিশ্লেষণ বিক্রিয়া।
আর্দ্রবিশ্লেষণ বিক্রিয়ায় অনেক ক্ষেত্রে অস্বচ্ছ দ্রবণীয় যৌগ উৎপন্ন করায় একে অধঃক্ষেপণ বিক্রিয়াও বলা হয়। যেমন-
অধঃক্ষেপ
ইলেকট্রন বিন্যাস হতে, Si এর শেষ কক্ষপথ । অরবিটাল উপস্থিত থাকার কারণে তা পানির সাথে বিক্রিয়ার সময় হাইড্রোক্সিল মূলক এ অরবিটালে স্থান দিতে পারে। ফলে বিক্রিয়ায় উৎপন্ন হয়। কিন্তু এর শেষ কক্ষপথে এ অরবিটাল না থাকায় তা মূলককে স্থান দিতে পারে না বলে বিক্রিয়াও ঘটে না।
যে সকল রাসায়নিক বিক্রিয়ায় আয়নিক যৌগগুলো কেলাস বা স্ফটিক গঠনের জন্য এক বা একাধিক পানির অণুর সাথে যুক্ত হয়, সে সকল বিক্রিয়া হচ্ছে পানিযোজন বিক্রিয়া (Hydration Reaction) যেমন, কপার সালফেট এর সাথে 5 অণু পানির অণুর যুক্ত হয়ে পেন্টাহাইড্রেট কপার সালফেট উৎপন্ন করে। তাই এটি পানিযোজন বিক্রিয়া।
বিক্রিয়া:
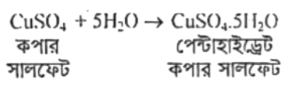
আর্দ্র-বিশ্লেষণ ও পানিযোজন বিক্রিয়ার মধ্যে ২টি পার্থক্য নিম্নরূপ:
| আর্দ্র-বিশ্লেষণ | পানিযোজন বিক্রিয়া |
| ১. আর্দ্র বিশ্লেষণ বিক্রিয়ায়-বিক্রিয়ক হিসাবে পানি অন্য কোনো যৌগের সাথে বিক্রিয়া করে উৎপাদ উৎপন্ন করে। | ১. পানিযোজন বিক্রিয়ায় আয়নিক যৌগের কেলাস গঠনের জন্য এক বা একাধিক পানির অণুর সাথে যুক্ত হলে। |
| ২. এটি এক ধরনের দ্বি-প্রতিস্থাপন বিক্রিয়া। | ২. এটি একটি সংযোজন বিক্রিয়া। |
পানিযোজন বিক্রিয়ায় আয়নিক যৌগগুলো কেলাস বা স্ফটিক গঠনের জন্য যে কয়টি পানির অণুর সাথে যুক্ত তাকে বলা হয় কেলাস পানি। যেমন, ফেরাস সালফেট এর 7 অণু পানি যুক্ত হয়ে হেন্টাহাইড্রেট ফেরাস সালফেট যৌগ উৎপন্ন করে। এক্ষেত্রে 7 অণু পানি তথা হচ্ছে কেলাস পানি।
বিক্রিয়া:
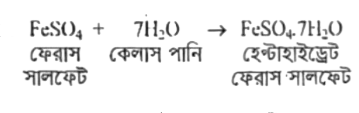
যদি দুইটি যৌগের আণবিক সংকেত একই থাকে কিন্তু গাঠনিক সংকেত ভিন্ন হয় তবে তাদেরকে পরস্পরের সমাণু বলে। একটি সমাণু থেকে অপর একটি সমাণু তৈরির প্রক্রিয়াকে বলে সমাণুকরণ বিক্রিয়া। যেমন- আণবিক সংকেতের ভিন্ন গাঠনিক সংকেত বিশিষ্ট দুটি যৌগ হলো: (অ্যামোনিয়াম সায়ানেট) ও (ইউরিয়া)। এরা পরস্পরের সমাণু। অ্যামোনিয়াম সায়ানেটকে তাপ দিলে তা সমাণুকরণ বিক্রিয়ায় ইউরিয়াতে পরিণত হয়।
সমাণুকরণ বিক্রিয়ায় যৌগের পরমাণুসমূহের পুনর্বিন্যাসের মাধ্যমে একটি সমাণু থেকে অপর সমাণু উৎপন্ন হয়। যেমন অ্যামোনিয়াম সায়ানেটকে তাপ দিলে ইউরিয়া উৎপন্ন হয়। এ প্রক্রিয়ায় অ্যামোনিয়া সায়ানেট ও ইউরিয়া পরস্পরের সমাণু।
দেখা যাচ্ছে যে, বিক্রিয়ক যৌগের পরমাণুসমূহ নিজেদের মধ্যে পুনর্বিন্যাসের মাধ্যমে NH₂CONH₂ তৈরি করেছে।
প্রভাবক, উচ্চচাপ ও তাপের প্রভাবে যখন এক বা একাধিক যৌগের অসংখ্য ক্ষুদ্র ক্ষুদ্র অণু পরস্পরের সাথে যুক্ত হয়ে একটি বৃহদাকার অণু তৈরি করে তখন তাকে বলে পলিমারকরণ বিক্রিয়া।
যেমন, ডিনাইল ক্লোরাইড যৌগের অসংখ্য অণু উচ্চ তাপ ও চাপের প্রভাবে পরস্পরের সাথে যুক্ত হয়ে বৃহৎ আণবিক ভরবিশিষ্ট নতুন যৌগ পলিভিনাইল ক্লোরাইড (PVC) গঠন করে।
বিক্রিয়া

এর সাথে লঘু -এর বিক্রিয়া ঘটে না। কারণ, লঘু সালফিউরিক এসিডের সাথে বিক্রিয়ায় ক্যালসিয়াম কার্বনেটের উপরিতলে, অদ্রবণীয় ক্যালসিয়াম সালফেটের আস্তরণ সৃষ্টি হয় বলে বিক্রিয়া শেষ পর্যন্ত অগ্রসর হতে পারে না।
(লঘু) বিক্রিয়া অসমাপ্ত।
আয়রন বাতাসের অক্সিজেন ও জলীয় বাষ্পের সাথে বিক্রিয়া করে যে আর্দ্রফেরিক অক্সাইড নামক যৌগ উৎপন্ন করে, তাকে বলা হয় মরিচা। এর রাসায়নিক সংকেত লোহাতে মরিচা পড়লে ধাতুর ক্ষয় হয়। মরিচা তৈরির বিক্রিয়া-
বিক্রিয়া
মরিচা
যে পরিবর্তনের ফলে সম্পূর্ন নতুন ধরনের এক বা একাধিক 'বস্তু সৃষ্টি হয়, তাকে বলা হয় রাসায়নিক পরিবর্তন। এক টুকরো লোহাকে অনেকদিন আর্দ্র বাতাসে বা উন্মুক্ত স্থানে রেখে দিলে তার উপর বাতাসের অক্সিজেন ও জলীয় বাষ্পের বিক্রিয়ায় পানিযুক্ত ফেরিক অক্সাইড উৎপন্ন হয়, যা মরিচা নামে পরিচিত। উৎপন্ন পদার্থ তথা মরিচার ধর্ম লোহা, অক্সিজেন ও পানি হতে সম্পূর্ণ ভিন্ন। সুতরাং বলা যায়, লোহায় মরিচা পড়া একটি রাসায়নিক পরিবর্তন।
কপার (Cu) এর দ্রব্যাদির ক্ষয় হয় না। কারণ Cu এর দ্রব্যাদি বাতাসের অক্সিজেনের সংস্পর্শে আসলে প্রথমে এর উপর CuO এর একটি আস্তরণ পড়ে। পরবর্তীতে বাতাসের অক্সিজেন উক্ত আস্তরণ ভেদ করে Cu এর সংস্পর্শে আর আসতে পারে না। ফলে আর বিক্রিয়া সংঘটিত হয় না। এজন্য Cu এর দ্রব্যাদির ক্ষয় হয় না।
মৌমাছি পোকার কামড়ের ক্ষতস্থানে পোকার শরীর থেকে যে বিষ প্রবেশ করে তাতে অম্লীয় উপাদান থাকে। মানুষ পোকার কামড়ের জ্বালাযন্ত্রণা নিবারণ করার জন্য ক্ষতস্থানে চুন ব্যবহার করে। কারণ, চুন ক্ষারকধর্মী পদার্থ। এটা অম্লীয় উপাদানের সাথে প্রশমন বিক্রিয়া করে। তাই মৌমাছি পোকার কামড়ের ক্ষতস্থানে চুন প্রয়োগ করা হয়।
শ্বসন প্রক্রিয়ায় দেহের প্রতিটি কোষে শক্তি উৎপন্ন হয়। শ্বসন প্রক্রিয়ায় মূলত গ্লুকোজ অণু অক্সিজেন অণু দ্বারা জারিত হয়ে কার্বন ডাইঅক্সাইড গ্যাস, পানি ও শক্তি উৎপন্ন করে।
বিক্রিয়া

এন্টাসিড হলো এর মিশ্রণ। আমাদের দেহে এসিডিটি বেড়ে গেলে এন্টাসিড জাতীয় ওষুধ খাওয়া হয়। এ ওষুধ অতিরিক্ত এসিড (HCI) এর এসিডিটিকে প্রশমিত করে। ফলে এসিডিটি থেকে মুক্তি পাওয়া যায়।
মানুষের শরীরের বিপাক ক্রিয়ায় অনেকের অতিরিক্ত HCI তৈরি হয়। অতিরিক্ত HCI কে প্রশমিত করার জন্য রোগীকে ডাক্তার এন্টাসিড জাতীয় ওষুধ খাওয়ার পরামর্শ দেন। এন্টাসিড হচ্ছে এর মিশ্রণ। এই স্ফারক দুটি অতিরিক্ত HCI কে প্রশমিত করে এবং রোগী এসিডিটি থেকে মুক্তি পান। এন্টাসিডের বিক্রিয়া নিম্নরূপ-
বিক্রিয়া
প্রাকৃতিক গ্যাসে বেশির ভাগই মিথেন থাকে। মিথেন গ্যাসকে অক্সিজেন পোড়ালে কার্বন ডাইঅক্সাইড, জলীয় বাষ্প ও তাপশক্তি উৎপন্ন হয়।

লোহায় জং ধরে। কারণ লোহাকে দীর্ঘদিন মুক্ত অবস্থায় রেখে দিলে বাতাসের অক্সিজেন ও জলীয় বাষ্পের সাথে বিক্রিয়া করে আর্দ্র ফেরিক অক্সাইড উৎপন্ন করে, যা জং নামে পরিচিত। জং ঝাঁঝরা জাতীয় পদার্থ হওয়ায় এর ভিতর দিয়ে রাতাসের অক্সিজেন এবং জলীয় বাষ্প ঢুকে লোহার পৃষ্ঠকে ক্রমাগত ক্ষয় করতে থাকে।
বিক্রিয়া:
জং
লোহার উপর মরিচা পড়া নিম্নোপায়ে রোধ করা যায়-
১. ধাতব আয়রনকে বায়ু ও পানির সংস্পর্শ থেকে দূরে রেখে।
২. ধাতব আয়রনের উপর রঙের প্রলেপ দিয়ে।
৩. আয়রন ধাতুর উপর গ্যালভানাইজিং, টিন প্লেটিং, তড়িৎ প্রলেপন-এর যেকোনো একটি প্রক্রিয়া সম্পাদন করে।
মরিচার ক্ষয় হতে লোহা জাতীয় দ্রব্যকে সুরক্ষিত করার ২টি উপায় হলো-
১. লোহার তৈরি দ্রব্যাদির উপর রং দিয়ে প্রলেপ দেওয়া।
২. লোহার তৈরি দ্রব্যাদির উপর তড়িৎবিশ্লেষণের মাধ্যমে লোহা অপেক্ষা কম সক্রিয় ধাতুর ইলেকট্রোপ্লেটিং করা।
তড়িৎবিশ্লেষণ প্রক্রিয়ায় কোনো ধাতুর উপর জিংক (Zn) ধাতুর প্রলেপ দেওয়াকে বলা হয় গ্যালভানাইজিং। যেমন, লোহার তৈরি দ্রব্যের উপর Zn ধাতুর প্রলেপ তথা গ্যালভানাইজিং করে মরিচার ক্ষয় থেকে রক্ষা করা যায়।
তড়িৎবিশ্লেষণ প্রক্রিয়ায় কোনো ধাতুর উপর টিন (Sn) ধাতুর প্রলেপ দেওয়াকে বলা হয় টিন প্লেটিং। যেমন লোহার তৈরি দ্রব্যের উপর টিন (Sn) ধাতুর ইলেকট্রোপ্লেটিং তথা টিন প্লেটিং করে মরিচার ক্ষয় থেকে রক্ষা করা যায়।
তড়িৎবিশ্লেষণ প্রক্রিয়ায় একটি ধাতুর উপর অন্য একটি ধাতুর প্রলেপ দেওয়ার প্রক্রিয়াই হচ্ছে ইলেকট্রোপ্লেটিং। লোহার তৈরি দ্রব্যাদির উপর লোহা অপেক্ষা কম সক্রিয় অপর একটি ধাতুর প্রলেপ দিয়ে ইলেকট্রোপ্লেটিং করা হয়। ফলে লোহার দ্রব্যটি বাতাসের সংস্পর্শে আসতে পারে না। আর তাই মরিচাও পড়তে পারে না।
বর্ষাকালে বাড়ির আঙ্গিনা পিচ্ছিল হলে বালু দেওয়া হয়। এর কারণ বর্ষাকালে বাড়ির আঙ্গিনা পিচ্ছিলধর্মী পদার্থ জমা হয়, যা মূলত ক্ষারধর্মী। এ সমস্যা দূর করতে এতে অম্লধর্মী পদার্থ বালু যোগ করা হয়। ফলে প্রশমন বিক্রিয়ার মাধ্যমে পিচ্ছিলতা দূর হয়ে যায়।
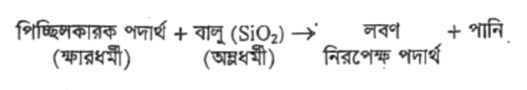
লোহার তৈরি সুচ যা দ্বারা সেলাই করা হয়, একে নারিকেল তেলের ভিতর ডুবিয়ে রাখা হয়। ফলে সুচ, বাতাসের অক্সিজেন ও জলীয় বাষ্পের সংস্পর্শেও আসতে পারে না। আর তাই রাসায়নিক বিক্রিয়াও ঘটাতে পারে না। ফলে সুচটি ক্ষয়ও হয় না। এভাবেই লোহার তৈরি সুচে মরিচা পড়া রোধ করা যায়।
একক সময়ে যে পরিমাণ বিক্রিয়ক উৎপাদে পরিণত হয় তাকে বিক্রিয়ার হার বা বিক্রিয়ার গতিবেগ বলা হয়। বিভিন্ন রাসায়নিক বিক্রিয়া সম্পন্ন হতে বিভিন্ন সময় নেয়। যে বিক্রিয়া সংঘটিত হতে অল্প সময় নেয়, সে বিক্রিয়ার হার বেশি। আর যে বিক্রিয়া সম্পন্ন হতে বেশি সময় নেয়, সে বিক্রিয়ার গতিবেগ বা হার কম।
প্রতি একক সময়ে বিক্রিয়কের ঘনমাত্রা হ্রাস ও উৎপাদের ঘনমাত্রা বৃদ্ধির পরিমাণ হলো বিক্রিয়ার হার। বিক্রিয়ার হার সাধারণত নিচের বিষয়গুলোর উপর নির্ভরশীল। যেমন-
(i) তাপমাত্রা, (ii) বিক্রিয়কের পৃষ্ঠতলের ক্ষেত্রফল, ঘনমাত্রা,(iii) বিক্রিয়কের (iv) বিক্রিয়ায় ব্যবহৃত প্রভাবক।
লা-শাতেলিয়ার নীতিটি হচ্ছে- "কোনো বিক্রিয়ার সাম্যাবস্থায় থাকাকালীন যদি ভাপ, চাপ, ঘনমাত্রা, ইত্যাদি পরিবর্তন করা হয় তবে সাম্যের অবস্থান এমনভাবে পরিবর্তিত হয় যেন তাপ, চাপ, ঘনমাত্রা ইত্যাদির পরিবর্তনের ফলাফল প্রশমিত হয়।"
তাপ, চাপ কিংবা ঘনমাত্রার প্রভাবে সাম্যাবস্থার কী ধরনের পরিবর্তন হয় লা-শাতেলিয়ার নীতির মাধ্যমে সেটি খুব সহজে ব্যাখ্যা করা যায়। অর্থাৎ, উভমুখী বিক্রিয়ার সাম্যাবস্থায় উৎপাদের পরিমাণ বৃদ্ধি বা হ্রাস লা-শাতেলিয়ার নীতি দ্বারা নিয়ন্ত্রিত হয়।
রাসায়নিক সাম্যাবস্থা কী ব্যাখ্যা কর।
উত্তর: জানা আছে, বিক্রিয়কের ঘনমাত্রা বৃদ্ধির সঙ্গে বিক্রিয়ার বেগ বৃদ্ধি পায়। অতএব, একটি উভমুখী বিক্রিয়ার শুরুতে সম্মুখ বিক্রিয়ার বেগ সবচেয়ে বেশি থাকবে এবং বিপরীত বিক্রিয়ার বেগ কম থাকবে। সময়ের সাথে সম্মুখ বিক্রিয়ার বেগ কমতে থাকবে এবং বিপরীত বিক্রিয়ার বেগ বাড়তে থাকবে। একসময় সম্মুখ ও বিপরীত বিক্রিয়ার বেগ সমান হবে। এ অবস্থাই হচ্ছে রাসায়নিক সাম্যাবস্থা।
তাপমাত্রা বিক্রিয়ার হারকে অধিক মাত্রায় পরিবর্তন করে। সাধারণত প্রতি 10°C তাপমাত্রা বাড়ার সাথে বিক্রিয়ার হার 2 থেকে 3 গুণ বেড়ে, যায়। তাপমাত্রা বৃদ্ধি করলে বিক্রিয়ক অণুর গতিশক্তি এবং গতিবেগ বৃদ্ধি পায়। এর ফলে একক সময়ে নির্দিষ্ট আয়তনে। অবস্থিত কণাগুলোর মধ্যে সংঘর্ষের হার বৃদ্ধি পায়। সংঘর্ষের হার বৃদ্ধি পেলে বিক্রিয়ার হারও বেড়ে যায়।
বিক্রিয়াটিতে বিক্রিয়কের মোল সংখ্যা 2 এবং উৎপাদের মোল সংখ্যা 4+1=5। সুতরাং বিক্রিয়াটি আয়তন বৃদ্ধির মাধ্যমে ঘটে। এজন্য কম চাপে এর বিয়োজন অধিক হয়। ফলে বিক্রিয়ার সাম্যাবস্থা ডানদিকে সরে গিয়ে উৎপাদ এর পরিমাণ বৃদ্ধি করে। অপরদিকে, চাপ বৃদ্ধি করলে এর বিয়োজন হ্রাস পায়। ফলে সাম্যাবস্থা বাম দিকে সরে গিয়ে উৎপাদের পরিমাণ কমে যায়।
বিক্রিয়কসমূহের ঘনমাত্রা বৃদ্ধির সাথে সাথে বিক্রিয়ার গতি বাড়তে থাকে।
ঘনমাত্রা বৃদ্ধির সাথে সাথে বিক্রিয়ক অণুসমূহের পরিমাণ বৃদ্ধি পায়।
অধিক বিক্রিয়কসমূহের উপস্থিতির কারণে বিক্রিয়কসমূহের মধ্যে সহজেই সংঘর্ষ ঘটে এবং বিক্রিয়া দ্রুত সম্পন্ন হয়।
বিক্রিরকসমূহের ঘনমাত্রা বৃদ্ধির সাথে সাথে বিক্রিয়ার গতি বাড়তে থাকে।
ঘনমাত্রা বৃদ্ধির সাথে সাথে বিক্রিয়ক অণুসমূহের পরিমাণ বৃদ্ধি পায়।
অধিক বিক্রিয়কসমূহের উপস্থিতির কারণে বিক্রিয়কসমূহের মধ্যে সহজেই সংঘর্ষ ঘটে এবং বিক্রিয়া দ্রুত সম্পন্ন হয়।
যদি কোনো পদার্থের অভ্যন্তরীণ রাসায়নিক গঠনের কোনো পরিবর্তন না ঘটে, শুধু বাহ্যিক অবস্থার পরিবর্তন ঘটে তাকেই ভৌত পরিবর্তন (Physical Change) বলে।
যে পরিবর্তনের ফলে সম্পূর্ণ ভিন্ন ধর্মবিশিষ্ট নতুন পদার্থে পরিণত হয়, তাকে রাসায়নিক পরিবর্তন বলে।
মোম জ্বালানোর সময় ভৌত ও রাসায়নিক উভয় ধরনের পরিবর্তন ঘটে।
যে রাসায়নিক বিক্রিয়ায় বিক্রিয়ক পদার্থ বিক্রিয়া করে উৎপাদে পরিণত হয় আবার উৎপাদ পদার্থগুলো বিক্রিয়া করে পুনরায় বিক্রিয়ক পদার্থে পরিণত হয় সে বিক্রিয়াকে উভমুখী বিক্রিয়া বলা হয়।
যে রাসায়নিক বিক্রিয়ায় তাপ উৎপন্ন হয় তাদের তাপ উৎপাদী বিক্রিয়া বলে।
যে সকল পদার্থ নিয়ে রাসায়নিক বিক্রিয়া শুরু করা হয় সেই সকল পদার্থকে বিক্রিয়ক বলা হয়।
যে রাসায়নিক বিক্রিয়ায় তাপশক্তির শোষণ ঘটে সেই রাসায়নিক বিক্রিয়াকে তাপহারী বিক্রিয়া বলে।
যে বিক্রিয়ায় কোনো পরমাণুর ইলেকট্রনের দান ঘটে, অর্থাৎ ঐ পরমাণুর ধনাত্মক চার্জের সংখ্যা বৃদ্ধি পায় বা ঋণাত্মক চার্জের সংখ্যা হ্রাস পায় সেই বিক্রিয়াকে জারণ বিক্রিয়া বলে।
জারণ-বিজারণ বিক্রিয়ায় যে বিক্রিয়কটি ইলেকট্রন গ্রহণ করে তাকে জারক পদার্থ বলে।
মুক্ত মৌলের জারণ সংখ্যা শূন্য।
যৌগ গঠনের সময় কোনো মৌল যত সংখ্যক ইলেকট্রন বর্জন করে ধনাত্মক আয়ন উৎপন্ন করে অথবা যত সংখ্যক ইলেকট্রন গ্রহণ করে ঋণাত্মক আয়ন উৎপন্ন করে তাকে মৌলের জারণ সংখ্যা বলে।
নিরপেক্ষ মৌলের জারণ সংখ্যা শূন্য (০)।
কোনো অধিক সক্রিয় মৌল বা যৌগমূলক অপর কোনো কম সক্রিয় মৌল বা যৌগমূলককে প্রতিস্থাপন করে নতুন যৌগ উৎপন্ন করার প্রক্রিয়াকে প্রতিস্থাপন বিক্রিয়া বলে।
যে বিক্রিয়ায় কোনো যৌগ তার উপাদান মৌলসমূহের প্রত্যক্ষ সংযোগে উৎপন্ন হয় তাকে সংশ্লেষণ বিক্রিয়া বলে।
যে রাসায়নিক বিক্রিয়ায় বিক্রিয়ক পদার্থগুলো উৎপাদে পরিণত হয় কিন্তু উৎপাদ পদার্থগুলো পুনরায় বিক্রিয়কে পরিণত হয় 'না তাকে একমুখী বিক্রিয়া বলে।
AH দ্বারা বিক্রিয়ায় তাপীয় পরিবর্তনকে বুঝানো হয়।
জারণ-বিজারণ বিক্রিয়ায় যে বিক্রিয়ক ইলেকট্রন বর্জন করে তাকে বিজারক বলে।
যে বিক্রিয়ায় বিক্রিয়কসমূহের মধ্যে ইলেকট্রনের আদান-প্রদান ঘটে তাকে রেডক্স (Redox) বিক্রিয়া বলে।
এ অক্সিজেনের জারণ সংখ্যা-।
যৌগে ০ এর জারণ মান -
যে বিক্রিয়ায় দুই বা ততোধিক যৌগ বা মৌল যুক্ত হয়ে নতুন যৌগ উৎপন্ন করে, সে বিক্রিয়াকে সংযোজন বিক্রিয়া বলে।
যে বিক্রিয়ায় এসিড ও ক্ষার পরস্পরের সাথে বিক্রিয়া করে - লবণ ও পানি উৎপন্ন করে, তাকে প্রশমন বিক্রিয়া বলে।
কোনো মৌল বা যৌগকে বাতাসের অক্সিজেনের উপস্থিতিতে পুড়িয়ে তার উপাদান মৌলের অক্সাইডে পরিণত করার প্রক্রিয়াকে দহন বিক্রিয়া বলে।
যে বিক্রিয়ায় দ্রবণীয় বিক্রিয়ক পদার্থ বিক্রিয়া করে অদ্রবণীয় কঠিন উৎপাদে পরিণত হয় তাকে অধঃক্ষেপণ বিক্রিয়া বলে।
যে বিক্রিয়ায় দ্রবণীয় বিক্রিয়ক পদার্থ বিক্রিয়া করে অদ্রবণীয় কঠিন উৎপাদে পরিণত হয় তাকে অধঃক্ষেপণ বিক্রিয়া বলে।
যে বিক্রিয়ায় দ্রবণীয় বিক্রিয়ক পদার্থ বিক্রিয়া করে অদ্রবণীয় কঠিন উৎপাদে পরিণত হয় তাকে অধঃক্ষেপণ বিক্রিয়া বলে।
যেসব আয়ন রাসায়নিক বিক্রিয়াকালে জারক ও বিজারকরূপে ক্রিয়া করে না অর্থাৎ বিক্রিয়াকালে যেসব আয়নের জারণ সংখ্যার পরিবর্তন হয় না তাদের দর্শক আয়ন বলে।
বদ্ধপাত্রে চুনাপাথরকে তাপ দিলে উভমুখী তাপীয় বিয়োজন ঘটে এবং এতে ক্যালসিয়াম অক্সাইড ও কার্বন ডাই অক্সাইড উৎপন্ন হয়।
উভমুখী বিক্রিয়ায় বিক্রিয়ক হতে উৎপাদ হওয়ার বিক্রিয়াকে সম্মুখমুখী বিক্রিয়া বলে।
কক্ষ তাপমাত্রায় এসিড ও ক্ষারের বিক্রিয়ায় লবণ ও পানি উৎপন্ন হতে যে তাপের উদ্ভব হয় তাকে প্রশমন তাপ বলে।
প্রশমন বিক্রিয়া সম্পূর্ণ হলে pH মান 7 হয়।
যে বিক্রিয়ায় কোনো পরমাণুর ইলেকট্রনের গ্রহণ ঘটে অর্থাৎ ঐ পরমাণুর ধনাত্মক চার্জের সংখ্যা হ্রাস পায় বা ঋণাত্মক চার্জের সংখ্যা "বৃদ্ধি পায় সে বিক্রিয়াকে বিজারণ বিক্রিয়া বলে।
ইলেকট্রন স্থানান্তরের মাধ্যমে সংযোজন, বিযোজন, প্রতিস্থাপন, দহন প্রভৃতি বিক্রিয়া সংঘটিত হয়।
রেডক্স (Redox) শব্দটি বিজারণ, Reduction- এর. Red এবং জারণ; Oxidation-এর ox নিয়ে গঠিত। অর্থাৎ রেডক্স অর্থ জারণ-বিজারণ।
জারক পদার্থ- অক্সিজেন ক্লোরিন বিজারক পদার্থ- হাইড্রোজেন , সোডিয়াম ।
এ S এর জারণ সংখ্যা 2.5 l
অ্যালডিহাইড জারিত হলে জৈব এসিড তৈরি হয়।
সিলভার ক্লোরাইডের অধঃক্ষেপ পড়ে।
যে বিক্রিয়ায় আয়নিক যৌগ কেলাস গঠনের সময় এক বা একাধিক সংখ্যক পানির অণুর সাথে যুক্ত হয় তাকে পানিযোজন বিক্রিয়া বলে।
যে বিক্রিয়ায় দুই অংশ পানির বিপরীত আধান বিশিষ্ট দুই অংশের সাথে যুক্ত হয়ে যৌগ উৎপন্ন করে, তাকে বলা হয় আর্দ্রবিশ্লেষণ বিক্রিয়া।
আয়নিক যৌগের কেলাস গঠনের সময় যুক্ত পানিকে কেলাস পানি বলে।
যদি দুটি যৌগের আণবিক সংকেত একই থাকে কিন্তু গাঠনিক সংকেত ভিন্ন হয় তবে তাদেরকে পরস্পরের সমাণু বলা হয় এবং একটি সমাণু থেকে অপর একটি সমাণু তৈরির প্রক্রিয়াকে সমাণুকরণ বিক্রিয়া বলে।
কোনো রাসায়নিক বিক্রিয়ায় যৌগের পরমাণুসমূহের পুনর্বিন্যাসের মাধ্যমে একটি সমাণু থেকে অপর সমাণু উৎপন্ন হলে তাকে সমাণুকরণ বিক্রিয়া বা পুনর্বিন্যাস বিক্রিয়া বলে।
যদি দুটি যৌগের আণবিক সংকেত একই থাকে কিন্তু গাঠনিক সংকেত ভিন্ন হয় তবে তাদেরকে পরস্পরের সমাণু বলা হয়।
প্রভাবক, উচ্চচাপ ও তাপের প্রভাবে যখন এক বা একাধিক যৌগের অসংখ্য ক্ষুদ্র ক্ষুদ্র অণু পরস্পরের সাথে যুক্ত হয়ে একটি বৃহদাকার অণু তৈরি করে তখন তাকে পলিমারকরণ বিক্রিয়া বলে।
বিশুদ্ধ লোহা, জলীয় বাষ্প ও বায়ুর অক্সিজেন রাসায়নিক বিক্রিয়ার মাধ্যমে লোহার যে অক্সাইড গঠন করে তাকে মরিচা বলে।
মরিচার সংকেত হলো
একক সময়ে যে পরিমাণ বিক্রিয়ক উৎপাদে পরিণত হয় তাকে বিক্রিয়ার হার বলে।
রাসায়নিক সাম্যাবস্থা হলো একটি গতিশীল অবস্থা যে অবস্থায় কোনো উভমুখী বিক্রিয়ার সম্মুখমুখী বিক্রিয়ার হার পশ্চাৎমুখী বিক্রিয়ার হারের সমান হয়।
লা-শাতেলিয়ার নীতিটি হচ্ছে- "কোনো বিক্রিয়ার সাম্যাবস্থায় থাকাকালীন যদি তাপ, চাপ, ঘনমাত্রা ইত্যাদি পরিবর্তন করা হয় তবে = সাম্যের অবস্থান এমনভাবে পরিবর্তিত হয় যেন তাপ, চাপ, ঘনমাত্রা ইত্যাদির পরিবর্তনের ফলাফল প্রশমিত হয়।
প্রতিটি রাসায়নিক পদার্থ একাধিক মৌল দ্বারা গঠিত l
পদার্থের দুই ধরনের পরিবর্তন হয় l
0 °C তাপমাত্রায় পানি বরফে পরিণত হয় l
পদার্থের শুধু বাহ্যিক পরিবর্তন ঘটলে তাকে ভৌত পরিবর্তন বলে l
বরফপানি বাষ্প : প্রক্রিয়াটি কী ধরনের পরিবর্তন ভৌত পরিবর্তনl
এর কঠিন অবস্থা বরফ l
পানির স্ফুটনাংক 100 °C l
পদার্থের অভ্যন্তরীণ ও বাহ্যিক পরিবর্তন ঘটে সম্পূর্ণ ভিন্নধর্মী পদার্থের পরিণত হলে তাকে রাসায়নিক পরিবর্তন বলে l
পুরাতন বন্ধনের ভাঙন এবং নতুন বন্ধন গঠন মূলত রাসায়নিক পরিবর্তন ধরনের পরিবর্তন l
প্রাকৃতিক গ্যাসের প্রধান উপাদান মিথেন
মিথেন গ্যাসের দহন বলতে অক্সিজেনের সাথে বিক্রিয়া বুঝায় l
মিথেন গ্যাসের দহন রাসায়নিক পরিবর্তন ধরনের পরিবর্তন l
ক্যালসিয়াম কার্বনেট ও হাইড্রোক্লোরিক এসিডের বিক্রিয়া রাসায়নিক পরিবর্তন ধরনের পরিবর্তন l
ক্যালসিয়াম কার্বনেট ও হাইড্রোক্লোরিক এসিডের বিক্রিয়ায় কার্বন ডাইঅক্সাইড গ্যাসীয় পদার্থ উৎপন্ন হয় l
ক্যালসিয়াম কার্বনেট ভেঙে চুন ও কার্বন ডাইঅক্সাইড উৎপন্ন হয় l
বিক্রিয়ার দিকের ভিত্তিতে রাসায়নিক বিক্রিয়া দুই প্রকার l
বিক্রিয়াটি একমুখী ধরনের বিক্রিয়া l
চুনের সংকেত CaO l
A B বিক্রিয়াটি একমুখী ধরনের l
A+BC+ D; বিক্রিয়াটি উভমুখী ধরনেরl
উভমুখী বিক্রিয়ায় বিক্রিয়ক হতে উৎপাদ হওয়ার বিক্রিয়াকে সম্মুখমুখী বিক্রিয়া বলে l
উভমুখী বিক্রিয়ায় বিক্রিয়ক ও উৎপাদের মধ্যে বিপরীতমুখী দুটি অর্ধ তীর চিহ্ন () চিহ্ন ব্যবহার করা হয় l
বিক্রিয়ায় A যৌগটি l
বিক্রিয়াটি উভমুখী ধরনের l
সাধারণত , এর বিয়োজন বিক্রিয়া খোলা পাত্রে সংঘটিত হলে বিক্রিয়া একমুখী ধরনের হয় l
তাপের পরিবর্তনের ভিত্তিতে রাসায়নিক বিক্রিয়া দুই প্রকারl
তাপোৎপাদী বিক্রিয়ায় তাপের তাপ উৎপন্ন হয় ধরনের পরিবর্তন হয় l
তাপহারী বিক্রিয়ায় তাপের তাপশক্তির শোষণ ঘটে ধরনের পরিবর্তন হয় l
নাইট্রোজেন ও হাইড্রোজেনের বিক্রিয়ায় অ্যামোনিয়া উৎপাদনে প্রয়োজনীয় তাপমাত্রা
l
বিক্রিয়ায় প্রয়োজনীয় বায়ুচাপl
নাইট্রোজেন ও হাইড্রোজেনের বিক্রিয়ায় অ্যামোনিয়া উৎপাদনে প্রভাবক হিসেবে Fe মৌল ব্যবহৃত হয় l
এবংএর বিক্রিয়ার মাধ্যমে 2 মোল অ্যামোনিয়া উৎপাদনে বিক্রিয়া তাপের পরিমাণ l
মোল অ্যামোনিয়া উৎপাদনে 2 মোল মোল হাইড্রোজেন প্রয়োজন l
একটি রাসায়নিক বিক্রিয়া সম্পন্ন হতে তাপের যে পরিবর্তন হয় তাকে বিক্রিয়া তাপ বলে l
রাসায়নিক বিক্রিয়ায় তাপ উৎপাদন হলে ∆H এর মান ঋণাত্মক রূপ হয় l
তাপশোষী বিক্রিয়ায় ∆H এর মান ধনাত্মক রূপ l
যে রাসায়নিক বিক্রিয়ায় তাপশক্তির শোষণ ঘটে তাকে তাপহারী বিক্রিয়া বলে l
নাইট্রোজেন ও অক্সিজেনের বিক্রিয়ায় 2 মোল নাইট্রিক অক্সাইড উৎপাদনের বিক্রিয়া তাপশোষী বিক্রিয়া ধরনের বিক্রিয়া l
বিক্রিয়ায় ∆H এর মান l
ইলেকট্রন স্থানান্তরের উপর ভিত্তি করে রাসায়নিক বিক্রিয়াকে দুই ভাগে করা যায় l
রেডক্স (Redox) অর্থ জারণ-বিজারণl
জারণ-বিজারণ বিক্রিয়ায় বিক্রিয়কসমূহের মধ্যে ইলেকট্রন আদান-প্রদান ঘটে l
জারণ প্রক্রিয়ায় ইলেকট্রন ত্যাগ ঘটে l
বিজারণ প্রক্রিয়ায় ইলেকট্রন গ্রহণ ঘটে l
যে বিক্রিয়ক ইলেকট্রন ত্যাগ করে তাকে বিজারক বলে l
বিক্রিয়ায় জারক পদার্থ ইলেকট্রন গ্রহণ করেl
বিক্রিয়ায় বিজারক Na l
বিক্রিয়ায় জারক
জারণ বিক্রিয়ায় ধনাত্মক চার্জের সংখ্যার বৃদ্ধি পায় পরিবর্তন ঘটে l
ঋণাত্মক চার্জের সংখ্যা বৃদ্ধি পায় বিজারণ বিক্রিয়ায় l
বিক্রিয়াটি বিজারণ ধরনের l
অণু, বা যৌগমূলকের মধ্যস্থিত কোনো পরমাণুর ধনাত্মক
বা ঋণাত্মক চিহ্নযুক্ত সংখ্যাকে জারণ সংখ্যা বলে l
একই পরমাণু দিয়ে গঠিত অণুতে সংশ্লিষ্ট পরমাণুসমূহের জারণ সংখ্যা শূন্য (0)l
অণুতে ক্লোরিন পরমাণুর জারণ সংখ্যা শূন্য (0) l
এর জারণ সংখ্যা +2 l
HCI এ CI এর জারণ সংখ্যা l
ধাতুসমূহের জারণ সংখ্যা ধনাত্মক হয় l
নিরপেক্ষ পরমাণু বা মুক্ত মৌলের জারণ সংখ্যা শূন্য (0) l
ক্ষারধাতুসমূহের জারণ সংখ্যা +1 l
মৃৎক্ষার ধাতুসমূহের জারণ সংখ্যা l
যৌগে Mg এর জারণ সংখ্যা +2 l
ধাতব হাইড্রাইডে হাইড্রোজেনের জারণ সংখ্যা -1
ধাতব হ্যালাইডে হ্যালোজেনের জারণ সংখ্যা -1 l
যৌগে H এর জারণ সংখ্যা -1 l
পার-অক্সাইডে অক্সিজেনের জারণ সংখ্যা -1 l
যৌগে অক্সিজেনের জারণ সংখ্যা -1 l
সুপার অক্সাইডে অক্সিজেনের জারণ সংখ্যা l
যৌগে অক্সিজেনের জারণ সংখ্যা l
যৌগমূলকের মোট জারণ সংখ্যা +1 l
যৌগে Mn এর জারণ সংখ্যা +7
H₂SO₄ যৌগে S এর জারণ সংখ্যা +6 l
জারণ সংখ্যা ও যোজনীর মধ্যে যোজনী সর্বদা পূর্ণসংখ্যা l
ধনাত্মক বা ঋণাত্মক, পূর্ণসংখ্যা, শূন্য এমনকি ভগ্নাংশ হতে জারণ সংখ্যা l
জারণ প্রক্রিয়ায় বিজারক পদার্থ ইলেকট্রন ত্যাগ করে l
বিজারণ প্রক্রিয়ায় জারক পদার্থ ইলেকট্রন গ্রহণ করে l
Simultaneous Process অর্থ যুগপৎ প্রক্রিয়া l
বিক্রিয়াটি রেডক্স বিক্রিয়ার অন্তর্গত সংযোজন বিক্রিয়া ধরনের বিক্রিয়া l
বিক্রিয়াটি সংশ্লেষণ বিক্রিয়া ধরনের বিক্রিয়া l
সংশ্লেষণ বিক্রিয়ায় বিক্রিয়ায় শুধু মৌলিক পদার্থ যুক্ত হয়ে যৌগ গঠন করে l
বিক্রিয়াটি বিয়োজন বিক্রিয়া ধরনের l
পানির তড়িৎ বিশ্লেষণ বিয়োজন বিক্রিয়ার মাধ্যমে সংঘটিত হয়l
পানির তড়িৎ বিশ্লেষণ বিয়োজন বিক্রিয়ার মাধ্যমে সংঘটিত হয় l
বিক্রিয়াটি প্রতিস্থাপন বিক্রিয়া ধরনের l
বাতাসের অক্সিজেন উপাদানের সাথে বিক্রিয়ায় দহন বিক্রিয়া সংঘটিত হয় l
বিক্রিয়াটি দহন বিক্রিয়া ধরনের l
দহন বিক্রিয়ায় অক্সিজেন জারক হিসেবে কাজ করে l
নন-রেডক্স বিক্রিয়া বিক্রিয়ায় কোনো পরমাণুর জারণ সংখ্যার হ্রাস-বৃদ্ধি ঘটে না l
ইলেকট্রন স্থানান্তরের ভিত্তিতে প্রশমন বিক্রিয়া নন-রেডক্স বিক্রিয়া ধরনের l
এসিড ও ক্ষারের বিক্রিয়ায় লবণ ও পানি উৎপন্ন হওয়ায় বিক্রিয়াকে প্রশমন বিক্রিয়া বলা হয় l
HCl(aq) + NaOH(aq) → NaCl(aq) + প্রশমন বিক্রিয়া বিক্রিয়ার অন্তর্গত l
তীব্র এসিড ও তীব্র ক্ষারের প্রশমন বিক্রিয়ায় ∆H এর মান l
প্রশমন বিক্রিয়া বলতে সাধারণত দুটি আয়নের সংযোগ বুঝায় l
মোল পানি উৎপন্ন করতে যে পরিমাণ তাপ উৎপন্ন হয় তাকে প্রশমন তাপ বলে l
মোল উৎপাদনে প্রশমন তাপের মান l
অধঃক্ষেপণ বিক্রিয়ায় বিক্রিয়ক তরল অবস্থায় থাকে l
পানিতে এর দ্রবণীয়তা বেশি l
আর্দ্র বিশ্লেষণ বিক্রিয়ার অপর নাম পানি বিশ্লেষণ বিক্রিয়া l
বিক্রিয়াটি আর্দ্র বিশ্লেষণধরনের l
যৌগের পানিতে দ্রবণীয়তা অদ্রবণীয় l
আয়নিক যৌগ কেলাস গঠনের জন্য এক বা একাধিক পানির অণুর সাথে যুক্ত হয়, একে পানিযোজন বিক্রিয়া বলে l
পেন্টা হাইড্রেট কপার সালফেট যৌগে 5 অণু অণু কেলাস পানি রয়েছে l
বিক্রিয়াটি পানিযোজন বিক্রিয়া প্রক্রিয়ায় অন্তর্গত l
হেন্টা হাইড্রেট ফেরাস সালফেটের সংকেত l
সমাণুকরণ বিক্রিয়া বিক্রিয়ার মাধ্যমে একটি সমাণু থেকে অপর একটি সমাণু তৈরি হয় l
A: বিক্রিয়ায় A যৌগটির সংকেত ।
যৌগের সমাণু যৌগ l
পলিমার অণুর ক্ষুদ্র একক অণুতে মনোমার বলে l
ইথিলিনের পলিমারকরণ বিক্রিয়ায় প্রয়োজনীয় বায়ুচাপের মান 1200 atm l
ইথিলিন মনোমার থেকে পলিথিন তৈরিতে প্রয়োজনীয় তাপমাত্রা 200°C l
বিক্রিয়ায় প্রয়োজনীয় প্রভাবক
মরিচা মূলত আর্দ্র ফেরিক অক্সাইড l
পদার্থের রাসায়নিক বিক্রিয়ায় মরিচা তৈরি হয়
ধাতব পদার্থের মরিচা সৃষ্টির ক্ষতিকর দিক ধাতুর পৃষ্ঠতল ক্ষয় l
মরিচার রাসায়নিক সংকেত l
অ্যালুমিনিয়ামের তৈরি জিনিসপত্র ক্ষয়ের জন্য দায়ী যৌগ
পিপড়ার মুখ বা মৌমাছির চুলে এসিড ধরনের পদার্থ থাকে
মৌমাছি হুল ফুটালে ক্ষতস্থানে ক্ষারক ধরনের পদার্থ যোগ করতে হয়l
আমাদের শরীরে শ্বসন প্রক্রিয়ার মূলত গ্লুকোজ পদার্থ জারিত হয়
শ্বসন প্রক্রিয়ায় গ্লুকোজ অক্সিজেন দ্বারা জারিত হয় l
Related Question
View Allযে রাসায়নিক বিক্রিয়ায় বিক্রিয়ক পদার্থগুলো উৎপাদে পরিণত হয়, কিন্তু উৎপাদ পদার্থগুলো পুনরায় বিক্রিয়কে পরিণত হয় না তাকে একমুখী বিক্রিয়া বলো হয়।
কোন বিক্রিয়ায় বিক্রিয়কের ঘনমাত্রা বৃদ্ধির সঙ্গে বিক্রিয়ার বেগ বৃদ্ধি পায়। অতএব, একটি উভমুখী বিক্রিয়ার শুরুতে সম্মুখ বিক্রিয়ার বেগ সবচেয়ে বেশী থাকবে এবং সময়ের সাথে বিক্রিয়ার পরিমাণ কমতে থাকবে ও উৎপাদের পরিমাণ বাড়তে থাকবে। কাজেই সময়ের সাথে সম্মুখ বিক্রিয়ার বেগ কমতে থাকবে এবং বিপরীত বিক্রিয়ার বেগ বাড়তে থাকবে। এক সময় সম্মুখ ও বিপরীত বিক্রিয়ার বেগ সমান হবে। এই অবস্থাকে রাসায়নিক সাম্যাবস্থা বলে।
আমরা জানি, কোন মৌল বা যৌগকে বায়ুর অক্সিজেনের উপস্থিতিতে পুড়িয়ে তার উপাদান মৌলের অক্সাইডে পরিণত করার প্রক্রিয়াকে দহন বিক্রিয়া বলে। এ বিক্রিয়াটি তাপোৎপাদী।
উদ্দীপকে উল্লেখিত অপু ও সেতু উভয়ের বাসায় রান্নার কাজে প্রাকৃতিক গ্যাস ব্যবহার করা হয়।
আমাদের দেশে প্রাপ্ত প্রাকৃতিক গ্যাস যা জ্বালানি হিসেবে ব্যবহৃত হয় তার রাসায়নিক নাম মিথেন। অর্থাৎ এক্ষেত্রে মিথেন গ্যাসকে বায়ুর অক্সিজেনের উপস্থিতিতে পুড়িয়ে বা দহন করে তাপ উৎপন্ন করা হয়।
তাই সেতুর বাসায় জ্বালানির দহনে পর্যাপ্ত অক্সিজেন সরবরাহ থাকায় জ্বালানির পূর্ণ দহনে দহন বিক্রিয়া সংঘটিত হয়।
CH4(g) + 2O2 (g) → CO2(g) + 2H2O(g) + তাপশক্তি।
আবার অক্সিজেনের সরবরাহ কম হলে জ্বালানির আংশিক দহনেও দহন বিক্রিয়া সংঘটিত হয়। তাই অপুর বাসায় মিথেনের দহনে বিক্রিয়াটিও দহন বিক্রিয়া।
CH4(g) + O2(g) →CO(g) + 2H2O (g) + শক্তি
CH4(g) + O2 (g) → C(s) + 2H2O(g) + শক্তি
উপরিউক্ত সকল বিক্রিয়ায় প্রাকৃতিক গ্যাস মিথেনকে বায়ুর উপস্থিতিতে পোড়ানো হয়। কাজেই রান্নায় সময় বাসায় সম্পন্ন বিক্রিয়া মূলত দহন বিক্রিয়া।
উদ্দীপকের আলোকে অপুর বাসায় রান্নার সময় পাত্রের নিচে কালো দাগ পড়ে। কিন্তু সেতুর বাসায় পাত্রের নিচে কোনো দাগ পড়ে না।
আমরা জানি, প্রাকৃতিক গ্যাস মিথেনকে বায়ুর অক্সিজেনের সাথে পোড়ালে কার্বন-ডাই অক্সাইড, পানি ও প্রচুর তাপ উৎপন্ন হয়। তবে দহনকালে অক্সিজেনের সরবরাহ কম হলে মিথেনের আংশিক দহনে কার্বন মনো অক্সাইড/কার্বন ও কম তাপ উৎপন্ন করে এবং পাত্রের নিচে কালো দাগ সৃষ্টি হয়।
শক্তি
শক্তি
অন্যদিকে অক্সিজেনের সরবরাহ পর্যাপ্ত হলে জ্বালানির পূর্ণ দহন হয় এবং উৎপাদ হিসেবে কার্বন ডাই অক্সাইড, জলীয় বাষ্প ও প্রচুর তাপ উৎপন্ন হয় কিন্তু পাত্রের তলায় কোন কাল দাগ সৃষ্টি করে না।
CH4 (g)+2O2 (g) CO2(g) + 2H2O + শক্তি।
তাই উপরিউক্ত আলোচনার আলোকে বলা যায় যে, অপুর বাসায় রান্নার কাজে গ্যাসের অপচয় হয়।
যে রাসায়নিক বিক্রিয়ার ফলে তাপশক্তি উৎপন্ন হয় তাকে তাপ উৎপাদী বিক্রিয়া বলে।
যৌগ গঠনের সময় কোনো মৌলের অন্য মৌলের সাথে যুক্ত হওয়ার ক্ষমতাকে তার যোজনী বলে। অপরদিকে, কোনো মৌলের জারণ সংখ্যা হলো মৌলটির চার্জযুক্ত যোজনী। ভিন্ন ভিন্ন যৌগে একই যোজনী বিশিষ্ট মৌলের জারণ মান ভিন্ন ভিন্ন হতে পারে। যেমন- CH4 এবং CCl4 উভয় যৌগে C এর যোজনী 4 কিন্তু CH4- এ C এর জারণ সংখ্যা -4 ও CCl4 এ +4 । অর্থাৎ, যোজনী ও জারণ সংখ্যা এক নয়।
১ ক্লিকে প্রশ্ন, শীট, সাজেশন ও
অনলাইন পরীক্ষা তৈরির সফটওয়্যার!
শুধু প্রশ্ন সিলেক্ট করুন — প্রশ্নপত্র অটোমেটিক তৈরি!





