ii নং মৌলটি ক্লোরিন। মৌলটির পরমাণুর ইলেকট্রন সংখ্যা 17. মৌলটির ইলেকট্রন বিন্যাস সঠিক বোরের মতবাদ অনুসারে ব্যাখ্যা করা সম্ভব।
বোর পরমাণু মডেল অনুসারে কোনো কোনো মৌলের নির্দিষ্ট প্রধান শক্তি স্তরে ইলেকট্রন সংখ্যা । যেখানে n প্রধান শক্তি স্তরের সংখ্যা।
Cl এর ক্ষেত্রে ১ম শেল বা K শেলে ইলেকট্রন সংখ্যা = 2টি যেখানে n = 1
২য় বা L শক্তিস্তরে ইলেকট্রন সংখ্যা
= 8[n = 2]
৩য় বা M শেলে ইলেকট্রন সংখ্যা
= 18 টি হওয়ার কথা হলেও CI পরমাণুর ইলেকট্রন সংখ্যা 17 হওয়ায় M শেলে ইলেকট্রন সংখ্যা 7 টি হয়।
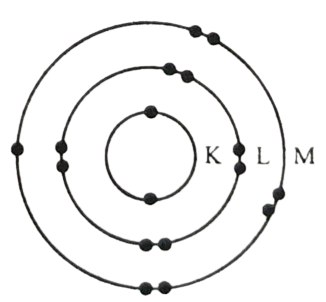
K = 2 টি ইলেকট্রন
L = 8 টি ইলেকট্রন অবশিষ্ট
M = 17 - (2 + 8) = 7টি
মূলত মৌলটির পারমাণবিক সংখ্যা 18 অপেক্ষা কম হলেও এটি বোরের মডেল অনুসারে ব্যাখ্যা করা সম্ভব। কারণ অভ্যন্তরের শক্তিঃস্তরগুলোতে নিয়ম অনুসরণ করে ইলেকট্রন সজ্জিত হয়। কিন্তু সর্বশেষ স্তরের ইলেকট্রন বিন্যাস নির্ণয়ের জন্য মোট প্রোটন সংখ্যা বা ইলেকট্রন সংখ্যা হতে পূর্ববর্তী শক্তিস্তরের ইলেকট্রন সংখ্যা বিয়োগ করতে হবে।
জ্ঞাতব্য: ইলেকট্রন বিন্যাসে 4s ও 3d, 5s ও 4d অরবিটাল সংক্রান্ত তারতম্যের কারণ আউফবাউ নীতি দ্বারা ব্যাখ্যা করা হয়। CI এর ক্ষেত্রে এ ধরনের তারতম্য নেই।
অতএব, 17CI এর ইলেকট্রন বিন্যাস বোর পরমাণু মডেল অনুসারে ব্যাখ্যা করা সম্ভব।
Related Question
View Allকোন মৌলের একটি পরমাণুর নিউক্লিয়াসে যতটি প্রোটন থাকে সে সংখ্যাকে ঐ মৌলের পারমাণবিক সংখ্যা বলে।
এবং মৌল দুটির প্রোটন সংখ্যা বা পারমাণবিক সংখ্যা যথাক্রমে 29 ও 30 এবং ভরসংখ্যা যথাক্রমে 64 ও 64। অর্থাৎ নিউক্লিয়ন সংখ্যা একই। নিউক্লিয়ন সংখ্যা হলো প্রোটন ও নিউট্রন সংখ্যার যোগফল। আমরা জানি, নিউট্রন সংখ্যা = ভর সংখ্যা (A) – পারমাণবিক সংখ্যা (Z)
সুতরাং এর নিউট্রন সংখ্যা = 64-29 = 35
এর নিউট্রন সংখ্যা = 64 - 30 = 34
যেহেতু, মৌল দুটির পারমাণবিক সংখ্যা বা প্রোটন সংখ্যা ভিন্ন তাই পরমাণু দুটির নিউক্লিয়ন সংখ্যা সমান হলেও, নিউট্রন সংখ্যা ভিন্ন হবে।
ফরিদের আঁকা মডেলটি রাদারফোর্ড পরমাণু মডেলকে সমর্থন করে। মডেলটির স্বীকার্যসমূহ হলো-
i. পরমাণুর কেন্দ্রস্থলে একটি ধনাত্মক চার্জ বিশিষ্ট ভারী বস্তু বিদ্যমান। এই ভারী বস্তুকে পরমাণুর কেন্দ্র বা নিউক্লিয়াস বলা হয়। পরমাণুর মোট আয়তনের তুলনায় নিউক্লিয়াসের 'আয়তন অতি নগণ্য। নিউক্লিয়াসে পরমাণুর সমস্ত ধনাত্মক চার্জ ও প্রায় সমস্ত ভর কেন্দ্রীভূত।
ii. পরমাণু বিদ্যুৎ নিরপেক্ষ। অতএব নিউক্লিয়াসের ধনাত্মক চার্জযুক্ত প্রোটন সংখ্যার সমান সংখ্যক ঋণাত্মক চার্জযুক্ত ইলেকট্রন পরমাণুর নিউক্লিয়াসকে পরিবেষ্টিত করে রাখে।
iii. সৌরজগতের সূর্যের চারদিকে ঘূর্ণায়মান গ্রহসমূহের মতো পরমাণুর ইলেকট্রনগুলো নিউক্লিয়াসের চারদিকে অবিরাম ঘুরছে। ধনাত্মক চার্জ বিশিষ্ট নিউক্লিয়াস ও ঋণাত্মক চার্জ বিশিষ্ট ইলেকট্রনসমূহের পারস্পরিক স্থির বৈদ্যুতিক আকর্ষণজনিত কেন্দ্রমুখী বল এবং ঘূর্ণায়মান ইলেকট্রনের কেন্দ্র বহির্মুখী বল পরস্পর সমান।

চিত্র: রাদারফোর্ডের পরমাণু মডেল
উদ্দীপকে বিদ্যমান ফরিদের অঙ্কিত মডেল হল রাদারফোর্ডের পরমাণু মডেল। এটি বিশ্লেষণ করলে দেখা যায়, ইলেকট্রনগুলো সর্পিলাকারে ঘুরতে ঘুরতে নিউক্লিয়াসে পতিত হচ্ছে, তাই অঙ্কিত মডেলটি একটি অস্থায়ী পরমাণু মডেল।
ম্যাক্সওয়েলের তত্ত্বানুসারে কোন চার্জযুক্ত কণা কোনো বৃত্তাকার পথে ঘুরতে থাকলে তা ক্রমাগত শক্তি বিকিরণ করবে এবং তার আবর্তন কক্ষপথের ব্যাসার্ধ ধীরে ধীরে কমতে থাকবে। সুতরাং ইলেকট্রনসমূহ ক্রমশ শক্তি হারাতে হারাতে নিউক্লিয়াসে প্রবেশ করবে। ফলে মডেলটি অর্থাৎ পরমাণুর অস্তিত্ব বিলীন হয়ে যাবে।
অর্থাৎ, রাদারফোর্ডের পরমাণু মডেল ম্যাক্সওয়েলের তত্ত্ব অনুসারে পরমাণু স্থায়ী হবে না।
কোনো মৌলের পূর্ণ নামের সংক্ষিপ্ত প্রকাশকে ঐ মৌলের প্রতীক বলা হয়।
বর্ণালি হলো বিভিন্ন বর্ণের আলোর সমাবেশ। বোর পরমাণু মডেল অনুসারে পরমাণুর মধ্যে কোনো ইলেকট্রন যখন একটি নিম্নতর কক্ষপথ থেকে উচ্চতর কক্ষপথে স্থানান্তরিত হয় তখন নির্দিষ্ট পরিমাণ শক্তি শোষণ করে। আবার যখন উচ্চতর শক্তিস্তর থেকে নিম্নতর শক্তিস্তরে স্থানান্তরিত হয় তখন নির্দিষ্ট পরিমাণ শক্তি বিকিরণ করে। বিকিরিত শক্তি আলোক শক্তিরূপে আমাদের চোখে ধরা পড়ে। এ আলোক শক্তিকে বর্ণালি হিসাবে পাওয়া যায়। এভাবে পরমাণুতে বর্ণালির সৃষ্টি হয়।
১ ক্লিকে প্রশ্ন, শীট, সাজেশন ও
অনলাইন পরীক্ষা তৈরির সফটওয়্যার!
শুধু প্রশ্ন সিলেক্ট করুন — প্রশ্নপত্র অটোমেটিক তৈরি!



