যৌগমূলক হচ্ছে একাধিক মৌলের একাধিক পরমাণুর সমন্বয়ে গঠিত একটি পরমাণুগুচ্ছ যা একটি আয়নের ন্যায় আচরণ করে।
কোনো মৌলের সর্বশেষ প্রধান শক্তিস্তরের মোট ইলেকট্রন সংখ্যাকে সেই মৌলের যোজ্যতা ইলেকট্রন বলে। অন্যদিকে ধাতব মৌলের ক্ষেত্রে সর্বশেষ কক্ষপথের ইলেকট্রন সংখ্যা এবং অধাতব মৌলের ক্ষেত্রে সর্বশেষ কক্ষপথের বিজোড় ইলেকট্রন সংখ্যা মৌলের যোজ্যতা নির্দেশ করে।
ম্যাগনেসিয়াম ধাতুর যোজ্যতা ও যোজ্যতা ইলেকট্রন উভয়ই 21 অপরদিকে অক্সিজেন অধাতব মৌল বিধায় যোজ্যতা ইলেকট্রন সংখ্যা 4 হলেও সর্বশেষ কক্ষপথে দুইটি বিজোড় ইলেকট্রনের অবস্থানের কারণে এর যো জজুতা হয় 2।
ম্যাগনেসিয়াম ধাতুর যোজ্যতা ও যোজ্যতা ইলেকট্রন উভয়ই 21 অপরদিকে অক্সিজেন অধাতব মৌল বিধায় যোজ্যতা ইলেকট্রন সংখ্যা 4 হলেও সর্বশেষ কক্ষপথে দুইটি বিজোড় ইলেকট্রনের অবস্থানের কারণে এর যো জজুতা হয় 2।
উপরোক্ত ইলেকট্রন বিন্যাস থেকে দেখা যায় ক্লোরিন পরমাণুর সর্বশেষ কক্ষপথে 7টি ইলেকট্রন বিদ্যমান। অষ্টক পূর্ণতার জন্য দুটি ক্লোরিন পরমাণুর প্রত্যেকে একটি করে ইলেকট্রন প্রদান করে এক জোড়া ইলেকট্রন শেয়ারের মাধ্যমে সমযোজী বন্ধন গঠনের মাধ্যমে একটি ক্লোরিন অণু (Cl2) গঠন করে। ফলে প্রতিটি ক্লোরিন পরমাণু নিকটবর্তী নিষ্ক্রিয় গ্যাস আর্গনের ইলেকট্রন বিন্যাস অর্জন করে।
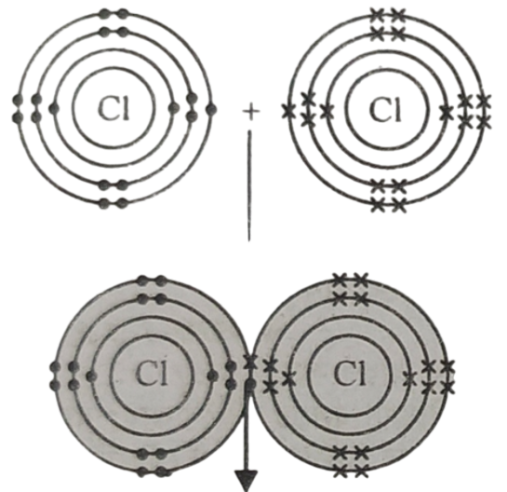
শেয়ারকৃত বন্ধন ইলেকট্রন
চিত্র: Cl2 অণুর বন্ধন গঠন।
এখানে X ও Y মৌল দুটির পারমাণবিক সংখ্যা যথাক্রমে 20 ও 17। সুতরাং মৌল দুটি হলো ক্যালসিয়াম (Ca) ও ক্লোরিন (CI)।
ক্যালসিয়াম পরমাণু তার সর্বশেষ কক্ষপথে বিদ্যমান ইলেকট্রন দুটি ত্যাগ করে ক্যালসিয়াম ক্যাটায়ন (Ca2+) এ পরিণত হয় এবং নিকটবর্তী নিষ্ক্রিয় গ্যাস আর্গনের ইলেকট্রন কাঠামো লাভ করে।
অন্যদিকে ক্লোরিন পরমাণুর শেষ কক্ষপথে 7টি ইলেকট্রন বিদ্যমান। অষ্টক পূর্ণতার জন্য প্রতিটি ক্লোরিন পরমাণু একটি করে ইলেকট্রন গ্রহণ করে ক্লোরাইড (CI-) গঠন করে। অ্যানায়ন ও ক্যাটায়ন পরস্পর স্থির বৈদ্যুতিক আকর্ষণ বলের প্রভাবে যুক্ত হয়ে আয়নিক যৌগ CaCl2 গঠন করে।
__________________________
আবার, পানিতে বিদ্যমান অক্সিজেনের তড়িৎ ঋণাত্মকতা হাইড্রোজেন অপেক্ষা বেশি। তাই পানির অণুতে অক্সিজেনে আংশিক ঋণাত্মক প্রান্তের ও হাইড্রোজেনে আংশিক ধনাত্মক প্রান্তের সৃষ্টি হয়।
আয়নিক যৌগ CaCl2 এ ধনাত্মক (Ca2+) এবং ঋণাত্মক (CI-) প্রান্ত বিদ্যমান। CaCl2 এর ধনাত্মক (Ca2+) প্রান্ত পানির ঋণাত্মক অক্সিজেন প্রান্ত দ্বারা এবং ঋণাত্মক (CI-) প্রান্ত পানির ধনাত্মক হাইড্রোজেন দ্বারা আকর্ষিত হয়ে দ্রবীভূত হয়।
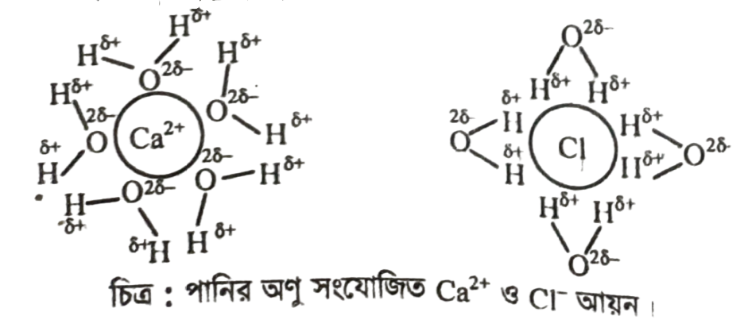
সুতরাং X ও Y দ্বারা গঠিত যৌগ CaCl2 আয়নিক যৌগ এবং এর বিপরীতধর্মী দুই মেরুর সাথে পানির বিপরীত দুই মেরুর আকর্ষণে এটি পানিতে দ্রবীভূত হয়।
Related Question
View All১ ক্লিকে প্রশ্ন, শীট, সাজেশন ও
অনলাইন পরীক্ষা তৈরির সফটওয়্যার!
শুধু প্রশ্ন সিলেক্ট করুন — প্রশ্নপত্র অটোমেটিক তৈরি!



