রাসায়নিক বিক্রিয়ার সময় একাধিক বিক্রিয়কের মধ্যে যে বিক্রিয়ক বিক্রিয়া করার পর আর অবশিষ্ট থাকে না তাকে লিমিটিং বিক্রিয়ক বলে।
পর্যায় সারণির 18 নং গ্রুপের মৌলসমূহকে নিষ্ক্রিয় গ্যাস বলা হয়। আর্গন, 1৪নং গ্রুপের মৌল। এর শেষ কক্ষপথে ৪টি ইলেকট্রন থাকে যা সুস্থিত ইলেকট্রন কাঠামো। তাই Ar কাউকে ইলেকট্রন দান বা গ্রহণ করে না অথবা শেয়ার করে যৌগ গঠন করেনা অর্থাৎ Ar রাসায়নিকভাবে নিষ্ক্রিয় হয়। এজন্য Ar কে নিষ্ক্রিয় গ্যাস বলা হয়।
উদ্দীপকের A যৌগটি একটি হাইড্রোকার্বন।
H এর সংযুতি = 14.29%
∴ C এর সংযুতি = (100 – 14.29)%
= 85.71%
আণবিক সংকেত নির্ণয় করতে প্রথমে স্থূল সংকেত নির্ণয় করতে হবে।
| বিষয় | H | C | মূল সংকেত |
| শতকরা সংযুতি | 14.29 | 85.71 | CH2 |
| শতকরা সংযুতি/আপেক্ষিক পারমাণবিক ভর | |||
| H : C | 14.29 : 7.1425 = 2 : 1 | ||
∴ যৌগটির স্থূল সংকেত = CH2
আণবিক সংকেত = (CH2)n
আণবিক ভর =
= 14n
দেওয়া আছে, প্রকৃত আণবিক ভর = 28
∴ 14n = 28
বা n = 2
সুতরাং যৌগটির প্রকৃত আণবিক সংকেত =
উদ্দীপকের 28 আণবিক ভরবিশিষ্ট A হাইড্রোকার্বনটি C2H4 (ইথিন)। এটি থেকে খাদ্য সংরক্ষক প্রস্তুত করা সম্ভব।
ইথিনকে H3PO4 এর উপস্থিতিতে 300°C তাপমাত্রায় ও 60 atm চাপে H2O এর সাথে বিক্রিয়া করালে ইথানল উৎপন্ন হয়।
H2C = CH2 + H2O H3C-CH2-OH
CH3 – CH2 – OH কে জারিত করলে প্রথমে অ্যালডিহাইড এবং পরে জৈব এসিড তৈরি হয়।
CH3-CH2-OH + [O] → CH3- CHO
CH3-CHO + [O] → CH3COOH
ইথানয়িক এসিড
এই ইথানয়িক এসিডের 4 – 10% জলীয় দ্রবণকে ভিনেগার বা সিরকা বলে যা খাদ্য সংরক্ষক হিসেবে ব্যবহৃত হয়। ইথানয়িক এসিড একটি জৈব এসিড যার ব্যাকটেরিয়া ধ্বংসের ক্ষমতা থাকে। ফলে খাদ্যদ্রব্যের পচনকারী ব্যাকটেরিয়া মেরে এটি খাদ্য সংরক্ষক হিসেবে কাজ করতে পারে।
Related Question
View Allপেট্রোলিয়ামের প্রধান উপাদান হলো হাইড্রোকার্বন।
অ্যালকেনসমূহ কার্বন-কার্বন ও কার্বন-হাইড্রোজেন শক্তিশালী একক সমযোজী বন্ধনের মাধ্যমে গঠিত হয়। এরা রাসায়নিকভাবে আসক্তিহীন বা প্যারাফিন নামে পরিচিত। এ কারণে অ্যালকেনসমূহ সাধারণত রাসায়নিক বিক্রিয়ায় অংশগ্রহণ করে না অর্থাৎ কম সক্রিয় জৈব যৌগ। পক্ষান্তরে অ্যালকিনসমূহের অণুতে কার্বন-কার্বন দ্বি-বন্ধন বিদ্যমান থাকে। কার্বন-কার্বন দ্বি-বন্ধনের প্রথমটি সিগমা বন্ধন হওয়ায় প্রথম বন্ধনটি শক্তিশালী হলেও দ্বিতীয় বন্ধটি পাই (গ) বন্ধন হওয়ায়, তুলনামূলকভাবে দ্বিতীয় বন্ধনটি প্রথম বন্ধন অপেক্ষা দুর্বল হয়। তাই পাই (গ) বন্ধনটির সহজে ভাঙ্গন ঘটে। ফলে এরা সংযোজন, পলিমারকরণ, দহন বিক্রিয়ায় অংশগ্রহণ করে। তাই অ্যালকিন রাসায়নিকভাবে অ্যালকেন অপেক্ষা সক্রিয় হয়।
আলুতে প্রচুর পরিমাণে স্টার্চ আছে। উদ্দীপকে বিদ্যমান বিক্রিয়ার মাধ্যমে স্টার্চ থেকে গ্লুকোজ ও গ্লুকোজকে জাইমেজ এনজাইমের উপস্থিতিতে ইথানলে রূপান্তরিত করা হয়। প্রাপ্ত ইথানলকে এসিডযুক্ত পটাসিয়াম ডাইক্রোমেট অথবা পটাসিয়াম পারম্যাঙ্গানেট দ্বারা জারিত করলে প্রথমে ইথান্যাল (অ্যাসিট্যালডিহাইড) ও পরে ইথানয়িক এসিড উৎপন্ন হয়।
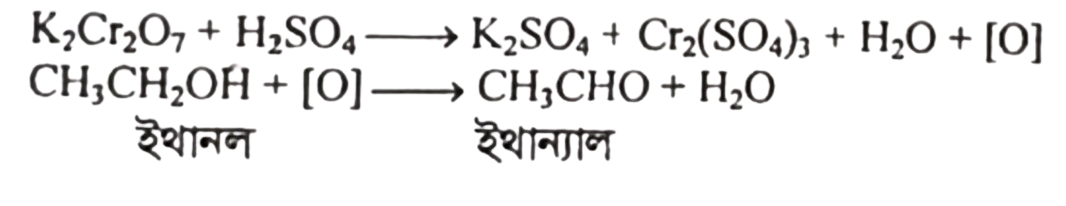
CH3CHO + [O] CH3COOH ইথানয়িক এসিড
এভাবে উৎপন্ন ইথানয়িক এসিডকে NaOH এর সাথে মিশ্রিত করলে সোডিয়াম ইথানয়েট উৎপন্ন হয়।
CH3COOH + NaOH → CH3COONa + H2O সোডিয়াম ইথানয়েট
এখানে প্রাপ্ত সোডিয়াম ইথানয়েটকে (CH3COONa) সোডালাইম (NaOH + CaO এর মিশ্রণ) সহ উত্তপ্ত করলে মিথেন (CH4) পাওয়া যায়।
বিক্রিয়া: CH3COONa CH4 + Na2CO3
এভাবে আমরা আলু থেকে মিথেন (CH4) প্রস্তুত করতে পারি।
আলুতে প্রচুর পরিমাণ স্টার্চ থাকে। অতিরিক্ত আলুতে বিদ্যমান স্টার্চ থেকে আমরা নিম্নলিখিত উপায়ে ইথানল প্রস্তুত করতে পারি যা বিকল্প জ্বালানি হিসেবে ব্যবহার করা যায়।
আলুকে প্রথমে সিদ্ধ করে কাই (Paste) এ পরিণত করা হয়। একে ম্যাস (mash) বলে। এ ম্যাসের সাথে মল্ট মিশ্রিত করে মিশ্রণটি প্রায় 45°C তাপমাত্রায় এক ঘন্টা রেখে দিলে মল্ট থেকে নিঃসৃত "ডায়াস্টেজ” নামক এক প্রকার এনজাইম দ্বারা স্টার্চ আর্দ্র বিশ্লেষিত হয়ে মল্টোজে পরিণত হয়।
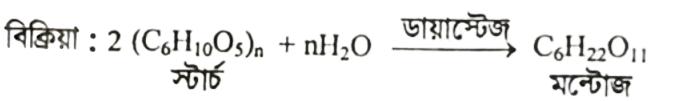
মল্টোজকে 20°C তাপমাত্রায় শীতল করে পানিযোগে লঘু (10%) করে ইস্ট যোগ করলে, ইস্ট থেকে নিঃসৃত ম্যালটেজ এনজাইম মল্টোজকে গ্লুকোজে এবং পরবর্তীতে জাইমেজ নামক এনজাইম গ্লুকোজকে ফারমেন্টেশন করে ইথানলে পরিণত করে।
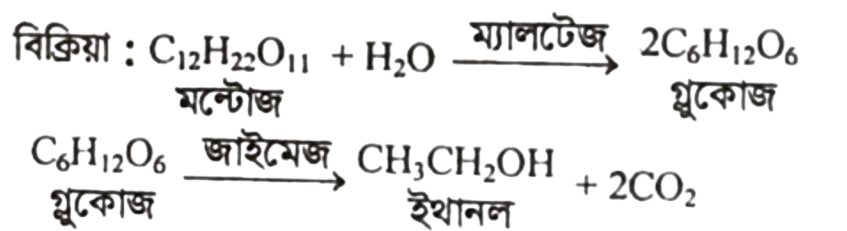
আলু থেকে এভাবে প্রাপ্ত ইথানল পৃথিবীর বিভিন্ন দেশে জীবাশ্ম জ্বালানির পরিবর্তে মটর ইঞ্জিন, বিমান, বাস, ট্রাক, কলকারখানায় বিকল্প জ্বালানিরূপে ব্যবহার করা হচ্ছে। পেট্রোলের সাথে (10-20%) ইথানল মিশ্রিত করে গ্যাসহোল (Gasohol) নামক জ্বালানি তৈরী করা হয়েছে, যা বিভিন্ন দেশে জ্বালানিরূপে ব্যবহৃত হয়ে আসছে।
CH3CH2OH + O2 → 2CO2 + 6H2O + তাপশক্তি
যেহেতু অ্যালকোহল থেকে আমরা প্রচুর পরিমাণ তাপশক্তি পাই, তাই অতিরিক্ত আলু থেকে ইথানল উৎপন্ন করে জীবাশ্ম জ্বালানির বিকল্প হিসেবে ব্যবহার সম্ভব।
হাইড্রোজেন ও কার্বন দ্বারা গঠিত দ্বি-মৌল যৌগসমূহকে হাইড্রোকার্বন বলা হয়।
অ্যারোমেটিক যৌগগুলোতে সাধারণত 5, 6 কিংবা 7 সদস্যের সমতলীয় যৌগ এবং এগুলোতে একান্তর দ্বিবন্ধন থাকে। বেনজিন ছয় সদস্যের সমতলীয় চাক্রিক যৌগ। এতে একান্তর দ্বিবন্ধন বিদ্যমান। অর্থাৎ পর্যায়ক্রমে কার্বন-কার্বন একটি একক বন্ধন এবং একটি দ্বিবন্ধন থাকে। তাই
বেনজিন  একটি অ্যারোমেটিক হাইড্রোকার্বন।
একটি অ্যারোমেটিক হাইড্রোকার্বন।
১ ক্লিকে প্রশ্ন, শীট, সাজেশন ও
অনলাইন পরীক্ষা তৈরির সফটওয়্যার!
শুধু প্রশ্ন সিলেক্ট করুন — প্রশ্নপত্র অটোমেটিক তৈরি!



