সর্বশেষ শক্তিস্তরে স্থায়ী বা নিকটতম নিষ্ক্রিয় গ্যাসের ইলেকট্রন বিন্যাস লাভের জন্য ইলেকট্রন শেয়ারের মাধ্যমে যে বন্ধন গঠিত হয়, তাকে সমযোজী বন্ধন বলে।
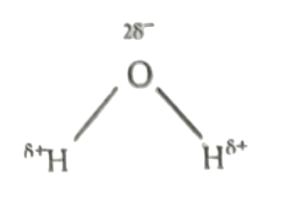
পানি (H2O) হাইড্রোজেন এবং অক্সিজেন পরমাণুর সমযোজী বন্ধনের ফলে সৃষ্ট একটি সমযোজী যৌগ। কিন্তু হাইড্রোজেন অপেক্ষা | অক্সিজেন পরমাণুর তড়িৎ ঋণাত্মকতা বেশি হওয়ায় সমযোজী রন্ধনের শেয়ারকৃত ইলেকট্রন যুগলের প্রতি অক্সিজেনের আকর্ষণ অধিক হয়। ফলে শেয়ারকৃত ইলেকট্রন অক্সিজেন পরমাণুর অধিক সন্নিকটে থাকে এবং অক্সিজেন পরমাণু আংশিক ঋণাত্মক চার্জ লাভ করে। অপরদিকে হাইড্রোজেন পরমাণু আংশিক ধনাত্মক চার্জ লাভ করে। ফলে পানির অণুতে দুটি বিপরীত মেরুর সৃষ্টি হয় এবং একে পোলারিটি বলে। তাই পানি একটি পোলার অণু।
উদ্দীপকের (৮) যৌগটি একটি ধাতব Na ও একটি অধাতব CI এর সমন্বয়ে গঠিত আয়নিক যৌগ। সকল আয়নিক যৌগ কঠিন অবস্থায় কেলাসাকারে থাকে। সুতরাং NaCl যৌগটি কেলাস গঠন করে।
তাদের কেলাস ল্যাটিসসমূহ ধনাত্মক ও ঋণাত্মক আয়ন দ্বারা সুশৃঙ্খল জ্যামিতিক আকারে এমনভাবে সজ্জিত থাকে যেন একই ধরনের আধান বিশিষ্ট আয়নসমূহ পরস্পর থেকে যত দূরে সম্ভব এবং বিপরীত আধানবিশিষ্ট আয়নসমূহ যত নিকটে সম্ভব অবস্থান করতে পারে।
আয়নিক যৌগে এককভাবে কোন অণুর অস্তিত্ব নেই। তাই NaCl এর কোনো অণু নেই। NaCl দ্বারা সোডিয়াম ক্লোরাইড কেলাসে ও CI আয়নসমূহের অনুপাতকে বুঝায়।
প্রতিটি আয়ন অষ্টতলকীয়ভাবে ছয়টি সমদূরত্বে অবস্থানকারী CI- আয়ন দ্বারা পরিবেষ্টিত। অনুরূপভাবে প্রতিটি Cl- আয়ন অষ্টতলকীয়ভাবে ছয়টি সমদূরত্বে অবস্থানকারী আয়ন দ্বারা পরিবেষ্টিত। অন্যান্য আয়নিক যৌগের গঠন NaCl এর মতো না হলেও এদের গঠন বিশেষ জ্যামিতিক আকৃতির হয়। রাসায়নিক সংকেতে ক্যাটায়ন ও অ্যানায়নের সংখ্যার অনুপাত এবং তাদের আয়ন ব্যাসার্ধের অনুপাতের উপরেই কেলাসের আকৃতি নির্ভর করে।
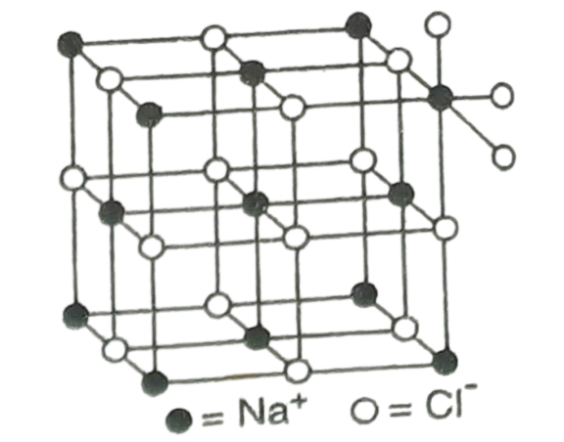
চিত্র: NaCl কেলাস
উল্লেখ্য যে, উদ্দীপকের a, c ও d যৌগত্রয় সমযোজী যৌগ হওয়ায় এরা কেলাস গঠন করে না।
উদ্দীপকের (b) যৌগটি (NaCl) একটি আয়নিক যৌগ যার মধ্যে ধনাত্মক Na+ ও ঋণাত্মক CI প্রান্ত বিদ্যমান। পানি সমযোজী যৌগ হলেও এর মধ্যে ধনাত্মক H+ প্রান্ত ও ঋণাত্মক OH° প্রান্ত বিদ্যমান। NaCl লবণকে পানিতে দিলে এটি পানির অণুর সাথে আকর্ষিত হয়। পানির ঋণাত্মক প্রান্ত NaCl এর ধনাত্মক Na⁺ প্রান্তকে এবং পানির ধনাত্মক প্রান্ত NaCl এর ঋণাত্মক CI প্রান্তকে আকর্ষণ করার মাধ্যমে পানিতে দ্রবীভূত করে।
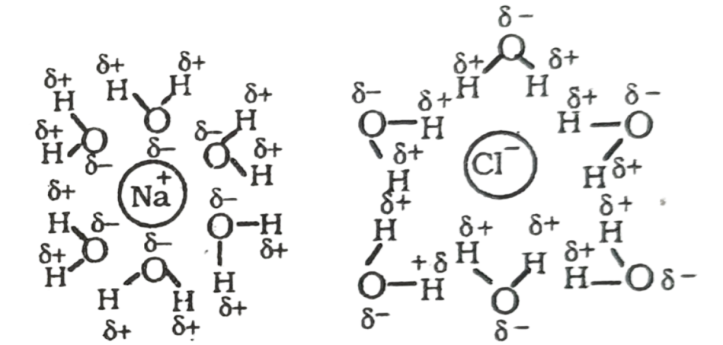
পানি অণু সংযোজিত Na+ আয়ন পানি অণু সংযোজিত CI আয়ন অপরদিকে উদ্দীপকের (c) যৌগটি (CCl4) এটি সমযোজী যৌগ। এর মধ্যে অনুরূপ কোন ধনাত্মক ও ঋণাত্মক প্রান্ত না থাকায় পানির অণুর সাথে এর কোন আকর্ষণ থাকে না। তাই এটি পানি ও অন্যান্য পোলার দ্রাবকে অদ্রবণীয়।
Related Question
View All১ ক্লিকে প্রশ্ন, শীট, সাজেশন ও
অনলাইন পরীক্ষা তৈরির সফটওয়্যার!
শুধু প্রশ্ন সিলেক্ট করুন — প্রশ্নপত্র অটোমেটিক তৈরি!



