পদার্থ (Matter)
যার ভর আছে, যা কোনো স্থান দখল করে অবস্থান করে, তাকে পদার্থ বলা হয়।
বৈশিষ্ট্য | পদার্থ | শক্তি |
| ভর | ভর আছে | ভর নাই |
| স্থান দখল | করে | করে না |
| উদাহরণ | বাতাস, পানি | তাপ, আলোক, বিদ্যুৎ |
পদার্থ ও শক্তি (Matter and Energy) প্রকৃতিতে দুটি ভিন্ন বিষয়ের অস্তিত্ব আমরা বুঝতে পারি একটি জড় বা পদার্থ (matter) এবং অন্যটি হল শক্তি (energy) ।
পদার্থ (Matter) : যা ইন্দ্রিয় গ্রাহ্য, যা কিছুটা স্থান দখল করে, যার ওজন আছে এবং বলপ্রয়োগের সাহায্যে যার স্থির বা গতিশীল অবস্থার পরিবর্তন করা যায়, তাকেই পদার্থ বলে । যেমন চেয়ার, টেবিল, ইট, বালি, খাতা, পেন্সিল ইত্যাদি । পদার্থের নির্দিষ্ট পরিমাণকে বস্তু বলে । যেমন প্লাস্টিক দিয়ে জলের বালতি, মগ তৈরি করা হয় সুতরাং জলের বালতি, মগ হল বস্তু কিন্তু এগুলির উপাদান প্লাস্টিক হল পদার্থ অর্থাৎ বস্তু যে উপাদানে তৈরি হয় তাকে জড় বা পদার্থ বলে । পৃথিবীতে জড়বস্তু এবং সজীব বস্তু এই দুই ধরনের বস্তু আমরা দেখতে পাই ।
ভর এবং ভার বা ওজন : বস্তুর ভার বা ওজন নির্ণয় : ভরের নিত্যতা সূত্র বা পদার্থের অবিনাশিতা সূত্র : শক্তির বিভিন্ন রূপ : শক্তির নিত্যতা সূত্র : শক্তির রূপান্তর : সূর্যই পৃথিবীর শক্তির প্রধান উৎস
# বহুনির্বাচনী প্রশ্ন
পদার্থের অবস্থাভেদ
States of Matter
পদার্থ সাধারণত ৩টি অবস্থায় থাকতে পারে। যথা: কঠিন, তরল এবং বায়বীয়
| কঠিন পদার্থ | কঠিন পদার্থের নির্দিষ্ট আয়তন ও নির্দিষ্ট আকার এবং দৃঢ়তা আছে। এর অণুসমূহ পরস্পরের অতি সন্নিকটে অবস্থান করে। যেমন: বালু, পাথর, লবণ ইত্যাদি। |
| তরল পদার্থ | তরল পদার্থের নির্দিষ্ট আয়তন আছে কিন্তু নির্দিষ্ট আকার নেই। তরল পদার্থের অণুসমূহ পরস্পরের সন্নিকটে থাকে, তবে তাদের মধ্যকার আকর্ষণ কঠিন পদার্থের মত প্রবল নয়। উদাহরণ: পানি, পেট্রোল, কেরোসিন, ভোজ্য তেল প্রভৃতি। |
| গ্যাসীয় পদার্থ | গ্যাসীয় পদার্থের নির্দিষ্ট আয়তন ও নির্দিষ্ট আকার নেই। গ্যাসীয় পদার্থের অণুসমূহের দূরত্ব অনেক বেশি, তাই আকর্ষণ শক্তি অনেক কম। ফলে তারা প্রায় সম্পূর্ণ মুক্তভাবে চলাচল করে। উদাহরণ: নাইট্রোজেন, অক্সিজেন, মিথেন ইত্যাদি। |
তাপ পদার্থের তিন অবস্থায় রূপান্তরের প্রধান কারণ। পানি একমাত্র পদার্থ যা প্রকৃতিতে কঠিন (বরফ), তরল (পানি) এবং বায়বীয় (জলীয় বাষ্প) তিন অবস্থাতেই পাওয়া যায়।
কঠিন | তরল | বায়বীয় |
| মেরু অঞ্চল বা পর্বত শীর্ষের বরফ | নদী, সমুদ্রের পানি | বায়ুর জলীয় বাষ্প |
# বহুনির্বাচনী প্রশ্ন
গলনাংক (Melting point)
যে তাপমাত্রায় কঠিন হতে তরল পদার্থের সৃষ্টি হয়, তাকে সে পদার্থের গলনাংক বলে। পানির গলনাংক ০° সেন্টিগ্রেড।
# বহুনির্বাচনী প্রশ্ন
স্ফুটনাংক (Boiling Point)
যে তাপমাত্রায় কোন তরল পদার্থ ফুটতে থাকে, তাকে সে পদার্থের স্ফুটনাংক বলে। পানির স্ফুটনাংক ১০০ ডিগ্রী সেন্টিগ্রেড।
# বহুনির্বাচনী প্রশ্ন
ঊর্ধ্বপাতন (Sublimation)
কোনো কোনো ক্ষেত্রে কঠিন পদার্থকে উত্তপ্ত করলে তা তরলে রূপান্তরিত না হয়ে সরাসরি বাষ্পে রূপান্তরিত হয়, তাকে ঊর্ধ্বপাতন বলা হয়। যেমন: কপূর, গন্ধক, আয়োডিন, ন্যাপথালিন, অ্যামোনিয়াম ক্লোরাইড, কার্বন ডাই অক্সাইড, আর্সেনিক, বেনজোয়িক এসিড ইত্যাদি।
পদার্থের শ্রেণিবিভাগ:
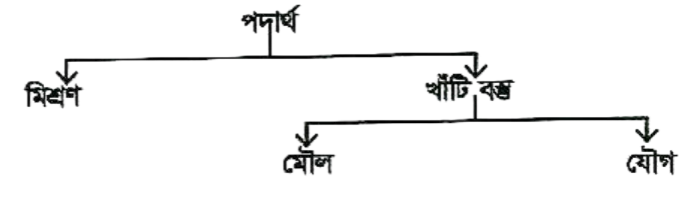
মিশ্রণ (Mixture)
দুই বা ততোধিক পদার্থকে যে কোন অনুপাতে একত্রে মিশালে যদি তারা নিজ নিজ ধর্ম বজায় রেখে পাশাপাশি অবস্থান করে, তবে উক্ত সমাবেশকে মিশ্রণ বলা হয়। বায়ু একটি মিশ্র পদার্থ কারণ বায়ুতে উপাদান মৌলসমূহ যেমন: নাইট্রোজেন, অক্সিজেন, কার্বন-ডাই-অক্সাইড ইত্যাদি নিজ নিজ ধর্ম বজায় রেখে পাশাপাশি অবস্থান করে।
খাঁটি বস্তু (Pure substance)
মৌল বা মৌলিক পদার্থ (Elements)
| সবচেয়ে হালকা মৌল | হাইড্রোজেন (H) |
| সবচেয়ে হালকা মৌলিক গ্যাস | হাইড্রোজেন (H) |
| সবচেয়ে ভারী মৌলিক গ্যাস | রেডন (Rn) |
যে বস্তুকে রাসায়নিকভাবে বিশ্লেষণ করে অন্য কোন সহজ বস্তুতে রূপান্তরিত করা যায় না, তাকে মৌল বা মৌলিক পদার্থ বলা হয়। যেমন: হাইড্রোজেন, নাইট্রোজেন, অক্সিজেন, সোনা, তামা, লোহা ইত্যাদি। পৃথিবীতে বর্তমানে মৌলিক পদার্থের সংখ্যা ১১৮। এদের মধ্যে ৯৮টি মৌল প্রকৃতিতে পাওয়া যায়। কৃত্রিম উপায়ে প্রাপ্ত মৌলিক পদার্থের সংখ্যা ২০।
যৌগ বা যৌগিক পদার্থ (Compound)
যে বস্তুকে রাসায়নিকভাবে বিশ্লেষণ করলে দুই বা ততোধিক মৌলিক পদার্থ পাওয়া যায়, তাকে যৌগ বা যৌগিক পদার্থ বলা হয়। যেমন: হাইড্রোজেন ও অক্সিজেন এ দুইটি মৌল নির্দিষ্ট ভর অনুপাতে পরস্পর যুক্ত হয়ে পানি উৎপন্ন করে। অতএব পানি একটি যৌগিক পদার্থ।
পদার্থের পরিবর্তন (Changes in matter)
পদার্থের পরিবর্তন দুই ধরনের। যথা: ভৌত বা অবস্থানগত পরিবর্তন এবং রাসায়নিক পরিবর্তন।
ভৌত বা অবস্থানগত পরিবর্তন (Physical Change)
যে পরিবর্তনের ফলে পদার্থের শুধু বাহ্যিক আকার বা অবস্থার পরিবর্তন হয় কিন্তু নতুন কোনো পদার্থে পরিণত হয় না, তাকে ভৌত বা অবস্থানগত পরিবর্তন বলে।
ভৌত পরিবর্তনের উদাহরণ :
➺ পানিকে ঠাণ্ডা করে বরফে এবং তাপ দিয়ে জলীয় বাষ্পে পরিণত করা।
➺ একটি লোহার টুকরাকে চুম্বক দ্বারা ঘর্ষণ করে চুম্বকে পরিণত করা।
➺ তাপ দিয়ে মোম গলানো।
রাসায়নিক পরিবর্তন : যে পরিবর্তনের ফলে এক বা একাধিক বস্তু প্রত্যেকে তার নিজস্ব সত্তা হারিয়ে সম্পূর্ণ নতুন ধর্ম বিশিষ্ট এক বা একাধিক নতুন বস্তুতে পরিণত হয়, তাকে রাসায়নিক পরিবর্তন বলে।
রাসায়নিক পরিবর্তনের উদাহরণ :
➺ লোহায় মরিচা ধরা। মরিচা (Rust) হলো আর্দ্র ফেরিক অক্সাইড (Fe2O3. nH2O)। লোহায় মরিচা ধরার জন্য পানি এবং অক্সিজেন প্রয়োজন।
➺ দুধকে ছানায় পরিণত করা
➺ চাল সিদ্ধ করলে ভাতে পরিণত হয়।
➺ দিয়াশলাইয়ের কাঠি জ্বালানো
# বহুনির্বাচনী প্রশ্ন
পদার্থের গঠন মূলত ক্ষুদ্রতম কণা, যেমন—পরমাণু ও অণু দ্বারা গঠিত, যা স্থান দখল করে এবং যার ভর আছে । পরমাণুর কেন্দ্রে প্রোটন ও নিউট্রন (নিউক্লিয়াস) এবং বাইরে ইলেকট্রন থাকে । এছাড়া, কোয়ার্ক ও লেপটন নামক অবিভাজ্য মৌলিক কণা দিয়েও পদার্থ গঠিত হতে পারে । পরমাণুসমূহ একত্রে অণু তৈরি করে এবং আন্তঃআণবিক বন্ধনের মাধ্যমে কঠিন, তরল বা গ্যাসীয় অবস্থায় থাকে ।
# বহুনির্বাচনী প্রশ্ন
ডাল্টনের পরমাণুবাদ (Dalton's atomic Theory)
গ্রীক দার্শনিক ডেমোক্রিটাস খ্রিস্টপূর্ব পঞ্চম শতাব্দীতে এ অভিমত প্রকাশ করেন যে, সকল পার্থিব বস্তু ক্ষুদ্র ক্ষুদ্র অবিভাজ্য কণার দ্বারা গঠিত। ডেমোক্রিটাস এ অবিভাজ্য ক্ষুদ্রতম কণার নাম দেন atomos। এ শব্দটি দুটি গ্রিক শব্দ হতে উদ্ভূত। a (অর্থাৎ না) এবং tomos (অর্থাৎ ভাগ করা)। তাই atomos শব্দের অর্থ যা ভাগ করা যায় না। ব্রিটিশ বিজ্ঞানী জন ডাল্টন ১৮০৩ সালে এ মতবাদকে বৈজ্ঞানিক মতবাদ হিসাবে প্রতিষ্ঠা করেন। আধুনিক রসায়নের ভিত্তি হচ্ছে এ পরমাণুবাদ। এ কারণে জন ডাল্টনকে 'আধুনিক রসায়নের জনক' বলা হয়।
পরমাণু (Atoms) | অণু (Molecules) |
| মৌলিক পদার্থের বৈশিষ্ট্য রক্ষাকারী ক্ষুদ্রতম কণা | মৌলিক বা যৌগিক পদার্থের বৈশিষ্ট্য রক্ষাকারী ক্ষুদ্রতম কণা। |
| রাসায়নিক প্রক্রিয়ায় সরাসরি অংশগ্রহণ করে। | রাসায়নিক প্রক্রিয়ায় সরাসরি অংশগ্রহণ করে না |
অধিকাংশ মৌলের পরমাণু খুব সক্রিয়। এরা যেমন ভিন্ন পদার্থের সাথে বিক্রিয়া করে যেমন যৌগিক পদার্থের সৃষ্টি করে, তেমনি একই পদার্থের সাথে মিলিত হয়ে মৌলিক পদার্থের অণু সৃষ্টি করে। মৌলিক গ্যাসের অণুসমূহ দ্বিপরমাণুক। যেমন- অক্সিজেন (O2), হাইড্রোজেন (H2) প্রভৃতি। নিষ্ক্রিয় গ্যাস [হিলিয়াম (He), নিয়ন (Ne), আর্গন (Ar), ক্রিপ্টন (Cr), জেনন (Xe), রেডন (Rn)]-এর অণুসমূহ এক পরমাণুক।
# বহুনির্বাচনী প্রশ্ন
পারমাণবিক ভর ও আণবিক ভর (Atomic mass and molecular mass)
পারমাণবিক ভর হচ্ছে একটি সরল রাশি যা একটি পরমাণু একটি কার্বন-১২ পরমাণুর ভরের ১/১২ অংশের তুলনায় কতগুণ ভারী তা প্রকাশ করে। আর আণবিক ভর হলো কোনো পদার্থের একটি অণুর ভর একটি কার্বন ১২ পরমাণুর ভরের ১/১২ অংশের যতগুণ ভারী, সে সংখ্যাকে আণবিক ভর বলা হয়। উদাহরণস্বরূপ, পানির সংকেত H2O। পানির একটি অণুতে ২টি হাইড্রোজেন ও ১টি অক্সিজেন পরমাণু বিদ্যমান।
পানির আণবিক ভর = (হাইড্রোজেনের পারমাণবিক ভর ২) + (অক্সিজেনের পারমাণবিক ভর ১)
= (১ ২) + (১৬ ১) = ২ + ১৬ = ১৮
একইভাবে, অক্সিজেনের সংকেত O2। অক্সিজেনের একটি অণুতে ২টি অক্সিজেন পরমাণু বিদ্যমান। অক্সিজেনের আণবিক ভর = অক্সিজেনের পারমাণবিক ভর ২ = ১৬ ২ = ৩২।
# বহুনির্বাচনী প্রশ্ন
অ্যাভোগেড্রোর সূত্র (Avogadro's Law)
একই তাপমাত্রা ও চাপে সমআয়তন বিশিষ্ট সকল গ্যাসে (মৌলিক ও যৌগিক) সমান সংখ্যক অণু থাকে। কোনো বস্তুর এক মোলে যত সংখ্যক অণু বা পরমাণু থাকে সেই সংখ্যাকে অ্যাভোগেড্রো সংখ্যা বলে। অ্যাভোগেড্রো সংখ্যার মান ৬.০২ ১০২৩। উদাহরণ: এক মোল (অর্থাৎ ১ গ্রাম) হাইড্রোজেনে ৬.০২ ১০২৩ টি হাইড্রোজেন পরমাণু আছে।
মৌলের প্রতীক
কোনো মৌলের ইংরেজি বা ল্যাটিন নামের সংক্ষিপ্ত রূপকে প্রতীক বলে। প্রত্যেকটি মৌলকে সংক্ষেপে প্রকাশ করতে তাদের আলাদা আলাদা প্রতীক ব্যবহার করা হয়। মৌলের প্রতীক লিখতে কিছু নিয়ম অনুসরণ করতে হয়।
মৌল | ল্যাটিন নাম | প্রতীক |
| কপার | Cuprum | Au |
| লেড | Plumbum | Pb |
| সোডিয়াম | Natrium | Na |
| টাংস্টেন | Wolfram | W |
| মারকারি | Hydrurgyrum | Hg |
| আয়রন | Ferrum | Fe |
| পটাশিয়াম | Kalium | K |
| সিলভার | Argentum | Ag |
| টিন | Stannum | Sn |
| এন্টিমনি | Stibium | sb |
| গোল্ড | Aurum | Au |
মৌল | ইংরেজি নাম | প্রতীক |
| হাইড্রোজেন | Hydrogen | H |
| অক্সিজেন | Oxygen | O |
| নাইট্রোজেন | Nitrogen | N |
মৌলের নামকরণ
মৌল | ইংরেজি নাম | প্রতীক |
| কার্বন | Carbon | C |
| ক্লোরিন | Chlorine | Cl |
| ক্যালসিয়াম | Calcium | Ca |
মৌলের নামকরণ (প্রথম অক্ষর এক)।
মৌল | ইংরেজি নাম | প্রতীক |
| কোবাল্ট | Cobalt | Co |
| ক্যাডমিয়াম | Cadmium | Cd |
| ক্রোমিয়াম | Chromium | Cr |
a) মৌলের ইংরেজি নামের প্রথম অক্ষর দিয়ে প্রতীক লেখা হয় এবং তা ইংরেজি বর্ণমালার বড় হাতের অক্ষর দিয়ে প্রকাশ করা হয়।
(b) যদি দুই বা দুইয়ের অধিক মৌলের ইংরেজি নামের প্রথম অক্ষর একই হয় তবে একটি মৌলকে নামের প্রথম অক্ষর (ইংরেজি বর্ণমালার বড় হাতের) দিয়ে প্রকাশ করা হয়। অন্যগুলোর ক্ষেত্রে প্রতীকটি দুই অক্ষরে লেখা হয়। নামের প্রথম অক্ষরটি ইংরেজি বর্ণমালার বড় হাতের অক্ষর এবং নামের অন্য একটি অক্ষর ছোট হাতের অক্ষর দিয়ে লেখা হয়।
(c) কিছু মৌলের প্রতীক তাদের ল্যাটিন নাম থেকে নেওয়া হয়েছে।
# বহুনির্বাচনী প্রশ্ন
অণু হলো পদার্থের ক্ষুদ্রতম কণা যাতে পদার্থের সকল গুণাগুণ বিদ্যমান থাকে, যা দুই বা ততোধিক পরমাণুর সমবায়ে গঠিত ।
আর অণুর সংকেত (Chemical Formula) হলো প্রতীকের সাহায্যে অণুর উপাদান ও গঠন সংক্ষিপ্তভাবে প্রকাশের পদ্ধতি, যা মৌল ও যৌগের সংকেত হিসেবে ব্যবহৃত হয় (যেমন: পানির অণু ।
# বহুনির্বাচনী প্রশ্ন
দুই বা ততোধিক মৌলের একাধিক পরমাণু এক সাথে যুক্ত হয়ে যদি একটি মাত্র পরমাণুর মতো আচরণ করে তবে তাকে যৌগমূলক বলে। যৌগমূলকসমূহের যোজনী একটি পরমাণুর মতো হয়ে থাকে। যেমন একটি যৌগমূলক, যার যোজনী ২।
যৌগমূলক ধনাত্মক কিংবা ঋণাত্মক আধানবিশিষ্ট হতে পারে। এদের আধান সংখ্যাই মূলত এদের যোজনী নির্দেশ করে। যেমন: একটি N পরমাণুর সাথে তিনটি H পরমাণু ও একটি H+ যুক্ত হয়ে অ্যামোনিয়াম (NH +) আয়ন নামক যৌগমূলকের সৃষ্টি করে। এর আধান সংখ্যা হলো +1 (এক)। সূতরাং এর যোজনীও 1 (এক)। আধান বা চার্জ ধনাত্মক বা ঋণাত্মক হতে পারে কিন্তু যোজনী শুধু একটি সংখ্যা এর কোনো ধনাত্মক চিহ্ন বা ঋণাত্মক চিহ্ন নেই।
# বহুনির্বাচনী প্রশ্ন
মৌলিক পদার্থের যে ক্ষুদ্রতম কণার মধ্যে মৌলটির সমস্ত ধর্ম উপস্থিত থাকে এবং যা রাসয়ানিক বিক্রিয়ায় অংশগ্রহণ করে তাকে মৌলিক পদার্থটির পরমাণু বলে। সমস্ত কঠিন, তরল, গ্যাস এবং আয়ন -এর গঠনের মূলে রয়েছে নিস্তরিত বা আধানগ্রস্ত পরমাণু। পরমাণুর আকার খুবই ক্ষুদ্র; সাধারনত এরা দৈর্ঘ্যে ১০০ পিকোমিটার (১ মিটারের ১০,০০০,০০০,০০০ ভাগের ১ ভাগ)।
পরমাণুর মাত্রা এই ক্ষুদ্রাকার হওয়ার কারণেই এর আচরনের বৈশিষ্টতা প্রথাগত পদার্থবিদ্যার সূত্র দিয়ে ব্যাখ্যা করা যায় না।
মৌলিক কণিকা (Fundamental Particles)
যে সব সূক্ষ্ম কণিকা দ্বারা পরমাণু গঠিত, তাদেরকে মৌলিক কণিকা বলে। পরমাণুতে তিন ধরনের মৌলিক কণিকা থাকে। যথা- ইলেকট্রন, প্রোটন এবং নিউট্রন।
| ইলেকট্রন | পরমাণুর ক্ষুদ্রতম কণিকা ইলেকট্রন |  |
| প্রকৃত ভর । প্রতীক e- | ||
| চার্জ বা আধান: ঋণাত্মক ( কুলম্ব) | ||
| প্রোটন | একটি হাইড্রোজেন পরমাণু থেকে একটি ইলেকট্রন সরিয়ে নিয়ে যা থাকে তা একটি প্রোটন। এই কারণে প্রোটনের সংকেত । |  |
| প্রকৃত ভর ।প্রতীক P | ||
| চার্জ বা আধান: ধনাত্মক (কুলম্ব) | ||
| নিউট্রন | নিউট্রনের কোনো আধান নাই। Neutral হওয়ার কারণেই এর এই নামকরণ করা হয়েছে। |  |
| প্রকৃত ভর । প্রতীক n |
# বহুনির্বাচনী প্রশ্ন
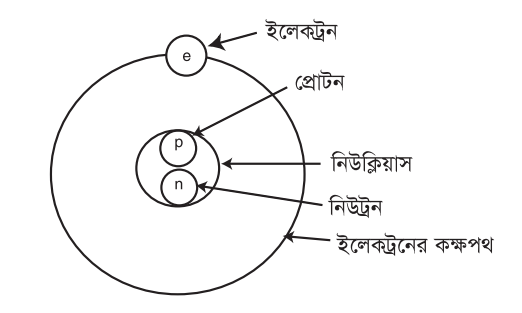
পরমাণুর গঠন (Structure of Atoms)
পরমাণুর একটি কেন্দ্র আছে, যার নাম নিউক্লিয়াস (Necleus)। এই নিউক্লিয়াসে প্রোটন ও নিউট্রন অবস্থান করে। সুতরাং পরমাণুর সকল ধনাত্মক আধান এবং প্রায় সম্পূর্ণ ভরই নিউক্লিয়াসে কেন্দ্রীভূত। ইলেকট্রন নিউক্লিয়াসের বাহিরে থাকে এবং তার চারদিকে ভ্রমণ করে। পরমাণু বৈদ্যুতিক নিরপেক্ষ, কারণ একটি পরমাণুতে যতটি প্রোটন আছে, ততটি ইলকট্রনও আছে। অবশ্য পরমাণু হতে সহজেই ইলেকট্রন বের করে আনা যায় এবং বাহির হতে অতিরিক্ত ইলেকট্রন যোগও করা যায়। তখন আর বিদ্যুৎ নিরপেক্ষ পরমাণু থাকে না, আধানযুক্ত আয়নের সৃষ্টি হয়। ঘর্ষণ, তাপ, রাসায়নিক প্রভৃতি প্রক্রিয়ায় সহজেই পরমাণু থেকে ইলেকট্রন নির্গত হয়।
# বহুনির্বাচনী প্রশ্ন
পরমাণুর ইলেকট্রন বিন্যাস (Electronic configuration of atoms)
পরমাণুতে ইলেকট্রনগুলো যেভাবে সজ্জিত বা বিন্যস্ত থাকে তাই ঐ পরমাণুর ইলেকট্রন বিন্যাস। পরমাণুর প্রতিটি শক্তিস্তরে সর্বোচ্চ ইলেকট্রনের সংখ্যা 2n2।
প্রথম শক্তিস্তরে (n=1) সর্বোচ্চ ইলেকট্রন ধারণক্ষমতা =2n2 = 212 = 2 .
দ্বিতীয় শেলে সর্বোচ্চ ইলেকট্রন ধারণক্ষমতা = 2n = 2 22 = 8
তৃতীয় শেলে সর্বোচ্চ ইলেকট্রন ধারণক্ষমতা = 2n = 2 32 = 18
চতুর্থ শেলে সর্বোচ্চ ইলেকট্রন ধারণক্ষমতা = 2n = 2 42 = 32

পারমাণবিক সংখ্যা (Atomic Number)
নিউক্লিয়াসে অবস্থিত প্রোটনের সংখ্যাকে মৌলের পারমাণবিক সংখ্যা বলা হয়। একে Z দ্বারা প্রকাশ করা হয়। যে কোনো মৌলের স্বাতন্ত্র্য এই সংখ্যার উপর নির্ভর করে। এটি যে কোনো মৌলের মৌলিক ধর্ম। যেমন- কার্বনের পরমাণুতে ৬টি প্রোটন আছে। সুতরাং কার্বনের পারমাণবিক সংখ্যা ৬।
ভর সংখ্যা বা নিউক্লিয়ন সংখ্যা (Mass Number)
নিউক্লিয়াসে অবস্থিত প্রোটন ও নিউট্রনের মোট সংখ্যাকে একটি পরমাণুর ভর সংখ্যা বলা হয়। ভর সংখ্যাকে A দ্বারা প্রকাশ করা হয়। কোনো পরমাণুর অন্তর্গত প্রোটন ও নিউট্রনের মোট সংখ্যাকে ভর সংখ্যা বলা হয়। ভর সংখ্যা A, প্রোটন সংখ্যা P এবং নিউট্রন সংখ্যা N হলে, পরমাণুর ভর সংখ্যা A = P + N। সোডিয়ামের একটি পরমাণুতে প্রোটন আছে ১১টি, নিউট্রন আছে ১২টি। সুতরাং সোডিয়ামের এই পরমাণুর ভর সংখ্যা ২৩।
কতিপয় গুরুত্বপূর্ণ মৌলের পারমাণবিক সংখ্যা ও ভর সংখ্যা
মৌল | পারমাণবিক সংখ্যা | ভর সংখ্যা | মৌল | পারমাণবিক সংখ্যা | ভর সংখ্যা |
| হাইড্রোজেন | ১ | ১ | সিলিকন | ১৪ | ২৮ |
| হিলিয়াম | ২ | ৪ | ক্যালসিয়াম | ২০ | ৪০.০৮ |
| কার্বন | ৬ | ১২ | আর্সেনিক | ৩৩ | ৭৫ |
| সোডিয়াম | ১১ | ২৩ | পারদ | ৮০ | ২০০.৬ |
| ম্যাগনেসিয়াম | ১২ | ২৪ | ইউরেনিয়াম | ৯২ | ২৩৮ |
# বহুনির্বাচনী প্রশ্ন
পর্যায় সারণীর জনক মেন্ডেলিফ। মেন্ডেলিফের পর্যায় সারণীর ভিত্তি ছিল পারমাণবিক ভর। আধুনিক পর্যায় সারণীর ভিত্তি পারমাণবিক সংখ্যা। আধুনিক পর্যায় সারণীতে ৭ টি পর্যায় পর্যায় এবং ৯টি গ্রুপ রয়েছে।
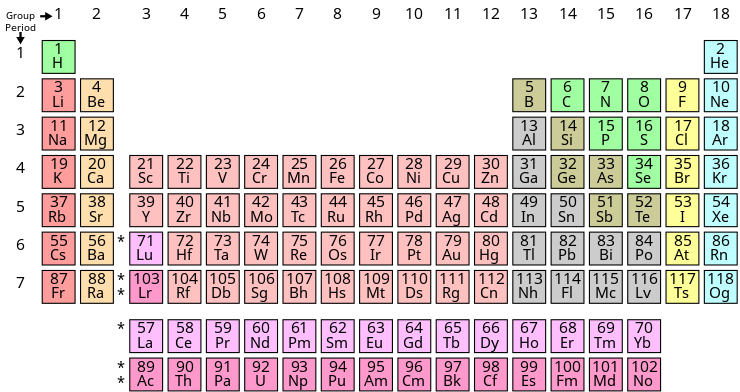
ক্ষার ধাতু (Alkali metal)
যে সকল ধাতু পানির সঙ্গে সরাসরি বিক্রিয়া করে তীব্র ক্ষার গঠন করে, তাকে ক্ষার ধাতু বলে। ক্ষার ধাতুগুলোর নাম লিথিয়াম, সোডিয়াম, পটাসিয়াম, রুবিডিয়াম এবং সিজিয়াম। পর্যায় সারণিতে ক্ষার ধাতুগুলোর অবস্থান IA গ্রুপে।
মৃৎক্ষার ধাতু (Mrtksara metal)
যে সকল ধাতু ভূ-ত্বকের মৃত্তিকার উপাদানরূপে পাওয়া যায় এবং পানির সঙ্গে বিক্রিয়া করে ক্ষারক গঠন করে, তাকে মৃৎক্ষার ধাতু বলে। উদাহরণ: ক্যালসিয়াম, ম্যাগনেসিয়াম। পর্যায় সারণিতে মৃৎক্ষার ধাতুগুলোর অবস্থান IIA গ্রুপে।
নিষ্ক্রিয় গ্যাস (Noble gas)
পর্যায় সারণির শূন্য গ্রুপের মৌলসমূহ রাসায়নিকভাবে নিষ্ক্রিয় এবং কক্ষ তাপমাত্রায় গ্যাসীয়। এদের নিষ্ক্রিয় গ্যাস বলে। নিষ্ক্রিয় গ্যাস ৬টি, যথা- হিলিয়াম (He), নিয়ন (Ne), আর্গন (Ar), ক্রিপ্টন (Kr), জেনন (Xe) এবং রেডন (Rn)। নিষ্ক্রিয় গ্যাসসমূহের সর্ববহিঃস্থ স্তরে ৮টি ইলেকট্রন থাকে (ব্যতিক্রম: হিলিয়াম)।
হিলিয়ামের সর্ববহিঃস্থ স্তরে ২টি ইলেকট্রন থাকে। মৌলিক গ্যাস' (হাইড্রোজেন (H2), অক্সিজেন (O2)] এর অণুসমূহ দ্বিপরমাণুক। কিন্তু নিষ্ক্রিয় গ্যাসের অণুসমূহ এক পরমাণুক। যেমন: হিলিয়াম (He), নিয়ন (Ne)। মৌলিক গ্যাস র্যাডন সর্বাপেক্ষা ভারি। রেডন তেজস্ক্রিয় মৌল। বিজ্ঞানী ডর্ন ১৯০০ সালে রেডিয়ামের তেজস্ক্রিয় বিভাজন হতে রেডন আবিষ্কার করেন। সূর্যে মৌলিক পদার্থের মধ্যে হিলিয়াম (He) এর পরিমাণ সবচেয়ে বেশি।
ব্যবহার
- বেলুনে এবং ডুবুরিদের জন্য হাইড্রোজেনের পরিবর্তে হিলিয়াম ব্যবহার করা। হাইড্রোজেন হিলিয়াম অপেক্ষা হালকা হলেও হাইড্রোজেন দাহ্য পক্ষান্তরে হিলিয়াম নিষ্ক্রিয়।
- সাধারণ বৈদ্যুতিক বাল্বের ভিতরে সাধারণত নাইট্রোজেন গ্যাস ব্যবহার করা হয়। কিন্তু টিউব লাইটে সাধারণত নিয়ন, আর্গন প্রভৃতি গ্যাস ব্যবহৃত হয়।
- ফটোগ্রাফিক ফ্লাশ লাইটে জেনন গ্যাস ব্যবহৃত হয়।
# বহুনির্বাচনী প্রশ্ন
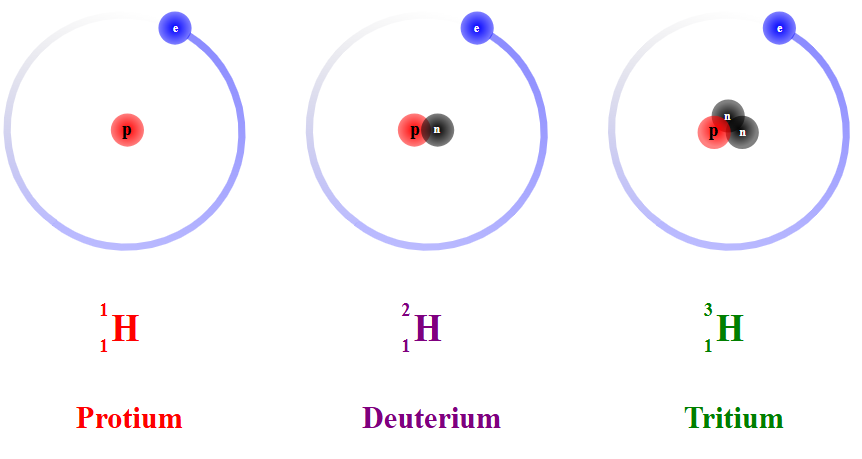
আইসোটোপ
যে সকল পরমাণুর পারমাণবিক সংখ্যা সমান কিন্তু ভর সংখ্যা ভিন্ন, তাদেরকে পরস্পরের আইসোটোপ বলা হয়। অন্যভাবে বলা যায়, এটমিক সংখ্যা একই হওয়া সত্ত্বেও নিউক্লিয়াসের নিউট্রন সংখ্যা বেশি হওয়ার ফলে ভরসংখ্যা বেড়ে যায়, তাদেরকে পরস্পরের আইসোটোপ বলা হয়। যেমন: হাইড্রোজেনের আইসোটোপগুলো হলো প্রোটিয়াম (1H1), ডিউটেরিয়াম (2H1) ও ট্রিটিয়াম (3H1)। হাইড্রোজেন, ডিউটেরিয়াম এবং ট্রিটিয়াম তিনটিরই পারমাণবিক সংখ্যা 1 কিন্তু ভর সংখ্যা যথাক্রমে 1, 2 এবং 3। লক্ষণীয়, হাইড্রোজেন পরমাণুতে কোনো নিউট্রন থাকে না। ইউরেনিয়ামের তিনটি আইসোটোপ (234U92), (235U92), (238U92) । পারমাণবিক চুল্লীতে বহুল ব্যবহৃত আইসোটোপ (235U92)|
# বহুনির্বাচনী প্রশ্ন
আইসোটোন (Isotone)
যে সকল পরমাণুর নিউট্রন সংখ্যা সমান কিন্তু প্রোটন সংখ্যা ও ভর সংখ্যা ভিন্ন, তাদেরকে পরস্পরের আইসোটোন বলে। যেমন: সিলিকন (30Si14), ফসফরাস (31P15) এবং সালফার (32S16) পরস্পরের
আইসোটোন কারণ
সিলিকনের নিউট্রন সংখ্যা = 30 - 14 = 16
ফসফরাসের নিউট্রন সংখ্যা = 31 - 15 = 16
সালফারের নিউট্রন সংখ্যা = 32 - 16 = 16
কিন্তু এ সকল মৌলের প্রোটন সংখ্যা এবং ভর সংখ্যা ভিন্ন।
# বহুনির্বাচনী প্রশ্ন
যে সকল পরমাণুর ভর সংখ্যা সমান কিন্তু প্রোটন সংখ্যা ভিন্ন, তাদেরকে পরস্পরের আইসোবার বলা হয়। যেমন: কপার (64Cu29) এবং জিংক (64Zn30) পরস্পরের আইসোবার কারণ উভয়ের ভরসংখ্যা 64 কিন্তু প্রোটন সংখ্যা যথাক্রমে 29 এবং 30।
# বহুনির্বাচনী প্রশ্ন
প্রস্তর যুগের পর আসে ধাতুর ব্যবহারের যুগ। খ্রিষ্টপূর্ব ৩৫০০ অব্দের পর পাথরের পর তামার ব্যবহার শুরু হয়। লোহার আবিষ্কার হয় খ্রিষ্টপূর্ব ১৫০০ অব্দে।
ধাতু (Metal)
যে সকল পদার্থ দেখতে চকচকে, তাপ ও বিদ্যুৎ সুপরিবাহী, আঘাত করলে টুনটুন শব্দ হয়, ঘাতসহ প্রসারণশীল ও নমনীয় তাদেরকে ধাতু বলে। এদের পরমাণু ইলেকট্রন ত্যাগ করে ক্যাটায়ন উৎপন্ন করে। উদাহরণ: লিথিয়াম, সোডিয়াম, পটাসিয়াম, ক্যালসিয়াম, ম্যাগনেসিয়াম, অ্যালুমিনিয়াম, দস্তা (Zinc), সোনা, রূপা, তামা (Cupper), প্লাটিনাম, পারদ (Mercury), টাংস্টেন প্রভৃতি।
বৈশিষ্ট্য | ধাতু | বৈশিষ্ট্য | ধাতু |
| সবচেয়ে হালকা ধাতু | লিথিয়াম (Li) | সবচেয়ে সক্রিয় ধাতু | পটাসিয়াম (K) |
| সবচেয়ে ভারী ধাতু | প্লাটিনাম (Pt) | সবচেয়ে তাড়াতাড়ি ক্ষয়প্রাপ্ত হয় | দস্তা (Zn) |
| সবচেয়ে মূল্যবান ধাতু | তার বানানো সহজতর | তামা (Cu) | |
| সর্বোচ্চ গলনাঙ্কের ধাতু | টাংস্টেন | সর্বনিম্ন গলনাঙ্কের ধাতু | পারদ (Hg) |
# বহুনির্বাচনী প্রশ্ন
সোডিয়াম (আধুনিক ল্যাটিন ভাষায় ন্যাট্রিয়াম) একটি মৌলিক পদার্থ যার প্রতীক Na এবং পারমাণবিক সংখ্যা ১১। এটি পর্যায় সারণীর তৃতীয় পর্যায়ে, প্রথম শ্রেণীতে অবস্থিত, যার কারণে এটি ক্ষার ধাতু হিসাবে পরিগণিত। তীব্র সক্রিয়তার কারণে একে প্রকৃতিতে আলাদাভাবে পাওয়া যায় না, সোডালাইট, ফেল্ডস্পার, রকসল্ট ইত্যাদি খনিজ রূপে পাওয়া যায়। মহাবিশ্বে এর উৎপত্তি হয় নক্ষত্রে, ৬০০ মেগাকেলভিন তাপমাত্রায় কার্বন দহন প্রক্রিয়ার মাধ্যমে যখন দুটি কার্বন পরমাণুর মধ্যে ফিউশান ঘটে।
# বহুনির্বাচনী প্রশ্ন
পটাশিয়াম হলো একটি রাসায়নিক উপাদান যা K প্রতীক দ্বারা প্রকাশ করা হয় ( নিও-ল্যাটিন ক্যালিয়াম থেকে ) এবং এর পারমাণবিক সংখ্যা ১৯ ৷ পটাশিয়াম হলো একটি রুপালি-সাদা ধাতু যা একটি ছুরির মাধ্যমে সামান্য শক্তি দিয়ে কাটার জন্য যথেষ্ট নরম।
অ্যালুমিনিয়াম একটি মৌলিক পদার্থ যার প্রতীক Al এবং পারমাণবিক সংখ্যা ১৩। এটি বোরন গ্রুপের সদস্য যার রং ধূসর সাদা; গঠনে কোমল, অচৌম্বকীয় এবং যথেষ্ট সংকোচন-প্রসারণক্ষম। ভর অনুপাতে ভূ-পৃষ্ঠের ৮ শতাংশ অ্যালুমিনিয়াম। অক্সিজেন ও সিলিকনের পর ভূ-পৃষ্ঠের মৌল হিসেবে এর অবস্থান ৩য়, যদিও ভূপৃষ্ঠের গভীরে নগন্য মাত্রায় বিদ্যমান। এর প্রধান আকরিক হল বক্সাইট। রাসায়নিকভাবে অ্যালুমিনিয়াম খুবই সক্রিয় বলে তীব্র বিজারনীয় পরিবেশ ছাড়া একে বিশুদ্ধ অবস্থায় পাওয়া যায় না। একারণে ২৭০ ধরনের ভিন্ন পদার্থে এর উপস্থিতি রয়েছে।
এটি বেশ হালকা ও দীর্ঘদিন ব্যবহারে অক্ষয়িষ্ণু। একারণে এর বহুবিধ ব্যবহার লক্ষ্য করা যায়। মহাকাশীয় যন্ত্রপাতি, যানবাহন ও নির্মানকাজে (জানালার কাঠামো, আংটা ইত্যাদি) অ্যালুমিনিয়াম ও এর সংকর ধাতুসমূহের বহুল ব্যবহার লক্ষনীয়। এর অক্সাইড ও সালফেটসমূহ সবচেয়ে বেশি ব্যবহৃত যৌগ। কোন জীবন্ত প্রাণী তাদের জৈবিক কার্যাবলিতে অ্যালুমিনিয়ামের লবণ ব্যবহার না করলেও মাটিতে প্রচুর পরিমাণে থাকায় উদ্ভিদসমূহে তাদের ভূমিকা রয়েছে।উদ্ভিদে এর ক্রিয়াবলি নিয়ে উপর্যুপরি গবেষণা চলছে।

# বহুনির্বাচনী প্রশ্ন
অ্যালুমিনিয়াম
দস্তা
লোহা
তামা
ক্যালশিয়াম হচ্ছে Ca প্রতীকযুক্ত একটি মৌলিক পদার্থ, যার পারমাণবিক সংখ্যা ২০। ক্যালসিয়াম একটি ক্ষারীয় ধাতব পদার্থ। এজন্য ক্যালসিয়াম বেশ সক্রিয় ধাতু, যা বায়ুর সংস্পর্শে আসার পরে গাঢ় অক্সাইড-নাইট্রাইড স্তর গঠন করে। এর গাঠনিক ও রাসায়নিক বৈশিষ্ট্যগুলির অধিকাংশই মিলে যায় এর চেয়ে কিছু ভারি ও সদৃশ মৌল স্ট্রনশিয়াম এবং বেরিয়ামের সাথে। পরিমাণের দিক থেকে এটি পৃথিবীর ভূত্বকের উপাদানগুলোর ভেতরে পঞ্চম অবস্থানে আছে। একইসাথে প্রাচুর্যের দিক থেকে পৃথিবীতে প্রাপ্ত ধাতুসমূহের ভেতরে এটি তৃতীয় অবস্থানে আছে, অর্থাৎ লোহা এবং অ্যালুমিনিয়ামের পরই এর অবস্থান। পৃথিবীতে সর্বাধিক পরিমাণে পাওয়া যায় এমন ক্যালসিয়াম যৌগটি হলো ক্যালসিয়াম কার্বোনেট, যা চুনাপাথর নামে পরিচিত। এটি সমুদ্রে প্রাপ্ত জীবাশ্মের অবশিষ্টাংশে পাওয়া যায়, যে জীবাশ্মগুলো সৃষ্ট হয়েছিলো সমুদ্র সৃষ্টির প্রারম্ভিক সময়ে। এর পাশাপাশি জিপসাম, অ্যানহাইড্রাইট, ফ্লোরাইট এবং অ্যাপাটাইট ক্যালসিয়ামের উৎস। ক্যালসিয়াম নামটি লাতিন শব্দ Calx Lime থেকে এসেছে। তৎকালে চুনাপাথরকে উত্তপ্ত করলে এটি পাওয়া যেত।

দস্তা বা জিংক হলো একটি মৌলিক পদার্থ, যার প্রতীক Zn এবং পারমাণবিক সংখ্যা ৩০। এর পারমাণবিক ভর ৬৫.৩৮ (সাধারণ কাজে ৬৫ ব্যবহার করা হয়)। এটি পর্যায় সারণীর চতুর্থ পর্যায়ে, দ্বাদশ গ্রুপে অবস্থিত। এটি একটি ডি-ব্লক মৌল হলেও এর d-অরবিটাল পূর্ণ থাকায় এটি সাধারণত অবস্থান্তর ধাতু হিসেবে বিবেচিত হয়না। গ্যালভানাইজিং করতে প্রচুর পরিমাণে জিঙ্ক ব্যবহৃত হয়।
জিংক বর্ণালী
পিতল, বিভিন্ন অনুপাতে তামা এবং দস্তার মিশ্রণ, খ্রিস্টপূর্ব তৃতীয় সহস্রাব্দের আগে এজিয়ান, ইরাক, সংযুক্ত আরব আমিরাত, কাল্মেকিয়া, তুর্কমেনিস্তান ও জর্জিয়ায় এবং দ্বিতীয় সহস্রাব্দে পশ্চিম ভারত, উজবেকিস্তান, ইরান, সিরিয়া, ইরাক এবং প্যালেস্তাইনে ব্যবহৃত হয়েছে।

# বহুনির্বাচনী প্রশ্ন
লোহা বা লৌহ একটি ধাতব মৌলিক পদার্থ। এর রাসায়নিক চিহ্ন Fe, পারমাণবিক সংখ্যা ২৬, পারমাণবিক ভর ৫৫.৮৫, যোজ্যতা ২ ও ৩। লোহার ঘনত্ব ৭.৮৫ গ্রাম/সিসি অর্থাৎ জলের থেকে ৭.৮৫ গুণ ভারি। এর গলনাঙ্ক ১৫৩৮° সেলসিয়াস এবং স্ফুটনাঙ্ক ২৮৬২° সেলসিয়াস। লোহাকে প্রকৃতিতে মুক্ত অবস্থায় পাওয়া যায় না। আকরিক থেকে লোহা নিষ্কাশন করা হয়। লোহার প্রধান আকরিকগুলি হলো, হেমাটাইট (Hematite, Fe2O3), ম্যাগনেটাইট (Magnetite, Fe3O4), আয়রন পাইরাইটিস (Iron Pyrites, FeS2) ও সিডারাইট (Siderite,FeCO3), লিমোনাইট (Fe2O3.3H2O)। পৃথিবীর বিভিন্ন স্থানে প্রচুর লোহার আকরিক পাওয়া যায়। ভূ-ত্বকে লোহার পরিমাণ শতকরা ৪.১২ ভাগ।

# বহুনির্বাচনী প্রশ্ন
পারদ (Mercury)
সর্বাপেক্ষা নিম্ন গলনাঙ্কবিশিষ্ট ধাতু পারদ। এটি স্বাভাবিক তাপমাত্রায় তরল অবস্থায় থাকে। তরল পদার্থগুলোর মধ্যে পারদ সর্বাপেক্ষা ভারী। পারদের প্রতীক Hg । থার্মোমিটারে পারদ রহুলভাবে ব্যবহৃত হয় কারণ অল্প তাপে পারদের আয়তন অনেক বেশি বৃদ্ধি পায়। ফলে তাপমাত্রার সহজে সূক্ষ্মভাবে মাপা যায়।
জেনে রাখা ভাল
১. সোডিয়াম পোড়ালে উজ্জ্বল হলুদ বর্ণের শিখা উৎপন্ন হয়।
২. বৈদ্যুতিক বাল্বের ফিলামেন্টে টাংস্টেন ব্যবহৃত হয়।
৩. বিশুদ্ধ সোনা ২৪ ক্যারেট।
# বহুনির্বাচনী প্রশ্ন
দুই বা ততোধিক ধাতু পরস্পরের সাথে মিশে যে সমসত্ব বা অসমসত্ব মিশ্রণ উৎপন্ন করে, সেই কঠিন ধাতব পদার্থকে সংকর ধাতু (Alloy) বলে। যেমন: কাঁসা হলো কপার ও টিনের সংকর ধাতু।
সংকর ধাতু | মিশ্রণ |
| ঢালাই লোহা বা কাস্ট আয়রন | লোহার সাথে ২-৪.৫৬% কার্বন থাকে। একে পিগ আয়রনও বলে। |
| ইস্পাত (Steel) | লোহার সাথে সুনিয়ন্ত্রিত পরিমাণ কার্বন থাকে। এতে কার্বনের শতকরা পরিমাণ ০.১৫ - ১.৫%। |
| স্টেইনলেস স্টিল Stainless Stell | লোহা (Fe)- ৭৩% + ক্রোমিয়াম (Cr) ১৮% + নিকেল (Ni)- ৮% + কার্বন (C)- ১% |
| ব্রোঞ্জ (Bronze) | ৯০% তামা + ১০% টিন |
| পিতল (Brass) | তামা ৮০% + দস্তা (জিঙ্ক) - ২০% |
| গান মেটাল | তামা ৮৮% + ১০% টিন+ দস্তা (জিঙ্ক) - ২% |
| ডুরালামিন | অ্যালুমিনিয়ামের সাথে মেশানো হয় কপার, ম্যাগনেসিয়াম এবং ম্যাঙ্গানিজ। |
| নাইক্রোম | নিকেল-৬০% + আয়রন-২৫% + ক্রোমিয়াম-১৫% |
| বৈদ্যুতিক ইস্ত্রি এবং হিটারে নাইক্রোম তার ব্যবহার করা হয়। | |
| টাইপ মেটাল | সীসা ৭৫% + অ্যান্টিমনি ২০% + টিন ৫% |
# বহুনির্বাচনী প্রশ্ন
বহুরূপতা
প্রকৃতিতে একই মৌলের বিভিন্ন ভৌত রূপে অবস্থান করার প্রবণতাকে বহুরূপতা বলে। কার্বন, ফসফরাস, সিলিকন, সালফার, জার্মেনিয়াম, নাইট্রোজেন, অক্সিজেন, টিন, বোরন ইত্যাদি মৌল বহুরূপতা প্রদর্শণ করে।
ক্যাটেনেশন
একই মৌলের পরমাণুসমূহের মধ্যে বন্ধন সৃষ্টির মাধ্যমে বিভিন্ন দৈর্ঘ্যের শিকল গঠনের ধর্মকে ক্যাটেনেশন বলা হয়। ক্যাটেনেশন ধর্ম দ্বারা কার্বন পরমাণুসমূহ নিজেদের মধ্যে একক বন্ধন, দ্বিবন্ধন বা ত্রিবন্ধন দ্বারা বিভিন্ন দৈর্ঘ্যের কার্বন পরমাণু শিকল ও বলয় গঠন করে বিভিন্ন জৈব যৌগ সৃষ্টি করতে পারে। এজন্য জৈব যৌগের সংখ্যা ২০ লক্ষাধিক। অজৈব যৌগের মধ্যে শুধুমাত্র সিলিকনে কিছুটা ক্যাটেনেশন দেখা যায়।
কার্বন (কার্বনের বহুমুখী ব্যবহার)
কার্বন অধাতু এবং বিজারক। কাঠ ও কয়লা প্রধানত কার্বন। আবার, হীরক এবং গ্রাফাইট হলো কার্বনের দুটি রূপভেদ। প্রকৃতিতে প্রাপ্ত সবচেয়ে কঠিন পদার্থ হীরক। হীরক কাঁচ কাটতে ব্যবহৃত হয়। হীরক বিদ্যুৎ অপরিবাহী কারণ এতে কোনো মুক্ত ইলেকট্রন থাকে না। গ্রাফাইট অধাতু হলেও তাপ ও বিদ্যুৎ পরিবহনে সক্ষম। বিভিন্ন গ্রেডের (2B, HB, 2H, HH) উড পেন্সিলের 'সীস' হিসেবে গ্রাফাইট ব্যবহৃত হয়। এছাড়াও সোডিয়াম ধাতুর নিষ্কাশনে গ্রাফাইট অ্যানোড হিসেবে ব্যবহৃত হয়।
অধাতু সাধারণত ভঙ্গুর, তাপ ও বিদ্যুৎ অপরিবাহী এবং আঘাত করলে কোনো শব্দ উৎপন্ন করে না। এগুলো চকচকে হয় না, কম গলনাঙ্ক ও স্ফুটনাঙ্কবিশিষ্ট, এবং কঠিন, তরল বা গ্যাসীয় অবস্থায় থাকতে পারে । এরা ইলেকট্রন গ্রহণ করে ঋণাত্মক আয়নে (অ্যানায়ন) পরিণত হয় এবং তাদের অক্সাইডগুলো সাধারণত অম্লীয় প্রকৃতির হয়।
কার্বন (কার্বনের বহুমুখী ব্যবহার)
কার্বন অধাতু এবং বিজারক। কাঠ ও কয়লা প্রধানত কার্বন। আবার, হীরক এবং গ্রাফাইট হলো কার্বনের দুটি রূপভেদ। প্রকৃতিতে প্রাপ্ত সবচেয়ে কঠিন পদার্থ হীরক। হীরক কাঁচ কাটতে ব্যবহৃত হয়। হীরক বিদ্যুৎ অপরিবাহী কারণ এতে কোনো মুক্ত ইলেকট্রন থাকে না। গ্রাফাইট অধাতু হলেও তাপ ও বিদ্যুৎ পরিবহনে সক্ষম। বিভিন্ন গ্রেডের (2B, HB, 2H, HH) উড পেন্সিলের 'সীস' হিসেবে গ্রাফাইট ব্যবহৃত হয়। এছাড়াও সোডিয়াম ধাতুর নিষ্কাশনে গ্রাফাইট অ্যানোড হিসেবে ব্যবহৃত হয়।
কার্বন ডাই অক্সাইড (CO2)
কার্বন ডাই অক্সাইড একটি এসিডধর্মী গ্যাস। পানিতে কার্বন ডাই অক্সাইডের দ্রবণকে সোডা ওয়াটার বলে। কার্বন ডাই অক্সাইড গ্যাসকে অত্যধিক চাপে তরল করে সোডা ওয়াটার তৈরি করা হয়। আবার হিমায়িত কঠিন কার্বন ডাই অক্সাইডকে শুষ্ক বরফ (Dry Ice) বলা হয়। অগ্নি নির্বাপক সিলিন্ডারে তরল কার্বন ডাই-অক্সাইড ব্যবহার করা হয়। রাসায়নিক অগ্নি নির্বাপক অগ্নিতে অক্সিজেন সরবরাহে প্রতিবন্ধকতা সৃষ্টি করে।
| গ্যাস | নিজে জ্বলে | অন্যকে জ্বলতে সাহায্য করে |
| কার্বন ডাই অক্সাইড | x | x |
| হাইড্রোজেন | ✓ | x |
| অক্সিজেন | x | ✓ |
কার্বন মনোক্সাইড (CO)
গাড়ি থেকে নির্গত কালো ধোঁয়ায় বিষাক্ত কার্বন মনোক্সাইড গ্যাস থাকে। কার্বন মনোক্সাইড হিমোগ্লোবিনের অক্সিজেন পরিবহন ক্ষমতা হ্রাস করে।
গ্যাস | রাসায়নিক নাম | সংকেত |
| ওয়াটার গ্যাস | কার্বন মনোক্সাইড ও হাইড্রোজেন গ্যাস | CO + H2 |
| প্রোডিউসার গ্যাস | কার্বন মনোক্সাইড ও নাইট্রোজেন গ্যাস | 2CO + N2 |
# বহুনির্বাচনী প্রশ্ন
অক্সিজেন (O)
বৃটিশ যাজক যোসেফ প্রিস্টলি সর্বপ্রথম ১৭৭৪ খ্রিস্টাব্দে অক্সিজেন আবিষ্কার করেন। অক্সিজেনের একটি বিশেষ ধর্ম হল ইহা নিজে জ্বলেনা কিন্তু অন্যকে জ্বলতে সাহায্য করে। যে পানিতে কঠিন বস্তু (লবণ) বেশি দ্রবীভূত থাকে সে পানিতে অক্সিজেনের পরিমাণ কম। যেমন: সমুদ্রের পানিতে কঠিন বস্তু (লবণ) দ্রবীভূত থাকে কিন্তু নদীর পানিতে থাকে না। ফলে সমুদ্রের পানি, ভূগর্ভস্থ পানির তুলনায় নদীর পানিতে অক্সিজেনের পরিমাণ বেশি। হাসপাতালে ব্যবহৃত অক্সিজেনে অক্সিজেনের পরিমাণ শতকরা ৯৩ ভাগ। বায়ুমণ্ডলে অক্সিজেনের পরিমাণ ২১.০১%। ওজোন (O3) অক্সিজেনের একটি রূপভেদ। বায়ুমণ্ডলে ওজোনের পরিমাণ ০.০০০১%, ওজোনের রং গাঢ় নীল।
# বহুনির্বাচনী প্রশ্ন
নাইট্রোজেন (N)
আকাশে বিদ্যুৎ ক্ষরণের ফলে নাইট্রোজেনের অক্সাইডসমূহ তৈরি হয়, যা পানির সাথে মিশে নাইট্রিক এসিড উৎপন্ন করে। এ নাইট্রিক এসিড বৃষ্টির পানির সাথে মিশে মাটিতে পতিত হয় এবং জমির ক্ষারীয় উপাদানের সাথে বিক্রিয়া করে নাইট্রেট লবণ উৎপন্ন করে। উদ্ভিদ এ নাইট্রেট গ্রহণ করে তাকে প্রোটিনে রূপান্তরিত করে, যা প্রাণিসকল গ্রহণ করে। উদ্ভিদ ও প্রাণির জীবন অবসানের পর পচন ক্রিয়ায় প্রোটিনের কিছু অংশ নাইট্রোজেন গ্যাসে পরিণত হয়। এভাবে প্রকৃতিতে "নাইট্রোজেন চক্র" চলে।
# বহুনির্বাচনী প্রশ্ন
ফসফরাস (P)
ফসফরাসের দুটি রূপভেদ আছে। যথা- লোহিত ফসফরাস ও শ্বেত ফসফরাস। শ্বেত ফসফরাস বেশি সক্রিয়। শ্বেত ফসফরাসের গন্ধ রসুনের মত। দিয়াশলাইয়ের কাঠির মাথায় লোহিত ফসফরাস ব্যবহৃত হয়। দিয়াশলাইয়ের বক্সের দু-ধারে কাগজের উপর যে বারুদ থাকে তা আসলে কাঁচচূর্ণ মিশ্রিত ফসফরাস। ফসফরাস পেন্টাক্সাইড (P2O5) নিরুদক হিসেবে ব্যবহৃত হয়। গ্যাস মাস্কের প্রধান উপাদান ফসফরাস পেন্টাক্সাইড।
সিলিকন (Si)
সিলিকার রাসায়নিক নাম সিলিকন ডাই অক্সাইড (SiO2)। সিলিকার বিশুদ্ধ রূপ কোয়ার্টজ। কোয়ার্টজ ঘড়িতে সিলিকা ব্যাপকভাবে ব্যবহৃত হয়। কাচ তৈরির প্রধান কাঁচামাল হলো বালি। বালির প্রধান উপাদান হলো সিলিকা। কাচ রাসায়নিকভাবে অত্যন্ত নিষ্ক্রিয়। কাঁচ বহুদিন রোদে বা পানিতে থাকলে নষ্ট, ক্ষয় বা বৃদ্ধি হয় না।
# বহুনির্বাচনী প্রশ্ন
হ্যালোজেন শব্দের অর্থ 'সামুদ্রিক লবণ উৎপাদক'। হ্যালোজেন বলতে ফ্লোরিন (F2), ক্লোরিন (Cl2), ব্রোমিন (Br2) এবং আয়োডিন (I2) এ চারটি মৌলকেই বোঝায়। সামুদ্রিক শৈবালে আয়োডিন পাওয়া যায়। পান করা পানির সাথে ক্লোরিন মিশানো হয় কারণ ক্লোরিন পানিতে থাকা ক্ষতিকর ব্যাক্টেরিয়া ধ্বংস করে। হ্যালোজেন এসিড শক্তির ক্রম: HI > HBr > HCI > HF পর্যায় সারণিতে হ্যালোজেনগুলোর VIIA গ্রুপে অবস্থান করে।
নিষ্ক্রিয় গ্যাস (Noble Gas): পর্যায় সারণির শূন্য গ্রুপের মৌলসমূহ রাসায়নিকভাবে নিষ্ক্রিয় এবং কক্ষ তাপমাত্রায় গ্যাসীয়। এদের নিষ্ক্রিয় গ্যাস বলে। নিষ্ক্রিয় গ্যাস ৭টি যথা- হিলিয়াম (He), নিয়ন (Ne), আর্গন (Ar), ক্রিপ্টন (Kr), জেনন (Xe) এবং রেডন (Rn) এবং ওগানেসন । নিষ্ক্রিয় গ্যাসমূহের সর্ববহিঃস্থ স্তরে ৮টি ইলেকট্রন থাকে। ব্যতিক্রম হিলিয়াম। হিলিয়ামের সর্ববহিঃস্থ স্তরে ২টি ইলেকট্রন থাকে। সূর্যে মৌলিক পদার্থের মধ্যে হিলিয়াম (He) এর পরিমাণ সবচেয়ে বেশি। রেডন তেজষ্ক্রিয় মৌল। বিজ্ঞানী ডর্ন ১৯০০ সালে রেডিয়ামের তেজষ্ক্রিয় বিভাজন হতে রেডন আবিষ্কার করেন।
নিষ্ক্রিয় গ্যাসের সংখ্যা সাত। এগুলো হল: হিলিয়াম, নিয়ন, আর্গন, ক্রিপ্টন, জেনন, র্যাডন এবং ওগানেসন। একে নোবেল গ্যাস বলা হয় ।
ব্যবহার
(১) হাইড্রোজেন হিলিয়াম অপেক্ষা হালকা হলেও হাইড্রোজেন দাহ্য পক্ষান্তরে হিলিয়াম নিষ্ক্রিয়। এজন্য বেলুনে এবং ডুবুরিদের জন্য হাইড্রোজেনের পরিবর্তে হিলিয়াম ব্যবহার করা হয়।
(২) ফটোগ্রাফিক ফ্লাশ লাইটে জেনন গ্যাস ব্যবহৃত হয়।
# বহুনির্বাচনী প্রশ্ন
সালফিউরিক এসিড (H2SO4)
সালফিউরিক এসিডের একটি অণুতে মোট ৭টি (২টি হাইড্রোজেন, ১টি সালফার, ৪টি অক্সিজেন) পরমাণু থাকে। ১০০% বিশুদ্ধ সালফিউরিক এসিডকে সালফান এবং ধূমায়মান সালফিউরিক এসিডকে ওলিয়াম (H2S2O7) বলে। সালফিউরিক এসিড রাসায়নিক পদার্থসমূহের রাজা বলা হয় কারণ প্রায় প্রত্যেক শিল্পে কোনো না কোনো স্তরে H2SO4 এসিড ব্যবহৃত হয়।
হাইড্রোজেন সালফাইড (H2S)
হাইড্রোজেন সালফাইড বর্ণহীন, পঁচা ডিমের গন্ধযুক্ত একটি গ্যাস। এটি পানিতে খুব সামান্য পরিমাণে দ্রবীভূত হয়। ১৭৭৭ সালে সুইডিশ রসায়নবিদ কার্ল উইলহেম শিলি হাইড্রোজেন সালফাইড আবিষ্কার করেন।
# বহুনির্বাচনী প্রশ্ন
নাইট্রিক এসিড (HNO3)
স্বর্ণ থেকে খাদ বের করতে নাইট্রিক এসিড ব্যবহার করা হয়। এক মোল গাঢ় নাইট্রিক এসিড (HNO3) এবং তিন মোল গাঢ় হাইডোক্লোরিক এসিডের (HCI) মিশ্রণকে অ্যাকোয়া রেজিয়া বা রাজ-অম্ল বলে। স্বর্ণ, প্লাটিনাম প্রভৃতি অভিজাত ধাতুসমূহ যে কোনো গাঢ়তার হাইড্রোক্লোরিক এসিড বা নাইট্রিক এসিডে দ্রবীভূত হয় না, কিন্তু এরা অ্যাকোয়া রেজিয়া বা রাজ অম্লে দ্রবীভূত হয়। 96-98% ঘনমাত্রার নাইট্রিক এসিডে অধিক নাইট্রোজেন ডাই অক্সাইড (NO2) দ্রবীভূত থাকে। NO2 গ্যাস বের হয়ে বায়ুতে ধোয়া উৎপন্ন করে। তাই এই ঘনমাত্রার নাইট্রিক এসিডকে ধূমায়মান নাইট্রিক এসিড বলে।
# বহুনির্বাচনী প্রশ্ন
নাইট্রোজেন অক্সাইড
নাইট্রাস অক্সাইড (N2O) এর মৃদু মিষ্টি গন্ধ আছে। নিশ্বাসের সাথে এটি অল্প পরিমাণ গ্রহণ করলে হাসির উদ্রেক করে। এজন্য একে লাফিং গ্যাস বলে। মৃদু চেতনানাশকরূপে N₂O ব্যবহার করা হয়।
এসিড বৃষ্টি (Acid Rain)
শিল্প সমৃদ্ধ এলাকায় সাধারণত এসিড বৃষ্টি দেখা যায়। বায়ুতে শিল্প কারখানা হতে নির্গত সালফার ডাই অক্সাইড (প্রধানত), নাইট্রোজেনের বিভিন্ন অক্সাইড এবং সালফিউরিক এসিড বাষ্প বেশি থাকলে বৃষ্টির সময় ঐ এসিড বাষ্প পানির সাথে যুক্ত হয়ে এসিড বৃষ্টির সৃষ্টি করে। এসিড বৃষ্টির ফলে পরিবেশের ব্যাপক ক্ষতি হয়।
রাসায়নিক বিক্রিয়া (Chemical Actions)
যদি কোনো পরিবর্তনের ফলে কোনো পদার্থ তার নিজের ধর্ম ও বৈশিষ্ট্য হারিয়ে নতুন ধর্ম লাভ করে সেই পরিবর্তনকে রাসায়নিক পরিবর্তন বলে। যে প্রক্রিয়ায় রাসায়নিক পরিবর্তন ঘটে সেই প্রক্রিয়াকে রাসায়নিক বিক্রিয়া বলে। রাসায়নিক বিক্রিয়াকে সংক্ষেপে উপস্থাপন করার জন্য যে সমীকরণ ব্যবহার করা হয় সেই সমীকরণকে রাসায়নিক সমীকরণ বলা হয়।
রাসায়নিক সমীকরণকে প্রকাশ করার জন্য প্রতীক, সংকেত এবং নানা রকম চিহ্ন ব্যবহার করা হয়।
যে সকল পদার্থ নিয়ে রাসায়নিক বিক্রিয়া শুরু করা হয় সেই সকল পদার্থকে বলা হয় বিক্রিয়ক। বিক্রিয়ার ফলে নতুন ধর্ম বিশিষ্ট যে সকল পদার্থ উৎপন্ন হয় সেই সকল পদার্থকে উৎপাদ বলা হয়।
রাসায়নিক বিক্রিয়াকে রাসায়নিক সমীকরণ আকারে লেখার জন্য কতোগুলো নিয়ম মানা হয় সেগুলো হচ্ছে:
1. গণিতে যেমন সমীকরণের মাঝে একটি সমান চিহ্ন (=) ব্যবহার করা হয় তেমনি কোনো বিক্রিয়ার বিক্রিয়ক বাম পাশে এবং উৎপাদ ডান পাশে লিখে তাদের মাঝে একটি সমান চিহ্ন (=) বা তীর চিহ্ন (→) বসাতে হয়।
2. বিক্রিয়কসমূহ এবং উৎপাদসমূহকে রাসায়নিক প্রতীক বা সংকেতের মাধমে লেখা হয়। বিক্রিয়ায় একাধিক বিক্রিয়ক থাকলে বিক্রিয়কসমূহের মাঝে যোগ চিহ্ন দিতে হয়। এবং একাধিক উৎপাদ থাকলে উৎপাদসমূহের মাঝে যোগ চিহ্ন দিতে হয়।
3. যে প্রক্রিয়ায় সমীকরণের বাম পাশের বিভিন্ন মৌলের পরমাণুর সংখ্যা এবং ডান পাশের ঐ একই মৌলের পরস্পর সংখ্যা সমান করা হয়। সেই প্রক্রিয়াকে রাসায়নিক সমীকরণের সমতা বলা হয়।
2H2 + O2→ 2H2O
2H2 + O2 = 2H2O
4. কখনো কখনো বিক্রিয়ার সমতা না করেও বিক্রিয়া দেখানো হয়, তখন সমান চিহ্ন (=) না দিয়ে তীর চিহ্ন (→) ব্যবহার করতে হয়।
H2 + O2 → H2O
5. অনেক সময় বিক্রিয়ক এবং উৎপাদের ভৌত অবস্থা উল্লেখ করেও রাসায়নিক সমীকরণ লেখা হয়। বিক্রিয়ক এবং উৎপাদের ভৌত অবস্থা পদার্থের ডান পাশে প্রথম বন্ধনীর মধ্যে প্রকাশ করা হয় । এক্ষেত্রে কোনো পদার্থ কঠিন হলে তার ইংরেজি নাম (Solid) এর প্রথম বর্ণ (s) লিখতে হয়, কোনো পদার্থ তরল (liquid) হলে তার ইংরেজি নামের প্রথম বর্ণ লিখতে হয়, কোনো পদার্থ গ্যাসীয় তার ইংরেজি নাম (gas) এর প্রথম বর্ণ (g) লিখতে হয়। কোনো পদার্থ পানিতে দ্রবীভূত হলে সেই দ্রবণকে বলা হয় জলীয় দ্রবণ। জলীয় দ্রবণের ইংরেজি নাম (aquas solution ) এর প্রথম 2টি বর্ণ (aq) লিখতে হয়। উপরের বিক্রিয়ায় হাইড্রোজেন ও অক্সিজেন গ্যাস এবং উৎপন্ন পদার্থ পানি তরল তাই তাকে লিখতে হবে।
2H2(g) + O2(g) → 2H2O(1)
রাসায়নিক সমীকরণ এর উদ্দেশ্য হচ্ছে কোন কোন পদার্থ বিক্রিয়া করে কোন কোন পদার্থ হয়েছে সেটি দেখানো। অনেক সময় সমতা না করেও সেটি দেখানো যেতে পারে।
6. তবে যদি কোনো বিক্রিয়ায় কতটুকু তাপ উৎপন্ন হয় বা কতটুকু তাপ শোষিত হয় তা সমীকরণে দেখাতে হয় তবে সেক্ষেত্রে রাসায়নিক বিক্রিয়ার সমতা করতে হবে এবং বিক্রিয়ক এবং উৎপাদের ভৌত অবস্থা (যেমন কঠিন, তরল, গ্যাসীয় অবস্থা, জলীয় অবস্থা ইত্যাদি) লিখতে হবে।
একই পদার্থের অসংখ্য অণু বা একাধিক পদার্থের অসংখ্য অণু পরস্পরের সাথে যুক্ত হয়ে বৃহৎ অণু গঠন করার প্রক্রিয়াকে পলিমারকরণ বলে। এই বিক্রিয়ায় উৎপন্ন বৃহৎ অণুকে পলিমার এবং বিক্রিয়ক অসংখ্য ক্ষুদ্র অণুর প্রত্যেকটিকে মনোমার বলে। একই বিক্রিয়কের অসংখ্য অণু যুক্ত হয়ে পলিমার গঠন করার প্রক্রিয়াকে যুত পলিমারকরণ (Addition Polymerisation) বলে।
যুত পলিমারকরণ বিক্রিয়া-
যে পলিমারকরণ বিক্রিয়ায় মনোমার অণুসমূহ পরস্পরের সাথে যুক্ত হওয়ার সময় ক্ষুদ্র ক্ষুদ্র অণু যেমন- ইত্যাদি অপসারণ করে সেই পলিমারকরণ বিক্রিয়াকে ঘনীভবন পলিমারকরণ বলে।
# বহুনির্বাচনী প্রশ্ন
পলিইথিলিন
ব্যাকেলাইট
পলিভিভিনাইল অ্যাসিটেট
পলিভিনাইল ক্লোরোইড
জারণ ও বিজারণ (Oxidation & Reduction)
জারণ (Oxidation)
যে বিক্রিয়ায় কোনো মৌল বা যৌগে তড়িৎ ঋণাত্মাক পরমাণু বা মূলক সংযুক্ত হয় বা তাদের অনুপাত বৃদ্ধি পায় অথবা কোনো তড়িৎ ধনাত্মক পরমাণু বা মূলকের অপসারণ হয় বা তাদের অনুপাত হ্রাস পায়, সেই বিক্রিয়াকে জারণ বলে।
ইলেকট্রনীয় ধারণা: যে বিক্রিয়ায় কোনো রাসায়নিক সত্তা (অণু, পরমাণু, মূলক বা আয়ন) ইলেকট্রন প্রদান করে, তাকে জারণ বলে।
যেমন: Na → Na+ + e- (ইলেকট্রন দান বা জারণ)
বিজারণ (Reduction)
যে বিক্রিয়ার কোনো মৌল বা যৌগে তড়িৎ ধনাত্মক পরমাণু বা মূলক সংযুক্ত হয় বা তাদের অনুপাত বৃদ্ধি পায় অথবা কোনো তড়িৎ ঋণাত্মক পরমাণু বা মূলকের অপসারণ হয় বা তাদের অনুপাত হ্রাস পায়, সেই বিক্রিয়াকে বিজারণ বলে।
ইলেকট্রনীয় ধারণা: যে বিক্রিয়ায় কোন রাসায়নিক সত্তা (অণু, পরমাণু, মূলক বা আয়ন) ইলেকট্রন গ্রহণ করে, তাকে বিজারণ বলে।
যেমন: Cl + e- → Cl- (ইলেকট্রন গ্রহণ বা বিজারণ)
যে বস্তু অন্য কোনো বস্তুর বিজারণ ঘটায় এবং নিজে জারিত হয়, তাকে বিজারক বলে। যেমন: সকল ধাতু, হাইড্রোজেন, কার্বন প্রভৃতি। বিজারক পদার্থ ইলেকট্রন বর্জন করে।
যে বস্তু অন্য কোনো বস্তুর জারণ ঘটায় 'এবং নিজে বিজারিত হয়, তাকে জারক বলা হয়। যেমন: অক্সিজেন, ফ্লোরিন, ক্লোরিন, ব্রোমিন, আয়েডিন, পটাসিয়াম ডাইক্রোমেট, পটাসিয়াম পারম্যাঙ্গানেট, HNO3, উত্তপ্ত গাঢ় H2SO4, পার অক্সাইডসমূহ, পার অক্সি এসিডসমূহ এবং তাদের লবণসমূহ।। জারক পদার্থসমূহ ইলেকট্রন গ্রহণ করে।
# বহুনির্বাচনী প্রশ্ন
# বহুনির্বাচনী প্রশ্ন
যেসব যৌগ জলীয় দ্রবণে আংশিক বা সম্পূর্ণরূপে বিয়োজিত হয়ে হাইড্রোজেন আয়ন (H+) উৎপন্ন করে তাকে এসিড বলে।
উদাহরণ- সালফিউরিক এসিড, সাইট্রিক এসিড, কার্বলিক এসিড।
যে সকল ক্ষারক পানিতে দ্রবীভূত হয় তাকে ক্ষার বলে।
যেমনঃ ক্যালসিয়াম হাইড্রোক্সাইড [Ca(OH)2], সোডিয়াম হাইড্রোক্সাইড [NaOH]
এসিড ও ক্ষারকের বিক্রিয়ায় যে নিরপেক্ষ পদার্থ উৎপন্ন হয় তাকে লবন বলে।
উদাহরণ- সোডিয়াম ক্লোরাইড [NaCl], ক্যালসিয়াম ক্লোরাইড [CaCl2]
এসিড (Acid)
যদি কোনো যৌগের অণুতে এক বা একাধিক প্রতিস্থাপনীয় হাইড্রোজেন পরমাণু থাকে এবং ঐ প্রতিস্থাপনীয় হাইড্রোজেন পরমাণু কোনো ধাতু বা ধাতুর ন্যায় ক্রিয়াশীল কোনো যৌগমূলক দ্বারা আংশিক বা সম্পূর্ণরূপে প্রতিস্থাপিত করা যায় এবং যা ক্ষারকের সাথে বিক্রিয়া করে লবণ ও পানি উৎপন্ন করে, তাকে অম্ল (Acid) বলে। অন্যভাবে বলা যায়, যে যৌগ বা আয়ন অন্য পদার্থকে প্রোটন দান করতে পারে, তাকে অম্ল (Acid) বলে। এসিডের স্বাদ টক। উদাহরণ: সালফিউরিক এসিড (H2SO4), নাইট্রিক এসিড (HNO3) ইত্যাদি।
# বহুনির্বাচনী প্রশ্ন
ফরমিক এসিড
অক্সালিক এসিড
নাইট্রিক এসিড
এসিটিক এসিড
ক্ষারক ও ক্ষার (Base & Alkali)
ধাতুর অক্সাইড ও হাইড্রোক্সাইডকে ক্ষারক বলে। অন্যভাবে বলা যায়, যে যৌগ বা আয়ন অম্ল হতে প্রোটন গ্রহণ করতে পারে, তাই ক্ষারক। উদাহরণ: সোডিয়াম হাইড্রোক্সাইড (NaOH), ম্যাগনেশিয়াম হাইড্রোক্সাইড (MgOH)। অধিকাংশ ক্ষারকই পানিতে দ্রবীভূত হয় না। যে সকল ক্ষারক পানিতে দ্রবীভূত হয়, তাকে ক্ষার বলে। উদাহরণ: সোডিয়াম হাইড্রোক্সাইড (NaOH). পটাসিয়াম হাইড্রোক্সাইড (KOH) ইত্যাদি।
| PH | দ্রবণ |
| =7 | নিরপেক্ষ |
| <7 | অম্লীয় |
| >7 | ক্ষারীয় |
PH
কোনো দ্রবণের হাইড্রোজেন আয়নের (H+) মোলার ঘনমাত্রার ঋণাত্মক লগারিদমকে ঐ দ্রবণের PH বলে অর্থ্যাৎ PH = -log[H+] । PH হলো এসিডীয় মাত্রা, ক্ষারকীয় মাত্রা এবং নিরপেক্ষতা নিদের্শক। PH স্কেলের রেঞ্জ ০-১৪।
বিভিন্ন পদার্থের PH এর মান
পদার্থ | PH এর মান | পদার্থ | PH এর মান |
| বিশুদ্ধ পানি | ৭ | চোখের পানি | ৪.৮০~৭.৫০ |
| মানুষের রক্ত | ৭.৩৫- ৭.৪৫ | মূত্র | ৪.৮০~৭.৫০ |
বাফার
যে দ্রবণ নিজস্ব PH স্থির রাখার ক্ষমতা রাখে, তাকে বাফার দ্রবণ বলে। হেন্ডারসন সমীকরণের দ্বারা বাফারের PH এর মান গণনা করা হয়।
নির্দেশক
যে সব যৌগ নিজেদের বর্ণ পরিবর্তনের কোন দ্রবণ অম্লীয় বা ক্ষারীয় তা নির্দেশ করে, তাদের নির্দেশক বলে।
| নির্দেশক | অম্লীয় মাধ্যমে বর্ণ | ক্ষারীয় মাধ্যমে বর্ণ |
| লিটমাস | লাল | নীল |
| ব্রোমোফেনল | হলুদ | নীল |
| মিথাইল অরেঞ্জ | লাল | হলুদ |
# বহুনির্বাচনী প্রশ্ন
লবণ (Salt)
"লবণ" শব্দটি সাধারণত রসায়নে একটি আয়নিক যৌগ বা খাদ্য লবণ (যেমন সোডিয়াম ক্লোরাইড) কে বোঝায়। রসায়নে, লবণ হল অ্যাসিড এবং ক্ষারকের মধ্যে বিক্রিয়ার ফলে উৎপন্ন একটি পদার্থ। খাদ্য লবণ, যা টেবিল লবণ নামেও পরিচিত, এটি সোডিয়াম ক্লোরাইড (NaCl)। এটি খাবারকে লবণাক্ত করতে এবং খাদ্য সংরক্ষণে ব্যবহৃত হয়।
# বহুনির্বাচনী প্রশ্ন
পানির খরতা
যে পানি সাবানের সাথে সহজে ফেনা উৎপন্ন করে না, অনেক সাবান খরচ করার পর ফেনা উৎপন্ন করে, তাকে খর পানি বলে। খর পানিতে সাবান ফেনা না দিলেও ডিটারজেন্ট উত্তম ফেনা দেয়। পানির খরতা দুই প্রকার। যথা: অস্থায়ী খরতা এবং স্থায়ী খরতা।
খরতা | কারণ |
| অস্থায়ী | ক্যালসিয়াম বা ম্যাগনেসিয়ামের বাইকার্বনেট (HCO3-) লবণ |
| স্থায়ী | ক্যালসিয়াম বা ম্যাগনেসিয়ামের সালফেট (SO4-) বা ক্লোরাইড (Cl-) লবণ |
দূরীকরণ পদ্ধতি | বৈশিষ্ট্য |
| ফুটানো | শুধু অস্থায়ী খরতা দূর করা যায়। |
| পারমুটিট পদ্ধতি | স্থায়ী ও অস্থায়ী খরতা দূর করা যায়। |
| সোডা পদ্ধতি | স্থায়ী ও অস্থায়ী উভয় প্রকার খরতা কাপড় কাচা সোডা (Na2 CO3) এর সাহায্যে দূর করা যায়। |
খর পানি ব্যবহার করলে কারখানার বয়লারে, মোটর গাড়ির শীতক প্রকোষ্ঠে ও কেতলীর তলায় অদ্রবণীয় ও তাপ অপরিবাহী ক্যালসিয়াম কার্বনেট, ক্যালসিয়াম সালফেট প্রভৃতি লবণের আবরণ পড়ে। বয়লারের গায়ে অদ্রবণীয় লবণের স্তর পড়ার কারণে বয়লারের তাপ পরিবাহিতা কমে যায়। ফলে জ্বালানি অপচয় ঘটে।
মৃদু পানি (Soft Water)
যে পানি সাবানের সাথে সহজে ফেনা উৎপন্ন করে, তাকে মৃদু পানি বলে। প্রাকৃতিক উৎসগুলোর মধ্যে বৃষ্টি থেকে সবচেয়ে বেশি মৃদু পানি পাওয়া যায়।
# বহুনির্বাচনী প্রশ্ন
# বহুনির্বাচনী প্রশ্ন
তড়িৎ কোষ (Electric Cell)
যে যন্ত্রের সাহায্যে রাসায়নিক শক্তি থেকে নিরবিচ্ছিন্নভাবে তড়িৎ শক্তি পাওয়া যায় তাকে তড়িৎ কোষ বলে। তড়িৎ কোষ দুই প্রকার। যথা:
(ক) তড়িৎ রাসায়নিক কোষ বা গ্যালভানিক সেল: যে কোষে রাসায়নিক বিক্রিয়া হতে বিদ্যুৎ উৎপন্ন হয়, তাকে তড়িৎ রাসায়নিক কোষ বলে। তড়িৎ রাসায়নিক কোষ আলেকসান্দ্রো ভোল্টা আবিষ্কার করেন।
(খ) তড়িৎ বিশ্লেষ্য কোষ: যে পাত্রে তড়িৎ বিশ্লেষণ চালানো হয়, তাকে তড়িৎ বিশ্লেষ্য কোষ বলা হয়। তড়িৎ বিশ্লেষ্য কোষে ধনাত্মক তড়িৎদ্বারকে অ্যানোড এবং ঋণাত্মক তড়িৎদ্বারকে কে ক্যাথোড বলে।
শুষ্ক কোষ (Dry Cell)
শুষ্ক কোষ একটি প্রাথমিক কোষ বা প্রাইমারি সেল। সাধারণ ড্রাইসেলে ইলেকট্রোড হিসাবে কার্বন দণ্ড (+) এবং দস্তার কৌটা (-) ব্যবহৃত হয়। শুষ্ক কোষে কার্বন দণ্ড ইলেকট্রন দান করে। কার্বন দণ্ডের চারপার্শ্বে কঠিন ম্যাঙ্গানিজ ডাই-অক্সাইড (MnO2) এবং কার্বন গুড়ার মিশ্রণ থাকে। এর চারপার্শ্বে অ্যামোনিয়াম ক্লোরাইডের (NH4CI) এর পেস্ট থাকে। NH4CI বিদ্যুৎ উত্তেজক হিসাবে এবং MnO2 ছদন নিবারক হিসাবে কাজ করে। বাজারে এটি ব্যাটারি নামে পরিচিত। ব্যাটারি থেকে আমরা D.C বিদ্যুৎ পাই। শুষ্ক কোষ একমুখী (DC) তড়িৎ প্রবাহ উৎপন্ন করে। এর তড়িচ্চালক বল ১.৫ ভোল্ট।
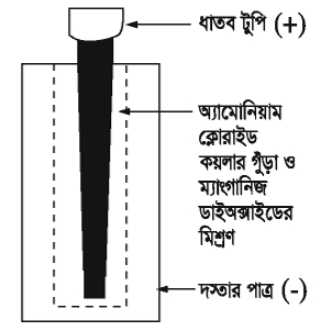
স্টোরেজ ব্যাটারি (Storage Battery)
গাড়িতে ব্যবহৃত এ সকল ব্যাটারিতে সীসার ইলেকট্রোডের সঙ্গে তড়িৎ বিশ্লেষ্য রূপে সালফিউরিক এসিড (H2SO4) ব্যবহৃত হয়।
# বহুনির্বাচনী প্রশ্ন
জৈব রসায়ন (Organic Chemistry)
কার্বন শিকল দ্বারা গঠিত বিভিন্ন যৌগের রসায়নকে জৈব রসায়ন বলে। অন্যভাবে বলা যায় যে, রসায়নের যে শাখায় হাইড্রোকার্বন ও হাইড্রোকার্বনের বিভিন্ন জাতক সম্বন্ধে আলোচনা করা হয়, তাকে জৈব রসায়ন বলে।
# বহুনির্বাচনী প্রশ্ন
জৈব যৌগ (Organic Compounds)
হাইড্রোজেন ও কার্বন দ্বারা গঠিত দ্বিমৌল যৌগসমূহকে হাইড্রোকার্বন বলে। জৈব যৌগ বলতে হাইড্রোকার্বন এবং হাইড্রোকার্বন থেকে উদ্ভুত যৌগসমূহকে বুঝায়। যেমন: মিথেন (CH4), ইথেন (C2H6), প্রোপেন (C3H8) প্রভৃতি। ফ্রেডারিক উহলারকে জৈব রসায়নের জনক বলা হয়। জৈব যৌগে কার্বন মৌলটি অবশ্যই থাকবে। বাজারে সিলিন্ডারে যে গ্যাস বিক্রি করা হয় তা মূলত বিউটেন। জৈব বস্তুর সম্পূর্ণ দহনে কার্বন ডাই-অক্সাইড এবং অসম্পূর্ণ দহনে কার্বন মনোক্সাইড উৎপন্ন হয়।
# বহুনির্বাচনী প্রশ্ন
অ্যালিফেটিক যৌগসমূহকে তিনটি শ্রেণীতে ভাগ করা যায় যথা-
ক) অ্যালকেন: হাইড্রোজেন ও কার্বন পরমাণু দ্বারা গঠিত একক বন্ধনে আবদ্ধ যৌগসমূহকে অ্যালকেন বলে। অ্যালকেনের সাধারণ সংকেত CnH2n+2। যেমন- মিথেন (CH4), ইথেন (CH3-CH3), প্রোপেন (CH3-CH2- CH3) ইত্যাদি।
খ) অ্যালকিন: হাইড্রোজেন ও কার্বন পরমাণু দ্বারা গঠিত দ্বি বন্ধনে আবদ্ধ যৌগসমূহকে অ্যালকিন বলে। অ্যালকেনসমূহের সাধারণ সংকেত CnH2n। যেমন- ইথিন (CH2=CH2), প্রোপিন (CH2= CH- CH2) ইত্যাদি।
গ) অ্যালকাইন: হাইড্রোজেন ও কার্বন পরমাণু দ্বারা গঠিত ত্রি বন্ধনে আবদ্ধ যৌগসমূহকে অ্যালকাইন বলে। অ্যালকাইনসমূহের সাধারণ সংকেত CnH2n+2। যেমন- ইথাইন (CH = CH), প্রোপাইন (CH = C-CH3) ইত্যাদি।
# বহুনির্বাচনী প্রশ্ন
বিভিন্ন খাদ্যে উপস্থিত জৈব এসিড।
বিভিন্ন প্রাকৃতিক খাদ্য ও ফলে বিভিন্ন ধরনের জৈব এসিড (Organic Acid) পাওয়া যায়, যা খাদ্যের স্বাদ, গন্ধ ও সংরক্ষণে ভূমিকা রাখে। প্রধান জৈব এসিডগুলোর মধ্যে লেবুতে সাইট্রিক এসিড, আপেলে ম্যালিক এসিড, তেঁতুলে টারটারিক এসিড, এবং দুধে ল্যাকটিক এসিড) অন্যতম।
# বহুনির্বাচনী প্রশ্ন
যে সব চাক্রিক বা হেটারোচাক্রিক যৌগে (4n + 2) সংখ্যক সঞ্চারণশীল পাই ইলেকট্রন বিদ্যমান, তাদেরকে অ্যারোমেটিক যৌগ বলে। 4n + 2 সূত্রে n = 1, 2, 3 হলে সঞ্চারণশীল পাই
ইলেকট্রন দাঁড়ায় যথাক্রমে 6, 10, 14। বেনজিন, ফেনল ও টলুইনে 6টি করে সঞ্চারণশীল পাই ইলেকট্রন বিদ্যমান। ন্যাপথালিন যৌগে 10টি পাই ইলেকট্রন বিদ্যমান। তাই এরা সবাই অ্যারোমেটিক যৌগ।
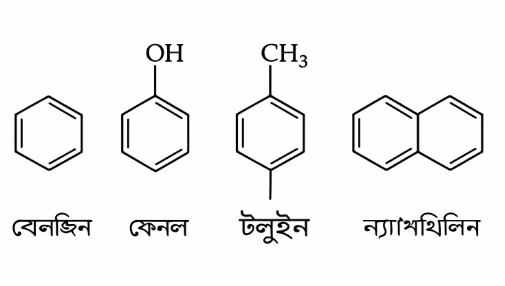
অধিকাংশ অ্যারোমেটিক যৌগই সুগন্ধযুক্ত ও এদের বেনজিন বলয় প্রতিস্থাপন বিক্রিয়া দেয়।
# বহুনির্বাচনী প্রশ্ন
প্রাত্যহিক জীবনে রসায়ন
আমাদের দৈনন্দিন জীবনের সকল ক্ষেত্রে রসায়ন এর ব্যাপক প্রভাব রয়েছে | আমরা প্রতিদিন যে খাবার খাই তাতে রসায়ন রয়েছে, যে বাতাসে আমরা নিশ্বাস নিই তাতে রসায়ন রয়েছে, আমাদের সাবান, আমাদের আবেগ এক কথায় যে সমস্ত বস্তু আমরা দেখতে ও স্পর্শ করতে পারি সকল কিছুতেই রসায়ন বিদ্যমান। আজ আমি আমাদের প্রাত্যহিক জীবনে কিসু মজার রসায়ন নিয়ে আলোচনা করব।
মানব দেহের উপাদান: মানব দেহের বেশির ভাগ হচ্ছে পানি । যেসমস্ত উপাদান দ্বারা তৈরী সেগুলো নিম্নরূপ:
১. অক্সিজেন (৬৫% )
২. কার্বন (১৮%)
৩. হাইধ্রজেন (১০%)
৪. নাইট্রজেন (৩%)
৫. কালসিয়াম (১.৫%)
৬. ফসফরাস (১.০%)
৭. পটাসিয়াম (০.৩৫%)
৮. সালফার (০.2৫%)
৯. সোডিয়াম (০.১৫%)
১০. ম্যাগনেসিয়াম (০.০৫%)
১১. কপার, জিঙ্ক, সেলেনিয়াম, মলিবডেনাম, ফ্লুরিন, ক্লোরিন, আয়োডিন, মান্গানিজ, কোবাল্ট, এবং আইরন (০.৭০%)
১২. লিথিয়াম, সট্রনিয়াম, এলুমিনিয়াম, সিলিকন, লীড ভানাদিয়াম, আর্সেনিক, ব্রোমিন ইত্যাদি ।
নির্মাণ সামগ্রী
নির্মাণ সামগ্রী হিসেবে ইট এবং সিমেন্ট খুবই গুরুত্বপূর্ণ। বালি ও পানির সাথে সিমেন্ট মিশিয়ে ‘মর্টার’ এবং ইট বা পাথরের টুকরা, সিমেন্ট, বালি ও পানি মিশিয়ে কংক্রিট তৈরি করা হয়।
সিমেন্ট
নির্মাণ কাজের অপরিহার্য উপাদান সিমেন্ট। সিমেন্টের প্রধান উপাদান চুন (৬২%), সিলিকা (২২%), অ্যালুমিনা, লৌহ প্রভৃতি। সিমেন্ট দুই ধরনের। যথা- পোর্টল্যান্ড সিমেন্ট এবং অ্যালুমিনাস সিমেন্ট। সিমেন্টে দ্রুত জমাট বাঁধা রোধ করার জন্য জিপসাম যোগ করা হয়।
পোর্টল্যান্ড সিমেন্ট আমাদের দেশে সবচেয়ে বেশি ব্যবহৃত হয়। চুনাপাথর (Limestone) এর সাথে। সামান্য কাদা বা এ্যালুমিনো সিলিকেট (Al2SiO5) মিশিয়ে বিশেষায়িত চুল্লীর মাধ্যমে ক্লিঙ্কার তৈরি করা হয়। ক্লিঙ্কার চূর্ণ (>= ৯৭%) করে তার সাথে সামান্য জিপসাম (=<৩%) মিশিয়ে আধুনিক পোর্টল্যান্ড সিমেন্ট তৈরি করা হয়।
ইট (Brick): তৈরির পদ্ধতি অনুসারে ইটকে তিনভাগে ভাগ করা যায়। বাংলা ইট, সিরামিক ইট এবং কংক্রিটের তৈরি ইট। সাধারণ ইটকে বাংলা ইট বলে। মেশিনে বানানো ইটকে সিরামিক ইট বলে। সিরামিক ইটে সিলিকা (৫৫%), অ্যালুমিনা (৩০%), লৌহ অক্সাইড (৮%), ম্যাগনেসিয়া (৫%), জৈব পদার্থ (১%) থাকতে পারে।
কাঁচ (Glass): কাঁচ রাসায়নিকভাবে অত্যন্ত নিষ্ক্রিয়। কাঁচ বহুদিন রোদে বা পানিতে থাকলে নষ্ট, ক্ষয় বা বৃদ্ধি হয় না। কাচ তৈরির প্রধান কাঁচামাল হলো বালি। বালির প্রধান উপাদান হলো সিলিকা। সিলিকার রাসায়নিক নাম সিলিকন ডাই অক্সাইড (SiO2)। সিলিকার বিশুদ্ধ রূপ কোয়ার্টজ।
# বহুনির্বাচনী প্রশ্ন
সারিন (Sarin): সারিন (C4H10FO2P) অত্যন্ত বিষাক্ত এক ধরনের বর্ণ ও গন্ধহীন তরল পদার্থ যা রাসায়নিক অস্ত্র হিসেবে ব্যবহৃত হয়। এটি স্নায়ুতন্ত্রকে আক্রমণ করে অকার্যকর করে দেয়।
নাইট্রোগ্লিসারিন (Nitroglycerin): নাইট্রোগ্লিসারিন বিস্ফোরক পদার্থটি সালফিউরিক এসিড ও নাইট্রিক এসিডের সংমিশ্রণে প্রস্তুত করা হয়। পাহাড় ভাঙ্গা, টানেল তৈরি ও খনিজ শিল্পে ব্যবহৃত বিস্ফোরক পদার্থ ডিনামাইট প্রস্তুতিতে নাইট্রোগ্লিসারিন ব্যবহৃত হয়।
টি.এন.টি (TNT): 2, 4, 6 ট্রাই নাইট্রো টলুইনকে সংক্ষেপে টি.এন.টি বলে। এটি প্রধানত বিস্ফোরক পদার্থ হিসেবে বিভিন্ন ধরনের বোমায় ব্যবহৃত হয়।
পিকরিক এসিড (Picric Acid): পিকরিক এসিডে রাসায়নিক নাম ২,৪,৬ এটাইনাইট্রোফেনল। এটি বিস্ফোরক যৌগ প্রস্তুতিতে ব্যবহৃত হয়। এছাড়া পোড়া ক্ষতের জ্বালা ও পচন নিবারণে
# বহুনির্বাচনী প্রশ্ন
ডিডিটি (DDT): ডিডিটি এর রাসায়নিক নাম প্যারা প্যারা ডাইক্লোরো ডাই ফিনাইল ট্রাই ক্লোরো ইথেন। শক্তিশালী জীবাণুনাশক ও কীটনাশক হিসেবে ডি.ডি.টি প্রচুর ব্যবহৃত হয়।
গ্যামেক্সিন বা লিনডেন: গ্যামেক্সিন পাউডার বা লিনডেন এর রাসায়নিক নাম বেনজিন হেক্সাক্লোরাইড (C6H6Cl6)। এটি শক্তিশালী জীবাণুনাশক ও কীটনাশক হিসেবে ব্যবহৃত হয়।
# বহুনির্বাচনী প্রশ্ন
# বহুনির্বাচনী প্রশ্ন
# বহুনির্বাচনী প্রশ্ন
Read more







