মৌলের ইলেকট্রন বিন্যাসে সর্বশেষ কক্ষপথের ইলেকট্রনসমূহকে যোজ্যতা ইলেকট্রন বলে।
যোজ্যতা ইলেকট্রন সর্বশেষ কক্ষপথের ইলেকট্রন সংখ্যা দ্বারা হিসাব করা হয় ।
পটাসিয়ামের যোজ্যতা ইলেকট্রন 1 টি ।
অক্সিজেনের সর্বশেষ কক্ষপথে ৩টি ইলেকট্রন থাকে ।
অক্সিজেনের যোজ্যতা ইলেকট্রন সংখ্যা 6 ।
নাইট্রোজেনের L কক্ষপথের ইলেকট্রন সংখ্যা 5 টি।
নাইট্রোজেনের যোজ্যতা ইলেকট্রন সংখ্যা 5 ।
কোনো মৌলের একটি পরমাণুর সাথে অপর মৌলের পরমাণুর যুক্ত হওয়ার ক্ষমতাকে যোজনী বা যোজ্যতা বলে ।
হাইড্রোজেনের যোজনী 1 ।
H2O অণুতে অক্সিজেনের যোজনী 2 ।
NaCl অণুতে সোডিয়ামের যোজনী 1 ।
CaO যৌগে ক্যালসিয়ামের যোজনী 2 ।
কোনো মৌলের একাধিক যোজনী থাকলে সেই মৌলের যোজনীকে পরিবর্তনশীল যোজনী বলে ।
আয়রন এর পরিবর্তনশীল যোজনী 2 এবং 3 ।
কোনো মৌলের সর্বোচ্চ যোজনী এবং সক্রিয় যোজনীর পার্থক্যকে সুপ্ত যোজনী বলে।
FeCl2 যৌগে Fe এর সুপ্ত যোজনী 1 ।
FeCl3 যৌগে Fe এর সুপ্ত যোজনী 0 ।
PCI5 যৌগে ফসফরাসের যোজনী 3 ।
PCI3 যৌগে ফসফরাসের সুপ্ত যোজনী 2 ।
PbCl2 যৌগে লেডের সুপ্ত যোজনী 2 ।
N2O5 যৌগে নাইট্রোজেনের সক্রিয় যোজনী 5 ।
SO3 অণুতে সালফারের যোজনী 6 ।
SO2 অণুতে সালফারের সুপ্ত যোজনী 2 ।
SO2 অণুতে সালফারের সক্রিয় যোজনী 4 ।
যৌগমূলকে কমপক্ষে ২টি মৌল থাকে ।
আধানযুক্ত পরমাণুগুচ্ছ যা মৌলের আয়নের ন্যায় আচরণ করে তাকে যৌগমূলক বলে।
অ্যামোনিয়াম ধনাত্মক যৌগমূলক ।
অ্যামোনিয়াম মূলকের সংকেত NH4 ।
অ্যামোনিয়ামের যোজনী 1 ।
হাইড্রোক্সাইড যৌগমূলকের আধান -1 ।
ফসফোনিয়াম মূলকের সংকেত PH4
ফসফেট যৌগমূলকের যোজনী 3 ।
নাইট্রেট মূলকের সংকেত ।
হাইড্রোজেন কার্বনেট মূলকের সংকেত
সালফেট এর যোজনী 2 ।
সালফাইট মূলকের সংকেত ।
হাইড্রোজেন সালফেট মূলকের সংকেত
যৌগমূলকের আধান ধনাত্মক কিংবা ঋণাত্মক ।
ফসফেটের আধান -3
ফসফোনিয়ামের আধান +1 ।
অক্সিজেন অণুতে 2টি পরমাণু আছে।
ওজোনের একটি অণুতে 3 টি অক্সিজেন পরমাণু থাকে ।
কোনো মৌলের অণুতে বিদ্যমান পরমাণুর সংখ্যা মৌলের প্রতীকের ডানপাশে নিচে লিখা হয় ।
অণু গঠন করে না বলে শুধু প্রতীক দিয়ে বোঝানো হয় সকল ধাতু ও নিষ্ক্রিয় মৌল।
O3 অণুটির রাসায়নিক নাম ওজোন।
N. O. Ar. CI মৌলগুলোর মধ্যে Ar (আর্গন) অণু গঠন করে না ।
অ্যালুমিনিয়াম অক্সাইডের সংকেত AI2O3
ম্যাগনেসিয়াম ফসফেটের সংকেত Mg3(PO4)2
CO2 অণুতে কার্বনের যোজনী 4 ।
FeSO4 যৌগে আয়রনের যোজনী 2 ।
বোরন নাইট্রাইডের সংকেত BN ।
বোরন নাইট্রাইড যৌগে নাইট্রোজেনের যোজনী 3 ।
অ্যামোনিয়াম ফসফেটের সংকেত (NH4)3PO4
মৌলের পরমাণুর প্রতীক ও পরমাণুর সংখ্যা দিয়ে আণবিক সংকেত প্রকাশ করা হয়।
একটি অণুতে মৌলের পরমাণুগুলো যেভাবে সাজানো থাকে প্রতীক এবং বন্ধনের মাধ্যমে প্রকাশ করাকে গাঠনিক সংকেত বলে ।
প্রোপেনের আণবিক সংকেত C3HS
মিথেনের আকৃতি চতুস্তলকীয় ।
মিথেন অণুতে কার্বনের যোজনী কত 4 ।
মিথেন অণুতে কার্বন ও হাইড্রোজেনের মধ্যে একক বন্ধন বিদ্যমান।
যৌগের অণুতে কোনো পরমাণুর সংখ্যা এবং বন্ধনের প্রকৃতি গাঠনিক সংকেতের মাধ্যমে জানা যায় ।
He এর ইলেকট্রন বিন্যাস দুই এর নিয়ম মেনে চলে ।
নিষ্ক্রিয় মৌলগুলোর মধ্যে হিলিয়াম (He) ইলেকট্রন বিন্যাস অষ্টক নিয়মের ব্যতিক্রম ।
Li+ এ ইলেকট্রন সংখ্যা 2 ।
ধাতু ধরনের মৌল ইলেকট্রন ত্যাগ করে অষ্টক পূরণ করতে পারে ।
BeCl2 অণুর কেন্দ্রীয় পরমাণু Be এর সর্বশেষ শক্তিস্তরে ইলেকট্রন সংখ্যা 2 জোড়া।
BF3 অণুর কেন্দ্রীয় পরমাণু B (বোরন)
BF3 অণুর কেন্দ্রীয় পরমাণুর সর্বশেষ শক্তিস্তরে কয়টি ইলেকট্রন বিদ্যমান ।
CH4 অণুর কেন্দ্রীয় পরমাণুর সর্বশেষ শক্তিস্তরে 4 জোড়া/৪ টি ইলেকট্রন বিদ্যমান ।
মৌলসমূহের অষ্টক কাঠামো অর্জনের কারণ স্থিতিশীলতা অর্জন ।
পটাসিয়াম ইলেকট্রন ত্যাগ করে নিকটস্থ নিষ্ক্রিয় গ্যাসের 2.8.8 ইলেকট্রন বিন্যাস লাভ করে।
LiH যৌগে লিথিয়াম ও হাইড্রোজেন পরমাণু দ্বৈত কাঠামো অর্জন করে।
দুই এবং অষ্টক নিয়মের মধ্যে দুই অধিকতর উপযোগী এবং আধুনিক ।
অষ্টক নিয়ম - পরমাণুর যোজ্যতা স্তরে ৪টি e- থাকা ।
অণুতে যেকোনো পরমাণুর সর্বশেষ শক্তিস্তরে এক বা একাধিক জোড়া ইলেকট্রন অবস্থানের নিয়মকে দুই' এর নিয়ম বলে ।
CH4 অণুতে কার্বন ও হাইড্রোজেন ইলেকট্রন শেয়ার প্রক্রিয়ায় সর্বশেষ শক্তিস্তরে অষ্টক কাঠামো অর্জন করে ।
পর্যায় সারণির 1-20 পরমাণবিক সংখ্যার মৌলসমূহ অষ্টক ও দুই এর নিয়ম ভালোভাবে অনুসরণ করে।
Is2 হিলিয়াম মৌলের ইলেকট্রন বিন্যাস।
নিষ্ক্রিয় গ্যাসের একটি অণুতে । টি পরমাণু থাকে ।
ক্রিপ্টনের ৩য় শক্তিস্তরে ইলেকট্রন সংখ্যা 8 টি ।
জেননের ৪র্থ শক্তিস্তরে ইলেকট্রন সংখ্যা 18 টি।
রেডনের ইলেকট্রনসমূহ 6 টি শক্তিস্তরে বিন্যস্ত ।
আর্গনের ৩য় শক্তিস্তরে ইলেকট্রন সংখ্যা 8 ।
হিলিয়ামের সর্বশেষ শক্তিস্তর পূর্ণ করতে প্রয়োজনীয় ইলেকট্রন সংখ্যা 2 টি ।
নিষ্ক্রিয় গ্যাসসমূহের যোজনী শূন্য (0)।
2,8. 18.8 ইলেকট্রন বিন্যাসটি ক্রিপ্টন (Kr) মৌলের ।
পর্যায় সারণির গ্রুপ- 18 গ্রুপের মৌলগুলো তড়িৎ নিরপেক্ষ ।
নিষ্ক্রিয় গ্যাসের সর্বশেষ শক্তিস্তরের সাধারণ ইলেকট্রন বিন্যাস ns2np0
নিষ্ক্রিয় গ্যাসগুলো অধিকতর স্থিতিশীল হওয়ার কারণ দ্বিত্ব ও অষ্টক পূর্ণ ।
নিষ্ক্রিয় গ্যাসগুলো রাসায়নিকভাবে আসক্তিহীন হওয়ার কারণ অধিকতর স্থিতিশীলতা ।
যৌগ গঠনে মৌলের পরমাণুসমূহ ইলেকট্রন আদান-প্রদান বা শেয়ার করে দ্বিত্ব বা অষ্টক পূরণের প্রবণতা ।
অণু গঠনকালে ইলেকট্রন গ্রহণ করে হিলিয়ামে ইলেকট্রন বিন্যাস প্রাপ্ত হয় হাইড্রোজেন (H)।
রাসায়নিক বন্ধন গঠনের মূল কারণ দ্বিত্ব বা অস্টক লাভের প্রবণতা।
অণুতে পরমাণুসমূহ যে আকর্ষণের মাধ্যমে একে অপরের সাথে যুক্ত থাকে তাকে রাসায়নিক বন্ধন বলে ।
ক্যাটায়ন তৈরি হয় ইলেকট্রন দান করে ।
অ্যানায়ন তৈরি হয় ইলেকট্রন গ্রহণ করে ।
ধনাত্মক চার্জযুক্ত পরমাণুকে ক্যাটায়ন বলা হয় ।
ঋণাত্মক চার্জযুক্ত পরমাণুকে অ্যানায়ন বলা হয় ।
সাধারণত ধাতব মৌলসমূহ ক্যাটায়ন সৃষ্টি করে।
পর্যায় সারণির একটি পর্যায়ের বাম থেকে ডানে গেলে ধাতব ধর্মের হ্রাস পায় ।
যেকোনো পর্যায়ের ডানের মৌলসমূহ সাধারণত অধাতু।
এর মধ্যে কোনটি ক্যাটায়ন Na ।
Mg2+, F-. Na এর মধ্যে F- অ্যানায়ন।
Na+ ক্যাটায়নে ইলেকট্রন সংখ্যা 10।
Ca2+, Cl- আয়ন দুটিতে ইলেকট্রন কণিকার সংখ্যা সমান ।
ধাতুসমূহের সর্বশেষ শক্তিস্তরের ইলেকট্রনগুলো নিউক্লিয়াস থেকে দূরে থাকার কারণ পারমাণবিক আকার বড় ।
অধাতুসমূহের সর্বশেষ শক্তিস্তরে সাধারণত 5,6 বা 7 টি ইলেকট্রন থাকে ।
ধাতুসমূহের সর্বশেষ শক্তিস্তরে সাধারণত 1, 2 বা 3 টি ইলেকট্রন থাকে ।
অধাতুসমূহের আয়নিকরণ শক্তির মান অনেক বেশি ।
অধাতুসমূহ ক্যাটায়ন তৈরি করে না আয়নিকরণ শক্তির মান বেশি তাই।
CI- আয়ন Ar মৌলের ইলেকট্রন বিন্যাসের অনুরূপ ।
অধাতুসমূহ সহজেই অ্যানায়নে পরিণত হওয়ার কারণ ইলেকট্রন আসক্তি বেশি ।
ক্যাটায়ন ও অ্যানায়নের মধ্যে ইলেকট্রোস্ট্যাটিক বল কাজ করে ।
তড়িৎযোজী বন্ধনে ক্যাটায়ন ও অ্যানায়ন পরস্পরের সাথে যুক্ত থাকে।
MgO. KF. NaCl যৌগগুলোর মধ্যে MgO এর প্রতিটি পরমাণুই নিয়ন গ্যাসের কাঠামো লাভ করে।
NaCl অণুটিতে আয়নিক বন্ধন বিদ্যমান।
শেষ শক্তিস্তরে কম সংখ্যক ইলেকট্রন থাকে ধাতুর ।
CaO, HCl, H2O এর মধ্যে CaO আয়নিক যৌগ।
ম্যাগনেসিয়াম পরমাণু ২টি ইলেকট্রন ত্যাগ করে Neপরমাণুর স্থায়ী অষ্টক বিন্যাস লাভ করে ।
আয়নিক বন্ধন গঠনে Mg পরমাণু Mg2+ আয়ন সৃষ্টি করে ।
MgO অণুতে Mg 2 টি ইলেকট্রন ত্যাগ করে স্থিতিশীল কাঠামো অর্জন করে ।
NaH অণুতে H পরমাণু হিলিয়াম (He)মৌলের স্থিতিশীল কাঠামো অর্জন করে ।
CaO যৌগে বিদ্যমান ক্যাটায়ন ও অ্যানায়ন হলো Ca2+,O2-
গ্রুপ 13 এর অ্যালুমিনিয়াম (AI3+)মৌলটি ক্যাটায়ন গঠন করে।
আয়নিক বন্ধন খুব শক্তিশালী হওয়ার কারণ স্থির বৈদ্যুতিক আকর্ষণ বল।
দুটি ক্লোরিন পরমাণু মিলে ক্লোরিন অণু তৈরি করে ।
দুটি অধাতব পরমাণুর মধ্যে ইলেকট্রন শেয়ারের মাধ্যমে বন্ধন গঠিত হয় ।
দুটি অধাতব পরমাণুর মধ্যে সমযোজী বন্ধন গঠিত হয় ।
N2 অণুতে বন্ধন ইলেকট্রন তিন জোড়া।
পানির একটি অণুতে অক্সিজেনের ২টি নিঃসঙ্গ ইলেকট্রন জোড় আছে ।
N2 অণু গঠনকালে পরমাণু দুটি কয়টি করে ইলেকট্রন শেয়ার করে ।
সমযোজী অণুসমূহের মধ্যে ভ্যানডার ওয়ালস শক্তি বিদ্যমান।
ইলেকট্রন শেয়ারের মাধ্যমে সমযোজী বন্ধন গঠিত হয় ।
প্রতিটি সমযোজী বন্ধনে 2 টি ইলেকট্রন অংশগ্রহণ করে ।
সালফার অণুর সংকেত S8
অক্সিজেন পরমাণুর সর্বশেষ শক্তিস্তরে অষ্টক অপেক্ষা 2টি ইলেকট্রন কম আছে।
O2 এর গাঠনিক সংকেত O=O ।
H2O অণুতে 2 টি সমযোজী বন্ধন বিদ্যমান ।
H2O অণুতে অক্সিজেন পরমাণুর 4 টি ইলেকট্রন বন্ধন গঠন করেন।
N2, Cl, Br2, HCI এর মধ্যে HCI সমযোজী যৌগ।
এর মধ্যে কোনটি স্বাভাবিক তাপমাত্রা ও চাপে তরল অবস্থায় থাকে
C10H8 স্বাভাবিক তাপমাত্রায় কঠিন অবস্থায় থাকে ।
CO2 একক অণু হিসেবে ঘুরে বেড়ানোর কারণ ভ্যানডার ওয়ালস শক্তির অনুপস্থিতি ।
একক অণু হিসেবে ঘুরে বেড়ায় এমন তিনটি যৌগের নাম CO2, NH3, O2 ।
ধাতুর অণুগুলো আয়নে পরিণত হলে ত্রিমাত্রিক কেলাসে অবস্থান করে ।
আয়নিক যৌগ দ্রবণীয় অবস্থায় বিদ্যুৎ পরিবহন করতে পারে ।
আয়নিক যৌগের গলনাঙ্ক ও স্ফুটনাঙ্ক অনেক বেশি হওয়ার কারণ শক্তিশালী ইলেকট্রোস্ট্যাটিক বল ।
এর মধ্যে যৌগটি পোলার ।
কাপড় কাচার সোড়ার সংকেত ।
তুঁতের সংকেত
আয়নিক যৌগ হওয়া সত্ত্বেও পানিতে অদ্রবণীয় একটি যৌগের নাম সিলভার ক্লোরাইড (AgCl) ।
পোলার সমযোজী যৌগ পানিতে দ্রবণীয় ।
সমযোজী বন্ধনীস্থ ইলেকট্রন যুগলকে কোনো পরমাণুর নিজের দিকে আকর্ষণ করার ক্ষমতাকে তড়িৎ ঋণাত্মকতা বলে ।
CH3OH সমযোজী যৌগ হলেও পানিতে দ্রবণীয় পোলার যৌগ বলে।
গ্রাফাইট মূলত কার্বনের রূপভেদ।
আয়নিক যৌগ জলীয় দ্রবণে বিদ্যুৎ পরিবহন করে ।
বিদ্যুৎ পরিবহনের জন্য ধনাত্মক বা ঋণাত্মক আয়ন প্রয়োজন ।
C6H12O6, বিদ্যুৎ পরিবহন করে না আয়নিক হয় না বলে।
ধাতব বন্ধনের মূল কারণ ইলেকট্রনের প্রতি ধাতব আয়নের স্থির বৈদ্যুতিক আকর্ষণ বল।
এক খণ্ড ধাতুর মধ্যে পরমাণুসমূহ যে আকর্ষণের মাধ্যমে যুক্ত থাকে তাকে ধাতব বন্ধন বলে ।
ধাতব পরমাণুর সৃষ্ট ধনাত্মক আয়নকে পারমাণবিক শাঁস বলে।
ধাতুর বিদ্যুৎ পরিবাহিতা ও তাপ পরিবাহিতার কারণ সঞ্চরণশীল ইলেকট্রন ।
ধাতব স্ফটিকে পারমাণবিক শাঁসগুলো ত্রিমাত্রিকভাবে বিন্যস্ত থাকে ।
পারমাণবিক শাঁসের মধ্যবর্তী স্থানের মুক্ত ইলেকট্রনকে সঞ্চরণশীল ইলেকট্রন বলে।
কোনো মৌলের ইলেকট্রন বিন্যাসে সর্বশেষ কক্ষপথে যে ইলেকট্রন বা ইলেকট্রনসমূহ থাকে তার সংখ্যাকে বলা হয় যোজ্যতা ইলেকট্রন। উদাহরণস্বরূপ, ফ্লোরিনের ইলেকট্রন বিন্যাসে সর্বশেষ কক্ষপথে যথাক্রমে 7টি ইলেকট্রন থাকে। তাই ফ্লোরিন (F) এর যোজ্যতা ইলেকট্রন 7। যেমন-

জানা আছে, কোনো মৌলের ইলেকট্রন বিন্যাস সর্বশেষ কক্ষপথে যে কয়টি ইলেকট্রন থাকে, সেটাই হচ্ছে উক্ত মৌলের যোজনী ইলেকট্রন বলে। যেমন,

নাইট্রোজেন (N) এর পারমাণবিক সংখ্যা 7। এর ইলেকট্রন বিন্যাস নিয়ে পাই,

Ca এর পারমাণবিক সংখ্যা 20। এর ইলেকট্রন বিন্যাস নিয়ে পাই-
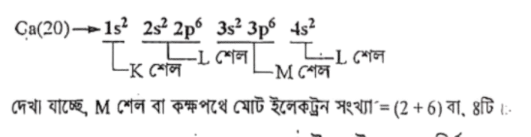
CI এর পারমাণবিক সংখ্যা 17। এর ইলেকট্রন বিন্যাস করে পাই-
অণু গঠনকালে কোনো মৌলের একটি পরমাণুর সাথে অপর একটি মৌলের পরমাণু যুক্ত হওয়ার ক্ষমতাকে যোজনী বা যোজ্যতা বলে। কোনো মৌলের একটি পরমাণু যতগুলো H বা CI পরমাণুর সাথে যুক্ত হতে পারে সেই সংখ্যাই হলো ঐ মৌলের যোজ্যতা। যেমন O এর ১টি পরমাণু H-এর ২টি পরমাণুর সাথে যুক্ত হয়ে H2O তৈরি। তাই O এর যোজনী ২।
কোনো মৌলের ইলেকট্রন বিন্যাসে সর্বশেষ কক্ষপথে বিজোড় ইলেকট্রন সংখ্যাই ঐ মৌলের যোজনী। ক্ষারধাতুসমূহের প্রত্যেকের সর্বশেষ কক্ষপথে । টি বিজোড় ইলেকট্রন বিদ্যমান, তাই ক্ষারধাতুসমূহের যোজনী। যেমন, Na. K. Rb ইত্যাদি।
Na এর যোজনী বা যোজ্যতা ।, কারণ Na এর ১টি পরমাণু ১টি ক্লোরিন (CI) পরমাণুর সাথে যুক্ত হয়ে NaCl গঠিত হয়। সুতরাং, Na এর যোজ্যতা 1 (এক)।
ক্যালসিয়ামের ইলেকট্রন বিন্যাস নিয়ে পাই,
দেখা যাচ্ছে, Ca ধাতব মৌলের সর্বশেষ শক্তিস্তরে s অরবিটালে ২টি ইলেকট্রন রয়েছে, যা ত্যাগ করে ক্যাটায়নে (Ca2+) পরিণত হয়। তাই Ca এর যোজনী 2 ।
জানা আছে, ১টি পরমাণুর সাথে যতটি অক্সিজেন পরমাণু যুক্ত হয়, সে সংখ্যার দ্বিগুণ করলে ঐ পরমাণুর যোজ্যতা বা যোজনী হয়। Ba এর ১টি পরমাণু ১টি ০ পরমাণুর সাথে যুক্ত হয়ে BaO তৈরি করে। এখানে O পরমাণুর সংখ্যা 1, যাকে 2 দ্বারা গুণ করলে হয় 2 । কাজেই Ba এর যোজনী 2 ।
12Mg এর ইলেকট্রন বিন্যাস নিয়ে পাই -
দেখা যাচ্ছে, Mg এর সর্ববহিঃস্থ শেলে ২টা e- আছে। তাই Mg-এর যোজনী 2। অন্যভাবে বলা যায়, Mg এর নিকটস্থ নিষ্ক্রিয় মৌল Ne এর নিষ্ক্রিয় চরিত্র অর্জন করতে ২টা e- ত্যাগ করতে হয়। তাই Mg এর যোজনী 2।
ম্যাগনেশিয়াম (Mg) এর e- বিন্যাস নিয়ে পাই
Mg(12)→1s2 2s22p6 3s2
দেখা যাচ্ছে, Mg এর সর্ববহিঃস্থ শক্তিস্তরে মাত্র 2টি e- রয়েছে। তাই এর যোজ্যতা ইলেকট্রন 2। আবার Mg এর বহিঃস্থ স্তরের e- ২টি ত্যাগ করে নিকটস্থ নিষ্ক্রিয় চরিত্র অর্জন করে ক্যাটায়নে পরিণত হয়ে যৌগ গঠন করে। তাই Mg এর যোজনীও 2 ।
সুতরাং বলা যায়, Mg এর যোজ্যতা ইলেকট্রন ও যোজনী উভয়ই 2 অর্থাৎ একই।
15X ইলেকট্রন বিন্যাস-
X(15)=1s22s22p 3s2 3px1 3py 13pz1
এটি একটি অধাতু এবং এর শেষ কক্ষপথে বিজোড় ইলেকট্রন সংখ্যা 3। সুতরাং, X এর যোজ্যতা ও। ইলেকট্রন বিন্যাস থেকে দেখা যায়, এর সর্বশেষ প্রধান শক্তিস্তরে ১টি ইলেকট্রন আছে। তাই X এর যোজ্যতা ইলেকট্রন 5। সুতরাং দেখা যাচ্ছে 15Xএর যোজ্যতা ও যোজ্যতা ইলেকট্রন একই নয়।
C এর ইলেকট্রন বিন্যাস: C(6) = 1s2 2s22p2
দেখা যাচ্ছে, C এর যোজ্যতান্তরে 4টি ইলেকট্রন আছে। তাই কার্বনের যোজ্যতা ইলেকট্রন 4। আবার, কার্বন অধাতু হওয়ায় কার্বনের যোজ্যতা স্তরের বিজোড় e- কে যোজ্যতা বলে।
ক্লোরিন (CI)-এর ইলেকট্রন বিন্যাস-
ইলেকট্রন বিন্যাস থেকে দেখা যায়, এতে যোজ্যতা স্তরে বিজোড় ইলেকট্রন। হওয়ায় যোজনী-। এবং যোজ্যতা স্তরের ইলেকট্রন সংখ্যা 7টি হওয়ায় যোজ্যতা ইলেকট্রন 7 । এ কারণেই অধাতব মৌল CI এর যোজ্যতা ইলেকট্রন ও যোজনী ভিন্ন।
ফ্লোরিনের (F) যোজনী ও যৌজনী ইলেকট্রন ভিন্ন। কারণ F এর ইলেকট্রন বিন্যাস হতে পাই-

ইলেকট্রন বিন্যাস থেকে দেখা যায়, মৌলটির যোজ্যতাস্তরে বিজোড় ইলেকট্রন সংখ্যা 1.। অর্থাৎ যোজনী। এবং যোজ্যতা স্তরে মোট ইলেকট্রন সংখ্যা 7। তাই এর যোজনী ইলেকট্রন 7।
Na(11) ও Cl(17) এর ইলেকট্রন বিন্যাস :
দেখা যাচ্ছে, Na পরমাণুর যোজ্যতা স্তরে। টি মাত্র ইলেকট্রন আছে। এজন্য Na এর যোজনী ।। অপরদিকে C'I পরমাণুর যোজ্যতা স্তরে 7টি ইলেকট্রন আছে। অর্থাৎ অষ্টক পূর্ণ অপেক্ষা। টি ইলেকট্রন কম আছে। তাই এটি 1টি ইলেকট্রন গ্রহণ করে CI আয়নে পরিণত হয়। এজন্য CI এর যোজনী । অর্থাৎ 11Na ও 11CI এর যোজনী একই।
০ এর ইলেকট্রন বিন্যাস নিয়ে পাই,

দেখা যাচ্ছে, অধাতব পরমাণু অক্সিজেন (০) শেষ কক্ষপথে বিজোড় ইলেকট্রন সংখ্যা 2। সুতরাং অক্সিজেনের যোজনী 2। আবার, ইলেকট্রন বিন্যাস হতে, অক্সিজেনের সর্বশেষ প্রধান শক্তিস্তরে ইলেকট্রন সংখ্যা হলো (2+4) = 6টি। অর্থাৎ যোজ্যতা ইলেকট্রন 6 ।
সুতরাং অক্সিজেনের যোজনী ও যোজনী ইলেকট্রন যথাক্রমে 2 ও 6, যা সমান নয়।
N এর ইলেকট্রন বিন্যাস হচ্ছে,
N(7): 1s2 2s2 2px1 2py1 2pz1
N এর বহিঃস্থ স্তরে ৩টি অযুগ্মা ইলেকট্রন রয়েছে।
অর্থাৎ, নাইট্রোজেনের যোজনী তিন। অপরদিকে নাইট্রোজেনের সর্বশেষ শক্তিস্তরে মোট ১টি ইলেকট্রন থাকায় এর যোজ্যতা ইলেকট্রন 5। সুতরাং, দেখা যাচ্ছে, N এর যোজনী ও এবং যোজ্যতা ইলেকট্রন 5. যা ভিন্ন।
Li এর যোজনী ও যোজ্যতা ইলেকট্রন একই। কারণ Li এর ইলেকট্রন বিন্যাস , Li(3) = 1s2 2s1
জানা আছে, কোনো মৌলের ইলেকট্রন বিন্যাসে সর্বশেষ কক্ষপথে যতটি ইলেকট্রন থাকে সেটি তার যোজ্যতা ইলেকট্রন। Li এর যোজাতা স্তরে। টি ইলেকট্রন থাকায় এর যোজ্যতা ইলেকট্রন।। আবার Li পরমাণু যোজ্যতা স্তরের 1টি ইলেকট্রন দান করে নিকটস্থ নিষ্ক্রিয় গ্যাস Hc এর ইলেকট্রন বিন্যাস লাভ করে বলে Li এর যোজনীও। ।
CI এর ইলেকট্রন বিন্যাস-
ইলেকট্রন বিন্যাস থেকে দেখা যায়, এতে যোজ্যতা স্তরে বিজোড় ইলেকট্রন। হওয়ায় যোজনী-। এবং যোজ্যতা স্তরের ইলেকট্রন সংখ্যা 7টি হওয়ায় যোজ্যতা ইলেকট্রন 7 । এ কারণেই অধাতব মৌল CI এর যোজ্যতা ইলেকট্রন ও যোজনী ভিন্ন।
কোনো মৌলের সর্বোচ্চ যোজনী এবং সক্রিয় যোজনীর পার্থক্যকে ঐ মৌলের সুপ্ত যোজনী বলা হয়। যেমন- ফেরিক ক্লোরাইড (FeCl3) যৌগে Fc এর সক্রিয় যোজনী 3, কিন্তু Fe এর সর্বোচ্চ যোজনী 3 ।
সুতরাং, FeCl3, যৌগে Fc এর সুপ্ত যোজনী = (3-3) = 0 ।
জানা আছে, কোনো মৌলের সর্বোচ্চ যোজনী ও সক্রিয় যোজনীর পার্থক্যকে ঐ মৌলের সুপ্ত যোজনী বলা হয়। ফসফরাস ট্রাইক্লোরাইড (PCI3) যৌগটিতে P এর সক্রিয় যোজনী 3। আবার P এর সর্বোচ্চ যোজনী 5 । সুতরাং , PCI3, যৌগটিতে P এর সুপ্ত যোজনী =(5-3)=2
কোনো মৌলের সর্বোচ্চ যোজনী ও সক্রিয় যোজনীর পার্থক্যকে ঐ মৌলের সুপ্ত যোজনী বলে। সালফার ট্রাইঅক্সাইড (SO3) যৌগে S এর সক্রিয় যোজনী 6 এবং S এর সর্বোচ্চ যোজনীও 6 । সুতরাং SO3 যৌগে S এর সুপ্ত যোজনী =6-6=0 ।
কোনো মৌলের সর্বোচ্চ যোজনী ও সক্রিয় যোজনীর পার্থক্যকে ঐ মৌলের সুপ্ত যোজনী বলে। কার্বন মনোক্সাইড (CO) যৌগে কার্বন (C) এর সক্রিয় যোজনী ২। কিন্তু এর সর্বোচ্চ যোজনী 4 ।
সুতরাং, CO যৌগে কার্বনের সুপ্ত যোজনী = 4-2=2 ।
যদি কোনো মৌলের একাধিক যোজনী থাকে সেই মৌলের যোজনীকে বলে পরিবর্তনশীল যোজনী। যেমন, Sn এর পরিবর্তনশীল যোজনী 2 ও4। আবার P এর পরিবর্তনশীল যোজনী 3 ও5। এভাবে - কোনো মৌলের একাধিক যোজনী থাকলেই, সেই যোজনী পরিবর্তনশীল যোজনী নামে পরিচিত।
ফসফরাস (P) এর স্বাভাবিক ও উত্তেজিত অবস্থায় ইলেকট্রন বিন্যাস হলো-
ইলেকট্রন বিন্যাস হতে দেখা যায় উত্তেজিত অবস্থায় 3s থেকে। টি
বিন্যাস হলো-ইলেকট্রন 3d অরবিটালে গমন করে ফলে P এর তাস্টক সম্প্রসারণ ঘটে। এ কারণে P পরিবর্তনশীল যোজ্যতা প্রদর্শন করে।
সালফার পরিবর্তনশীল যোজনী প্রদর্শন করে। সালফার এর স্বাভাবিক ও উত্তেজিত অবস্থায় ইলেকট্রন বিন্যাস নিম্নরূপ-
যোজনী 2
যোজনী 4
যোজনী 6
স্বাভাবিক অবস্থায় সালফারের যোজনী-2 হলেও উত্তেজিত অবস্থায় যোজনী 4, 6 হয়। অর্থাৎ S এর একাধিক (2, 4 ও 6) যোজনী রয়েছে।
কার্বনের ইলেকট্রন বিন্যাস :
যোজ্যতা স্তরে 2টি বিজোড় ইলেকট্রন থাকায় যোজ্যতা 2 । কিন্তু উত্তেজিত অবস্থায় ' এর ইলেকট্রন বিন্যাস:
যোজ্যতা স্তরে 4টি বিজোড় ইলেকট্রন থাকায় যোজ্যতা 4। অর্থাৎ কার্বন ২.ও 4 তথা একাধিক যোজ্যতা প্রদর্শন করে।
জানা আছে, ।টি পরমাণুর সাথে যতটি অক্সিজেন পরমাণু যুক্ত হয়, সে সংখ্যার দ্বিগুণ করলেই ঐ পরমাণুর যোজনী হয়। এক্ষেত্রে S এর ১টি পরমাণু ২টি পরমাণুর সাথে যুক্ত হয়ে SO2 যৌগ উৎপন্ন করেছে। এখানে O পরমাণুর সংখ্যা 2, যাকে 2 দ্বারা গুণ করলে হয় (22) বা 4। অর্থাৎ, S এর যোজনী 4 ।
জানা আছে, ১টি পরমাণুর সাথে যতটি O পরমাণু যুক্ত হয়, সে সংখ্যার দ্বিগুণ করলেই ঐ পরমাণুর যোজনী হয় । এক্ষেত্রে ১ এর ১টি পরমাণু 3টি () পরমাণুর সাথে যুক্ত হয়ে SO, তৈরি করেছে। এখানে O পরমাণুর সংখ্যা 3, যাকে 3 দ্বারা গুণ করলে হয় বা 6 ।
অর্থাৎ, ৪ এর যোজনী 6 ।
একাধিক মৌলের কতিপয় পরমাণু বা আয়ন পরস্পরের সাথে মিলিত হয়ে ধনাত্মক বা ঋণাত্মক আধানবিশিষ্ট একটি পরমাণুগুচ্ছ তৈরি করে এবং এটি একটি মৌলের আয়নের ন্যায় আচরণ করে; এ ধরনের পরমাণুগুচ্ছকে যৌগমূলক বলা হয়। এটি ধনাত্মক বা ঋণাত্মক আধানবিশিষ্ট হতে পারে। উদাহরণস্বরূপ , SO42- একটি ঋণাত্মক যৌগমূলক, যা 1টি' ও.4টি পরমাণুর সমন্বয়ে গঠিত এবং এর যোজনী 2 ।
NH4+ একটি যৌগমূলক। কারণ এটি একাধিক মৌলের তথা 1টি N পরমাণু ও 4টি H পরমাণুর সমন্বয়ে গঠিত একটি ধনাত্মক আধানযুক্ত-মূলক। রাসায়নিক বিক্রিয়ায় NH4+ একটি মাত্র পরমাণুর ন্যায় আচরণ করে এবং বিক্রিয়া শেষে অপরিবর্তিত থাকে।
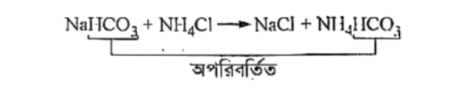
হাইড্রোজেন কার্বনেট (HCO-3) একটি ঋণাত্মক যৌগমূলক বা পরমাণুগুচ্ছ। কারণ HCO, আয়নটি ঋণাত্মক আধানবিশিষ্ট, যা একাধিক পরমাণু (H, C, O) এর সমন্বয়ে গঠিত। রাসায়নিক বিক্রিয়ায় একটিমাত্র পরমাণুর ন্যায় আচরণ করে বিক্রিয়া শেষে অপরিবর্তিত থাকে। যেমন-
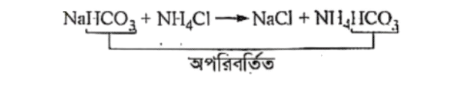
নাইট্রেট একটি যৌগমূলক। কারণ NO3- আয়নটি ঋণাত্মক আধানবিশিষ্ট, যা একাধিক পরমাণু সমন্বয়ে গঠিত। রাসায়নিক বিক্রিয়ায় এটি একটি মাত্র পরমাণুর ন্যায় আচরণ করে এবং বিক্রিয়া শেষে অপরিবর্তিত থাকে। যেমন :
কার্বনেট কে যৌগমূলক বলা হয়। কারণ মূলকটি 1টি C পরমাণু ও ওটি ০ পরমাণুর সমন্বয়ে গঠিত, যা একটি মাত্র পরমাণুর ন্যায় আচরণ করে এবং বিক্রিয়া শেষে অপরিবর্তিত থাকে।

সালফেট কে যৌগমূলক বলা হয়। কারণ মূলকটি একাধিক পরমাণুর সমন্বয়ে গঠিত, রাসায়নিক বিক্রিয়ায় একটিমাত্র পরমাণুর ন্যায় আচরণ করে এবং বিক্রিয়া শেষে অপরিবর্তিত থাকে। যেমন- Zn + H2SO4 → ZnSO4 + H2(g)
বিক্রিয়া থেকে দেখা যায়, বিক্রিয়ক ও উৎপাদে SO42- এর কোনো পরিবর্তন হয়নি। সুতরাং SO42- একটি যৌগমূলক।
অ্যামোনিয়াম একটি ধনাত্মক যৌগমূলক। যৌগমূলকটিতে ১টি N পরমাণুর সাথে ৩টি H পরমাণু ও ১টি যুক্ত হয়ে অ্যামোনিয়াম আয়ন নামক যৌগমূলক সৃষ্টি করেছে। এর আধান সংখ্যা +1 । আয়ন ধাতুর ন্যায় ক্রিয়াশীল, যা অধাতব আয়ন এর সাথে যুক্ত হয়ে যৌগ গঠন করে যেমন - NH4OH, (NH4)2SO4 ইত্যাদি ।
মৌল বা যৌগমূলকের প্রতীক বা সংকেত ও তাদের সংখ্যার মাধ্যমে কোনো যৌগ অণুকে প্রকাশ করাই হলো উক্ত যৌগের রাসায়নিক সংকেত (Chemical Formula)। যেমন- একটি নাইট্রোজেন (N) পরমাণু ও তিনটি হাইড্রোজেন (H) পরমাণু মিলে অ্যামোনিয়া (NH3) অণু গঠিত হয়।
সুতরাং, NH3 হলো অ্যামোনিয়া অণুর রাসায়নিক সংকেত।
সোডিয়াম এর প্রতীক Na এবং এর যোজনী + 1 । ফ্লোরিন এর প্রতীক F এবং এর যোজনী ।
এখন, Na-ও F মৌলদ্বয় দ্বারা গঠিত যৌগের সংকেত: NaF ।
Na2SO4 হলো সোডিয়াম সালফেটের রাসায়নিক সংকেত। এ সংকেতটি তৈরিতে প্রায়োগিক দুইটি নিয়ম হলো-
১. প্রথমে ধাতব মৌলটির (Na) প্রতীকের সাহায্যে এবং অধাতব পরমাণু গুচ্ছ তথা যৌগমূলক (SO4) এর সংকেত শেষে লেখা হয়েছে।
২. SO4 মূলকের যোজনী (2) ১ম মৌল (Na) এর ডানে একটু নিচে লেখা হয়েছে এবং Na এর যোজনী (1) SO4 এর ডানে লেখা হয়েছে; এক্ষেত্রে 1 উহ্য রয়েছে।
পটাশিয়াম (K) মৌল, SO4 ও CO3 যৌগমূলক দ্বারা গঠিত ২টি যৌগের সংকেত হলো-
| যৌগের নাম | রাসায়নিক সংকেত |
| পটাশিয়াম সালফেট | K2SO4 |
| পটাশিয়াম কার্বনেট | K2CO3 |
অ্যামোনিয়াম ফসফেটের রাসায়নিক সংকেত : (NH4)3PO4, NH4)3, PO4 যৌগটিতে-

অ্যালুমিনিয়াম সালফেটের রাসায়নিক সংকেত : Al2(SO4)3 ।
এখন , Al2(SO4)3 যৌগটিতে -
SO4মূলক-এ অক্সিজেন (০) পরমাণু রয়েছে।
SO4 মূলক রয়েছে = 3টি
∴ O পরমাণুর সংখ্যা = টি
সুতরাং , Al2(SO4)3 যৌগটিতে অক্সিজেন (O) পরমাণুর সংখ্যা 12টি।
NH3 ও NH4 +এর মধ্যে পার্থক্য:
| NH3 | NH4 + |
১. নিরপেক্ষ যৌগ। ২. মোট চার্জের পরিমাণ শূন্য। ৩. এক জোড়া মুক্তজোড় ইলেকট্রন বিদ্যমান । | ১. যৌগমূলক বা চার্জিত যৌগ। ২. মোট চার্জের পরিমাণ+। ৩. মুক্তজোড় ইলেকট্রন নেই। |
ধরি, ধনাত্মক যৌগমূল: NH4 +
ঋণাত্মক যৌগমূলক: SO42-
খঋণাত্মক যৌগমূলক্ : PO43-
উক্ত যৌগমূলক দ্বারা গঠিত ২টি যৌগের সংকেত: ১) (NH4)PO4 (২) (NH4)2SO4 ।
হচ্ছে ধনাত্মক যৌগমূলক, যার যোজনী + 1
আবার OH- , SO42- হচ্ছে ঋণাত্মক যৌগমূলক, যাদের যোজনী যথাক্রমে -1, -2 ।

| প্রদত্ত যৌগের নাম | রাসায়নিক সংকেত |
| ১. অ্যামোনিয়াম কার্বনেট | (NH4)2CO3 |
| ২. ক্যালসিয়াম ফসফেট | Ca3(PO4)2 |
বোরনের প্রতীক = B
নাইট্রোজেন প্রতীক = N
আবার, B ও N এর উভয়ের যোজনী 3। এদের 3 দ্বারা ভাগ করলে
যোজনী হয় । ও ।
সুতরাং, বোরন নাইট্রাইডের সংকেত: B1N1, রা BN ।
ফেরিকের প্রতীক ও যোজনী = Fe(III)।
সালফেটের যৌগমূলকের সংকেত ও যোজনী = SO42-
নিয়মানুযায়ী আয়রন তথা, ফেরিক এর যোজনী সালফেট মূলকের ডানে একটু নিচে আবার সালফেটের যোজনী ফেরিক এর ডানে একটু নিচে বসিয়ে সংকেত লেখা হয়।
∴ ফেরিক সালফেটের সংকেত :
ফেরাস সালফেট যৌগে-
ফেরাস তথা আয়রনের প্রতীক ও যোজনী→ Fe, 2
সালফেট মূলক/আয়নের সংকেত ও যোজনী→ SO42-
অর্থাৎ, উভয়ের যোজনী 2। এই সংখ্যাটিকে 2 দ্বারা ভাগ করে। ও।
পাওয়া যায়। সুতরাং, ফেরাস সালফেটের সংকেত : FeSO4 |
একটি মৌল বা যৌগের অণুতে যে যে ধরনের মৌলের পরমাণু থাকে তাদের প্রতীক এবং যে মৌলের পরমাণু যতটি থাকে সেই সকল সংখ্যা দিয়ে প্রকাশিত সংকেতকে আণবিক সংকেত বলা হয়। যেমন, 4টি C পরমাণু 10টি H পরমাণুর সাথে যুক্ত হয়ে বিউটেন (C4H10) অণু গঠিত হয়। অর্থাৎ, বিউটেন এর আণবিক সংকেত: C4H10 ।
একটি অণুতে মৌলের পরমাণুগুলো যেভাবে সাজানো থাকে, প্রতীক এবং বন্ধনের মাধ্যমে তা প্রকাশ করাকে গাঠনিক সংকেত বলা হয়। যেমন বিউটেন যৌগে 4টি C' পরমাণু একে অপরের সাথে শিকলের আকারে যুক্ত হয় এবং অবশিস্ট যোজনীগুলো H দ্বারা পূর্ণ করে প্রতিটি C এর যোজনী 4 হয়।
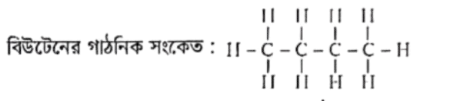
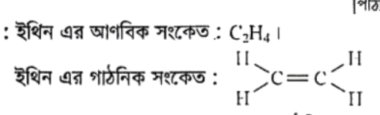
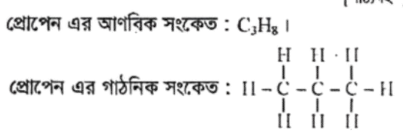
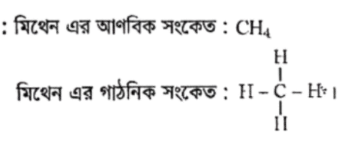

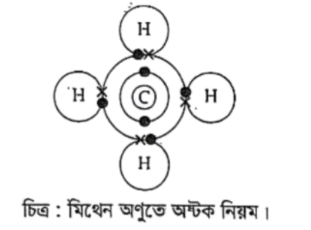
অণু গঠনকালে কোনো মৌল ইলেকট্রন গ্রহণ, বর্জন অথবা ভাগাভাগির মাধ্যমে তার সর্বশেষ শক্তিস্তরে ৮(৪) টি করে ইলেকট্রন ধারণের মাধ্যমে নিষ্ক্রিয় গ্যাসের ইলেকট্রন বিন্যাস লাভ করে। একেই অষ্টক নিয়ম বলা হয়। যেমন CO2 অণুটি গঠনের ক্ষেত্রে C ও O উভয়েই ইলেকট্রন শেয়ার করে সর্বশেষ শক্তিস্তরে ৪টি ইলেকট্রন অর্জন করেছে। ফলে নিকটস্থ নিষ্ক্রিয় গ্যাসের ইলেকট্রন বিন্যাস লাভ করেছে। অর্থাৎ, CO2 যৌগটি গঠনে অষ্টক নিয়ম অনুসৃত হয়েছে।
অণু গঠনে কোনো পরমাণুর সর্বশেষ শক্তিস্তরে এক বা একাধিক জোড়া ইলেকট্রন বিদ্যমান থাকবে, এটিই হচ্ছে 'দুই' এর নিয়ম। যেমন : BeCl2 অণুর কেন্দ্রীয় পরমাণু Be এর সর্বশেষ শক্তিস্তরে 2 জোড়া অর্থাৎ 4টি ইলেকট্রন বিদ্যমান- এটিই হচ্ছে 'দুই' এর নিয়ম।
CH4 যৌগটি গঠনে কেন্দ্রীয় পরমাণু কার্বন (C) ইলেকট্রন শেয়ার করে স্থিতিশীলতা অর্জন করেছে। ফলে যৌগটির কেন্দ্রীয় পরমাণু C এর সর্বশেষ শক্তিস্তরে 8টি ইলেকট্রন লাভ করেছে। অর্থাৎ অষ্টক নিয়ম অনুসৃত হয়েছে।
BeCl2 যৌগটির কেন্দ্রীয় পরমাণু Be এর বহিঃস্থ স্তরের 2টি e- 2টি ক্লোরিন পরমাণুকে দান করেছে। এক্ষেত্রে উভয়েই e- আদান-প্রদান করে স্থিতিশীলতা অর্জন করেছে। ফলে কেন্দ্রীয় পরমাণু Be এর সর্বশেষ শক্তিস্তরে 2 জোড়া বা 4টি e- লাভ করেছে। অর্থাৎ, দ্বিত নিয়মের প্রয়োগ ঘটেছে।
যেমন-
আর্গন (Ar) ও ক্রিপটন (Kr) হচ্ছে দুইটি নিষ্ক্রিয় গ্যাস। এদের ইলেকট্রন বিন্যাস নিম্নরূপ-
কোনো মৌলের সর্বশেষ শক্তিস্তরে 2টি ইলেকট্রন থাকলে তাকে দ্বিত বলে। সর্বশেষ শক্তিস্তরে দ্বিত্ব পূর্ণ থাকার কারণে নিষ্ক্রিয় গ্যাসগুলো অধিকতর স্থিতিশীল হয়। আর অধিকতর স্থিতিশীলতার কারণে নিষ্ক্রিয় গ্যাসগুলো ইলেকট্রন আদান-প্রদান করে না। ফলে যৌগও গঠন করে না।
কোনো মৌলের সর্বশেষ শক্তিস্তরে ৮(৪)টি ইলেকট্রন থাকলে তাকে অষ্টক বলে। সর্বশেষ শক্তিস্তরে অষ্টক পূর্ণ থাকার কারণে নিষ্ক্রিয় গ্যাসগুলো অধিকতর স্থিতিশীল হয়। আর অধিকতর স্থিতিশীলতার কারণে নিষ্ক্রিয় গ্যাসগুলো ইলেকট্রন আদান-প্রদান করে না বলেই যৌগও গঠন করতে পারে না।
আর্গন (Ar) নিষ্ক্রিয় গ্যাস। কারণ 18Ar এর (Is22s22p6 3s2 3p6) সর্ববহিঃস্থ স্তরে ইলেকট্রন দ্বারা, অস্টকপূর্ণ থাকে যা অত্যন্ত সুস্থিত। এ সুস্থিত ইলেকট্রন বিন্যাস ভাঙতে অনেক শক্তির প্রয়োজন। তাই Ar স্বাভাবিক অবস্থায় কোনো মৌলের সাথে যুক্ত হয় না। অর্থাৎ বহিঃস্থ স্তরের সুবিন্যস্ত ইলেকট্রন বিন্যাসের কারণে Ar নিষ্ক্রিয় তথা সক্রিয় নয়।
নিয়ন (Ne) এর ইলেকট্রন বিন্যাস নিম্নরূপ-
Ne(10) Is22s2 2p6
ইলেকট্রন বিন্যাস থেকে দেখা যাচ্ছে যে, Ne এর শেষ কক্ষপথে ৪টি ইলেকট্রন বিদ্যমান। ফলে তাদের ইলেকট্রনীয় কাঠামো অত্যন্ত স্থিতিশীল হয়। স্থিতিশীল ইলেকট্রনীয় গঠনের কারণে Ne অন্য কোনো মৌলের সাথে রাসায়নিক বিক্রিয়ায় অংশগ্রহণ করে না। তাই Ne এর যোজনী শূন্য।
Kr এর ইলেকট্রন বিন্যাস নিম্নরূপ-
Kr(36) = 1s2 2s2 2p6 3s2 3p6 3d10 4s2 4p6
ইলেকট্রন বিন্যাস থেকে দেখা যাচ্ছে যে, Kr এর শেষ কক্ষপথে ৪টি ইলেকট্রন বিদ্যমান। ফলে তাদের ইলেকট্রনীয় কাঠামো অত্যন্ত স্থিতিশীল হয়। স্থিতিশীল ইলেকট্রনীয় গঠনের কারণে Kr অন্য কোনো মৌলের সাথে রাসায়নিক বিক্রিয়ায় অংশগ্রহণ করে না। তাই Kr এর যোজনী শূন্য।
অণুতে পরমাণুসমূহ যে আকর্ষণের মাধ্যমে একে অপরের সাথে যুক্ত থাকে তাকেই বলা হয় রাসায়নিক বন্ধন। যেমন, HCI যৌগটিতে H ও CI পরমাণুর মধ্যে এক ধরনের আকর্ষণ বল কাজ করে; এ আকর্ষণ বলই হচ্ছে মূলত রাসায়নিক বন্ধন।
জানা আছে, প্রত্যেক মৌলই নিকটস্থ নিষ্ক্রিয় গ্যাসের চরিত্র অর্জনের জন্যই মূলত ইলেকট্রনের দান-প্রদান ও শেয়ার করে। এর ফলে তাদের মধ্যে এক ধরনের আকর্ষণ বলের সৃষ্টি হয়, যা রাসায়নিক বন্ধন নামে পরিচিত। তাই বলা যায়, রাসায়নিক বন্ধন গঠনের মূল কারণ হচ্ছে পরমাণুর সর্বশেষ শক্তিস্তরে ইলেকট্রনসমূহের দ্বিত বা অষ্টক পূর্ণতা তথা নিষ্ক্রিয় গ্যাসের স্থিতিশীল লাভের প্রবণতা।
ধনাত্মক আধান বা পজিটিভ চার্জবিশিষ্ট আয়নকে বলা হয় ক্যাটায়ন। সাধারণত ধাতব মৌলসমূহ তাদের সর্ববহিস্থ শক্তিস্তরের এক বা একাধিক ইলেকট্রন ত্যাগ করে ক্যাটায়নে পরিণত হয়। যেমন; K ধাতব মৌলটি সর্বশেষ শক্তিস্তরের ৫ টি ত্যাগ করে K' ক্যাটায়নে পরিণত হয়।
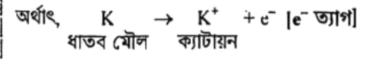
ঋণাত্মক আধান বা নেভেটিভ চার্জবিশিষ্ট অধাতব পরমাণুকে -অ্যানায়ন বলে। যেমন- ক্লোরিন (CI) পরমাণু এর সর্বশেষ শক্তিস্তরে ।টি গ্রহণ করে নিকটস্থ নিষ্ক্রিয় গ্যাস Ar এর স্থিতিশীলতা অর্জন করে। ফলে CI ঋণাত্মক আধানে তথা অ্যানায়নে পরিণত হয়।
অর্থাৎ
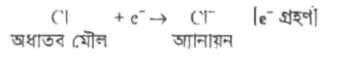
ক্যাটায়ন ও অ্যানায়নের মধ্যে ২টি পার্থক্য নিম্নরূপ-
| ক্যাটায়ন | অ্যানায়ন |
| ১. ক্যাটায়নে ইলেকট্রনের চেয়ে প্রোটনের সংখ্যা বেশি থাকে। | ১. অ্যানায়নে প্রোটনের চেয়ে ইলেকট্রনের সংখ্যা বেশি থাকে। |
| ২. ক্যাটায়নের উদাহরণ : Ca2+, Mg2+, NH4 ইত্যাদি। | ২. অ্যানায়নের উদাহরণ: O2-, OH-, CI-, F- ইত্যাদি। |
যে সকল মৌল এক বা একাধিক ইলেকট্রন ত্যাগ করে ধনাত্মক আয়নে পরিণত হয় তাদেরকে ধাতু বলে। ধাতুর ইলেকট্রন ত্যাগের এই ধর্মকে ধাতব ধর্ম বলে। যে মৌলের পরমাণু যত সহজে ইলেকট্রন ত্যাগ করতে পারবে সেই মৌলের ধাতব ধর্ম তত বেশি। যেমন, পটাসিয়াম (K) একটি ধাতু। কারণ K 1টি ইলেকট্রন ত্যাগ কর K+ এ পরিণত হয়।
পর্যায় সারণিতে যেকোনো পর্যায়ে বাম থেকে ডানে ধাতব ধর্ম হ্রাস পায়।
যে সকল মৌলের সর্বশেষ শক্তিস্তরে কমসংখ্যক (1, 2 বা 3টি) ইলেকট্রন থাকে তাদের নিউক্লিয়াস বহিঃস্থ ইলেকট্রনের সাথে দুর্বলভাবে আকর্ষিত থাকে। ফলে এসব মৌলের পরমাণু সহজেই ইলেকট্রন ত্যাগ করে দ্বিত বা অষ্টক পূর্ণ করে। এভাবে ইলেকট্রন ত্যাগের মাধ্যমে নিউক্লিয়াসে ধনাত্মক চার্জের পরিমাণ বেড়ে যায় এবং ধনাত্মক চার্জযুক্ত পরমাণু বা ক্যাটায়নের সৃষ্টি হয়।
ধাতব পরমাণু যোজ্যতা স্তরের তথা শেষ স্তরের ইলেকট্রন ত্যাগ করে নিকটবর্তী নিষ্ক্রিয় গ্যাসের ইলেকট্রন কাঠামো অর্জন করে। এভাবে ইলেকট্রন ত্যাগ করে ধাতব পরমাণু ক্যাটায়নে রূপান্তরিত হয়। যেমন, Mg ধাতব পরমাণুর যোজ্যতা স্তরের 2টি e- ত্যাগ করে ক্যাটায়ন (Mg)-এ পরিণত হয়।
Mg → Mg2+ + 2e
যে সকল মৌলের সর্বশেষ শক্তিস্তরে 5, 6 বা 7টি ইলেকট্রন থাকে তাদের ক্ষেত্রে নিকটস্থ নিষ্ক্রিয় মৌলের ইলেকট্রন বিন্যাস অর্জনের জন্য প্রয়োজনীয় সংখ্যক ইলেকট্রন গ্রহণ করতে হয় এবং ফলে দ্বিত বা অষ্টকপূর্ণ কাঠামো গঠিত হয়। এভাবে ইলেকট্রন গ্রহণের ফলে পরমাণুটি ঋণাত্মক চার্জযুক্ত পরমাণু বা আয়ন গঠন করে তথা অ্যানায়ন গঠিত হয়।
ধাতব পরমাণু তার সর্বশেষ শক্তিস্তরের এক বা একাধিক ইলেকট্রনকে অধাতব পরমাণুর সর্বশেষ শক্তিস্তরে স্থানান্তর করে ধনাত্মক ও ঋণাত্মক আয়ন সৃষ্টির মাধ্যমে যে বন্ধন গঠিত হয়, তাই হচ্ছে আয়নিক বন্ধন। অর্থাৎ, ইলেকট্রন আদান-প্রদানের মাধ্যমে যে বন্ধন গঠিত হয় তাকে বলা হয় আণবিক বন্ধন। যেমন: আয়নিক বন্ধনের মাধ্যমে NaCl, KCI ইত্যাদি আয়নিক যৌগ গঠিত হয়।
MgO অণুতে Mg 2টি e- ত্যাগ করে নিকটস্থ নিস্ক্রিয় গ্যাস Ne এর e- বিন্যাস অর্জন করে এবং ক্যাটায়নে পরিণত হয়।
Mg → Mg2+ +2e-
আবার, () পরমাণু Mg এর ত্যাগকৃত e- ২টি গ্রহণ করে স্থিতিশীলতা অর্জন করে অ্যানায়নে পরিণত হয়।
O+2e- → O2-
উৎপন্ন Mg 2+ ও O2- আয়নন্বয় পরস্পরের সংযোগে MgO আয়নিক যৌগ গঠিত হয়।
ম্যাগনেসিয়ামের ইলেকট্রন বিন্যাস হলো-
12Mg Is2 2s22p6 3s2
ম্যাগনেশিয়াম পরমাণুর সর্ববহিঃস্থ কক্ষপথে ২টি ইলেকট্রন থাকায় ইলেকট্রন শেয়ার বা গ্রহণের মাধ্যমে অন্টকপূর্ণ করতে পারে না। কিন্তু Mg পরমাণুর সর্ববহিঃস্থ কক্ষপথের 2টি ইলেকট্রন সহজেই ত্যাগ করে অণ্টক পূর্ণ করতে পারে। তাই ম্যাগনেশিয়াম কেবল আয়নিক বন্ধনের মাধ্যমে আয়নিক যৌগ গঠন করতে পারে।
সোডিয়াম (Na) পরমাণুর ইলেকট্রন বিন্যাস-
Na(11) = 1s2 2s2 2p6 3s1
Na পরমাণুর সর্বশেষ শক্তিস্তরে ।টি মাত্র ইলেকট্রন থাকায় এটি সহজেই একটি ইলেকট্রন দান করে নিকটতম নিষ্ক্রিয় গ্যাস নিয়নের কাঠামো অর্জন করে। যেহেতু। টি ইলেকট্রন দান করে সেহেতু এটি অধাতুর সাথে যুক্ত হয়ে আয়নিক বন্ধন গঠন করে। ইলেকট্রন শেয়ারের মাধ্যমে সমযোজী বন্ধন গঠন করতে পারে না।
দুটি অধাতব পরমাণু তাদের সর্বশেষ শক্তিস্তরের একটি (এক বা একাধিক) ইলেকট্রনকে সরবরাহ করে একজোড়া ইলেকট্রন তৈরি করে। এরপর এই এক জোড়া ইলেকট্রন উভয় পরমাণু শেয়ারের মাধ্যমে যে বন্ধন গঠিত হয় তাই হচ্ছে সমযোজী বন্ধন। অর্থাৎ ইলেকট্রন শেয়ারের মাধ্যমে দু'টি অধাতব পরমাণুর মধ্যে যে বন্ধন গঠিত হয় তা হচ্ছে সমযোজী বন্ধন। সমযোজী বন্ধনের মাধ্যমে সমযোজী যৌগ যেমন SO2 H2O ইত্যাদি গঠিত হয়।
H পরমাণুর ইলেকট্রন বিন্যাস-
H(1) → Is1
দুটি H অধাতব মৌল/পরমাণু যখন কাছাকাছি আসে তখন উভয় পরমাণুই।টি করে e- শেয়ার করে নিকটস্থ নিষ্ক্রিয় মৌল He এর e- বিন্যাস অর্জন করে তথা স্থিতিশীলতা লাভ করে। ফলে (H-H) সমযোজী বন্ধনের সৃষ্টি হয়। যেমন-

H2O তে সমযোজী বন্ধন বিদ্যমান। কারণ: H2O-তে দুইটি হাইড্রোজেন পরমাণু একটি করে ইলেকট্রন অক্সিজেনের যোজ্যতা স্তরের দুইটি ইলেকট্রনের সাথে শেয়ার করে অক্সিজেন অষ্টক ও হাইড্রোজেন দুই এর নিয়ম বা বিন্যাস লাভ করে।
অক্সিজেনের পারমাণবিক সংখ্যা 8. সুতরাং এর ইলেকট্রন বিন্যাস দাঁড়ায় 2.6। অষ্টক পূরণের জন্য এর আরো দুইটি ইলেকট্রন দরকার। তাই অক্সিজেন অণু (০২) তে দুইটি অক্সিজেন পরমাণু পরস্পর ২টি করে ইলেকট্রন শেয়ার করে দুইটি সমযোজী বন্ধন গঠন করে এবং পরস্পর আবদ্ধ থাকে।
জানা আছে, দুটি অধাতব মৌল ইলেকট্রন শেয়ারের মাধ্যমে সমযোজী যৌগ গঠিত হয়। এখানে H2O যৌগটি গঠনে H ও O উভয়ই অধাতব মৌল ইলেকট্রন শেয়ার করেছে এবং স্থিতিশীলতা অর্জন করেছে। অর্থাৎ, সমযোজী বন্ধনের মাধ্যমে H2O সমযোজী যৌগ সৃষ্টি হয়েছে
দুটি সমযোজী অণু যখন খুবই নিকটবর্তী হয়, তখন তাদের মধ্যে এক ধরনের দুর্বল আকর্ষণ বল কাজ করে, এই আকর্ষণ বলকেই বলা হয় ভ্যানডার ওয়ালস আকর্ষণ বল। সমযোজী অণুগুলো পরস্পরের সাথে এই দুর্বল ভ্যানডার ওয়ালস আকর্ষণের মাধ্যমে যুক্ত থাকে।
কোনো পরমাণুর যোজ্যতান্তরের ইলেকট্রন জোড় যা বন্ধন গঠনে অংশগ্রহণ করে না, এদেরকে মুক্তজোড় ইলেকট্রন বলে। যেমন HCI যৌগ গঠনের সময় CI এর তিনজোড়া যোজ্যতা ইলেকট্রন বন্ধনে অংশগ্রহণ করে না। সুতরাং, HCI অণুতে তিনটি মুক্তজোড় ইলেকট্রন বিদ্যমান।
কোনো পরমাণুর যোজ্যতা স্তরের ইলেকট্রন যা বন্ধন গঠনে অংশগ্রহণ করে তাকে বন্ধনজোড় ইলেকট্রন বলে। যেমন HCI এর গঠনে ('। এর যোজ্যতা স্তরের একটি ইলেকট্রন এবং H এর একটি ইলেকট্রন মিলে HCI গঠিত হয়।
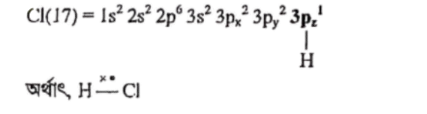
SO2 অণুর গঠন:
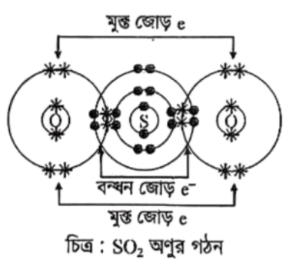
দেখা যাচ্ছে, SO2 অণুতে 4টি বন্ধন জোড় এবং 4টি মুক্তজোড় ইলেকট্রন বিদ্যমান। কারণ 4 জোড়া ইলেকট্রন 8 ও O শেয়ারের মাধ্যমে SO2গঠন করে যা বন্ধন জোড় ইলেকট্রন। এছাড়া দুটি O এ আরও 4 জোড়া ইলেকট্রন রয়েছে যা বন্ধনে অংশগ্রহণ করে নি। এগুলো মুক্তজোড় ইলেকট্রন।
কার্বন (C) ও ক্লোরিনের (CI) ইলেকট্রন বিন্যাস:
C(6)=1s2 2s1 2px1 2py12px1
Cl(17) = 1s2 2s2 2p6 3s23px23py² 3pz1
দেখা যায়, C এর সর্বশেষ স্তরে 4টি এবং CI এর। টি অযুগ্ম ইলেকট্রন আছে। CI পরমাণুর যোজ্যতা স্তরের অযুগ্ম ইলেকট্রনটি C এর সাথে বন্ধন গঠনে অংশগ্রহণ করলে যোজ্যতা স্তরে আরও তিনটি মুক্তজোড় ইলেকট্রন বিদ্যমান থাকে। তাই CCI4যৌগে চারটি CI পরমাণুর তিনটি করে মোট 12টি মুক্তজোড় ইলেকট্রন বিদ্যমান। কিন্তু C এর যোজ্যতা স্তরের সবগুলো ইলেকট্রন বন্ধন গঠনে অংশ নেয় বলে এতে কোনো মুক্তজোড় ইলেকট্রন নেই।

আয়নিক যৌগের ২টি বৈশিষ্ট্য নিম্নরূপ-
১. আয়নিক যৌগের গলনাঙ্ক ও স্ফুটনাঙ্ক অনেক বেশি হয়।
২. প্রায় সকল আয়নিক যৌগ পানিতে দ্রবীভূত হয় [ব্যতিক্রম: AgCl আয়নিক যৌগ পানিতে অদ্রবণীয়।]
সমযোজী যৌগের ২টি বৈশিষ্ট্য নিম্নরূপ-
১. অধিকাংশ সমযোজী যৌগ পানিতে দ্রবীভূত হয় না; ব্যতিক্রম H2O একটি পোলার সমযোজী যৌগ।
২. জলীয় দ্রবণে সমযোজী যৌগ বিদ্যুৎ পরিবহন করে না।
দ্রবণে আয়নিক যৌগ ধনাত্মক ও ঋণাত্মক আয়নে পরিণত হয়। এর ধনাত্মক আয়ন পানির ঋণাত্মক প্রান্তের সাথে আর ঋণাত্মক আয়ন পানির ধনাত্মক প্রান্তের সাথে যুক্ত হয়। এ কারণে আয়নিক যৌগ পানিতে দ্রবণীয় হয়।
আয়নিক যৌগের স্ফটিক ল্যাটিসে প্রতিটি আয়ন নির্দিষ্ট সংখ্যক বিপরীত চার্জযুক্ত আয়ন দ্বারা পরিবেষ্টিত থাকে। এ অবস্থায় বিপরীত চার্জযুক্ত আয়নসমূহ পরস্পরের সাথে স্থির বিদ্যুৎ আকর্ষণ শক্তি দ্বারা যুক্ত থাকার কারণে প্রতিটি আয়ন দৃঢ় সংঘবদ্ধভাবে থাকে। ফলে এদেরকে পরস্পর হতে বিচ্ছিন্ন করতে প্রচুর তাপশক্তির প্রয়োজন। তাই আয়নিক যৌগের গলনাংক ও স্ফুটনাংক উচ্চ।
KCI একটি আয়নিক যৌগ। সাধারণত সকল আয়নিক যৌগ পানিতে দ্রবণীয়। আয়নিক যৌগসমূহ পানির বিপরীত আয়ন দ্বারা আকর্ষিত হয়। ফলে KCI এর ল্যাটিস শক্তি পানির হাইড্রেশন' শক্তি - অপেক্ষা কম হয়। তাই KCI পানিতে দ্রবীভূত হয়।
ইথানল একটি পোলার যৌগ। এতে বিদ্যমান অক্সিজেনের তড়িৎ ঋণাত্মকতার মান অনেক বেশি হওয়ায় এটি পোলারিটি প্রদর্শন করে। অপরদিকে পানি একটি পোলার যৌগ হওয়ায় পোলার যৌগ ইথানল পোলার পানিতে দ্রবীভূত হয়।

HCI অণুস্থিত হাইড্রোজেন (2.1) ও ক্লোরিনের (3.O) তড়িৎ ঋণাত্মকতার পার্থক্য বেশি হওয়ায় CI বন্ধনজোড় ইলেকট্রনকে নিজের দিকে টেনে নেয়। ফলে H আংশিক ধনাত্মক ও CI আংশিক ঋণাত্মক চার্জে চার্জিত হয়। এভাবে সৃষ্ট আংশিক ধনাত্মক ও আংশিক ঋণাত্মক চার্জযুক্ত যৌগ পোলার যৌগ। এ কারণে HCI যৌগটি পোলার।
অধিকাংশ সমযোজী যৌগ পানিতে দ্রবীভূত না হলেও কিছু কিছু সমযোজী যৌগ যেমন- অ্যামোনিয়া (NH,), হাইড্রোক্লোরিক এসিড (HCI) পানিতে দ্রবণীয়। NH₁, HCI প্রভৃতি যৌগ পানির সাথে নিম্নোক্ত বিক্রিয়া করে এবং এদের মধ্যে হাইড্রোজেন বন্ধন থাকায় এরা পানিতে দ্রবীভূত হয়।
যে সমযোজী যৌগে পোলারিটির সৃষ্টি হয় তাকে পোলার যৌগ বলে। ফ্লরিনের তড়িৎঋণাত্মকতা হাইড্রোজেন অপেক্ষা বেশি। তাই H-F এ শেয়ারকৃত ইলেকট্রনযুগল F পরমাণুর দিকে বেশি আকৃষ্ট হয়। ফলে F পরযাণুতে আংশিক ঋণাত্মক প্রাপ্ত এবং H পরমাণুতে আংশিক ধনাত্মক প্রান্তের সৃষ্টি হয়। এ কারণে HF পোলার যৌগ।
পানির (H2O) অণুতে অক্সিজেনের অধিক তড়িৎ ঋণাত্মকতার কারণে বন্ধন জোড় ইলেকট্রনটি অক্সিজেনের দিকে সরে আসে। ফলে পানির অণুতে আংশিক ধনাত্মক ও আংশিক ঋণাত্মক প্রান্তের সৃষ্টি হয় বলে পানি একটি পোলার যৌগ।
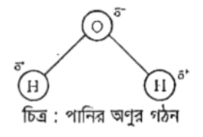
SiO2 একটি পলিমার যৌগ। (SiO2)n গঠনে একটি Si পরমাণু 4টি ০-পরমাণুর সাথে সমযোজী বন্ধনের মাধ্যমে যুক্ত হয়ে বিরাট দৈত্যকার অণু গঠন করে। তাই SiO2কঠিন। অপরদিকে, H2O যৌগে H ও এর মধ্যে তড়িৎঋণাত্মকতার পার্থক্যের কারণে H-পরমাণু আংশিক ধনাত্মক ও ()-পরমাণু আংশিক ঋণাত্মক চার্জ লাভকরে। পোলারিত H2O অণুসমূহ H-বন্ধনের মাধ্যমে যুক্ত হয়ে দীর্ঘ গুচ্ছ রচনা করে। তাই H2O তরল।
তড়িৎ পরিবহনের জন্য আয়নসমূহের চলাচল দরকার যা কঠিন অবস্থায় সম্ভব না। গলিত বা দ্রবীভূত অবস্থায় আয়নগুলো চলাচল করতে পারে। ফলে আয়নিক যৌগগুলো গলিত অবস্থায় তড়িৎ পরিবহন করে।
বিদ্যুৎ পরিবহনের পূর্বশর্ত হলো ইলেকট্রন প্রবাহ। CaCl2 একটি আয়নিক যৌগ। CaCl2জলীয় দ্রবণে Ca2 আয়ন এবং CI আয়ন উৎপন্ন করে। এই আয়নসমূহ জলীয় দ্রবণে মুক্তভাবে চলাচল করে এবং ইলেকট্রন বাহক হিসাবে কাজ করে। তাই CaCl2 গলিত অবস্থায় বিদ্যুৎ পরিবহন করে।
কঠিন অবস্থায় KCI অণু ত্রিমাত্রিকভাবে সুবিন্যস্ত হয়ে একটি স্ফটিক তৈরি করে। এ অবস্থায় ধনাত্মক (K') ও ঋণাত্মক (CI) আয়নে পরিণত হতে পারে না। জানা আছে, বিদ্যুৎ পরিবহনের জন্য ইলেকট্রনের আদান-প্রদান প্রয়োজন হয়। কিন্তু কঠিন KCI ইলেকট্রন স্থানান্তর করতে পারে না বলে বিদ্যুৎ পরিবহন করে না।
গ্রাফাইট হলো কার্বনের একটি রূপভেদ। কার্বন-কার্বন পরমাণু যখন গ্রাফাইট অণুর আকারে সজ্জিত হয় তখন তার তিনটি ইলেকট্রন সমযোজী বন্ধনে আবদ্ধ থাকে এবং অন্য ইলেকট্রনটি মুক্ত থাকে। এই মুক্ত ইলেকট্রনের মাধ্যমে বিদ্যুৎ পরিবাহিত হয়। তাই গ্রাফাইটকে ইলেকট্রনিক পরিবাহী বলা হয়।
বিদ্যুৎ পরিবহনের জন্য আয়নসমূহের চলাচল প্রয়োজন। সমযোজী বন্ধন বিশিষ্ট যৌগ গঠিত হয় ইলেকট্রন শেয়ারের মাধ্যমে। ফলে এতে কোনো আয়ন সৃষ্টি হয় না, পানিতে দ্রবীভূত করলেও আয়ন সৃষ্টি হয় না। ফলে সমযোজী যৌগসমূহ বিদ্যুৎ অপরিবাহী হয়।
সমযোজী যৌগের দ্রবণে আয়না না থাকলে তা কখনোই বিদ্যুৎ পরিবহন করতে পারে না। গ্লুকোজ (C6H12O6) একটি সমযোজী যৌগ। এটি দ্রবণে আয়ন আকারে বিভক্ত হয় না, কাজেই গ্লুকোজ দ্রবণে বিদ্যুৎ পরিবহন করতে পারবে না। অর্থাৎ গ্লুকোজ বিদ্যুৎ অপরিবাহী।
এক খণ্ড ধাতুর মধ্যে পরমাণুসমূহ যে আকর্ষণের মাধ্যমে যুক্ত থাকে, তাকেই বলা হয় ধাতব বন্ধন। উদাহরণস্বরূপ, Cu তার, লোহা (Fe) এর তৈরি ছুরি, কাঁচি, জানালার গ্রিল ইত্যাদির মধ্যে একই ধাতুর অসংখ্য পরমাণু পরস্পরের সাথে ধাতব বন্ধনের মাধ্যমে আবদ্ধ থাকে।
প্রত্যেক ধাতব পরমাণুর ইলেকট্রন বিন্যাসে সর্বশেষ শক্তিস্তরে সাধারণত ।টি, ২টি বা ওটি ইলেকট্রন থাকে এবং এদের আকার একই পর্যায়ের অধাতব পরমাণুর চেয়ে বড় হওয়ায় সর্ববহিঃস্থ স্তরের এই ইলেকট্রনের প্রতি নিউক্লিয়াসের আকর্ষণ অনেক কম হয়। ফলে এসব ধাতুসমূহ সর্ববহিঃস্থ স্তরের ইলেকট্রনগুলো ত্যাগ করে ধনাত্মক আয়নে পরিণত হয়। এই ধনাত্মক আয়নকেই বলা হয় পারমাণবিক শাঁস (Atomic Core)। ধাতব স্ফটিকে পারমাণবিক শাঁসগুলো সুনির্দিষ্ট ত্রিমাত্রিকভাবে বিন্যস্ত থাকে।
ধাতব পরমাণু কর্তৃক ত্যাগকৃত ইলেকট্রনগুলো পারমাণবিক শাসের মধ্যবর্তী স্থানে মুক্তভাবে ঘোরাফেরা করে; এই ধরনের ইলেকট্রনকে সঞ্চরণশীল ইলেকট্রন (Délocalized Electron) বলে। এই ইলেকট্রনগুলো কোনো নির্দিষ্ট পরমাণুর অধীনে থাকে না, পুরো ধাতব খণ্ডের সবগুলো ধাতব আয়নের ইলেকট্রন হয়ে যায়।
সকল ধাতুই বিদ্যুৎ সুপরিবাহী। কারণ ধাতুর স্ফটিকে মুক্তভাবে বিচরণশীল ইলেকট্রনগুলো বিদ্যুৎ পরিবহনের কাজটি করে থাকে। ধাতব খণ্ডের দুই প্রান্তের সাথে ব্যাটারির ধনাত্মক (+) ও ঋণাত্মক (-) প্রান্ত সংযুক্ত করা হলে ইলেকট্রন (e-) গুলো ঋণাত্মক প্রান্ত হতে ধনাত্মক দিকে প্রবাহিত হবে। অর্থাৎ ধনাত্মক প্রান্ত হতে ঋণাত্মক প্রান্তের দিকে বিদ্যুৎ প্রবাহিত হবে। এই সঞ্চারণশীল ইলেকট্রনের (e-) জন্যই মূলত ধাতুর মধ্যে বিদ্যুৎ প্রবাহিত হয়।
Na (11)→ 1s22s22p6 3s1
ইলেকট্রন বিন্যাস থেকে দেখা যায়, Na ধাতুর সর্ববহিঃস্থ স্তরে। টি অযুগ্ম ইলেকট্রন রয়েছে, যা ত্যাগ করে আয়নে, পরিণত হয়। এই ত্যাগকৃত ইলেকট্রনই ধাতব স্ফটিকে মুক্তভাবে বিচরণ করে। এই মুক্ত - ইলেকট্রনই মূলত বিদ্যুৎ পরিবহনের জন্য দায়ী। সঞ্চারণশীল এই ইলেকট্রন না থাকলে Na বিদ্যুৎ সুপরিবাহী হত না। অর্থাৎ স্যারণশীল ইলেকট্রন থাকায় Na ধাতু বিদ্যুৎ সুপরিবাহী।
ধাতব স্ফটিকে পারমাণবিক শাঁসগুলো, সুনির্দিষ্ট ত্রিমাত্রিকভাবে বিন্যস্ত থাকে। আর ধাতব পরমাণু কর্তৃক ত্যাগকৃত ইলেকট্রনগুলো উক্ত পারমাণবিক শাঁসের মধ্যবর্তী স্থানে মুক্তভাবে ঘোরাফেরা করে। এই ধরনের ইলেকট্রনকে সঞ্চারণশীল ইলেকট্রন বলে। এই ইলেকট্রনগুলো কোনে। নির্দিস্ট পরমাণুর অধীনে না থেকে পুরো ধাতব খণ্ডের সবগুলো ধাতব আয়নের ইলেকট্রন হয়ে যায়। ধাতব স্ফটিকে দুটো ধাতব আয়নের মধ্যবর্তী স্থানে যখন একটি সঞ্চারণশীল ইলেকট্রন অবস্থান করে তখন ইলেকট্রনের প্রতি উভয় ধাতব আয়নই স্পির বৈদ্যুতিক আকর্ষণে আকর্ষিত হয়। এ কারণে ধাতব আয়ন দুটি পরস্পর থেকে বিচ্ছিন্ন হতে পারে না। এটিই মূলত ধাতব বন্ধনের মূল কারণ।
Al (1s2 2s22p63s13px1 3py1)এর সর্ববহিঃস্থ স্তরে 3টি অযুগ্ম ইলেকট্রন থাকে, যা ত্যাগ করে আয়নে পরিণত হয়। এই ত্যাগকৃত ইলেকট্রনই ধাতব স্ফটিকে মুক্তভাবে বিচরণ করে। এই ইলেকট্রনগুলোই মূলত বিদ্যুৎ পরিবহনের জন্য দায়ী। সঞ্চারণশীল এই ইলেকট্রন না থাকলে অ্যালুমিনিয়াম বিদ্যুৎ সুপরিবাহী হত না। অর্থাৎ সঞ্চারণশীল ইলেকট্রন থাকায় অ্যালুমিনিয়াম বিদ্যুৎ সুপরিবাহী
ধাতুসমূহের তাপ পরিবাহিতার কারণ সঞ্চারণশীল ইলেকট্রন। তাপ প্রদানের সাথে সাথে সঞ্চরণশীল ইলেকট্রনগুলো শক্তি গ্রহণ করে, ফলে এদের গতিবেগ বেড়ে যায়; অধিক তাপমাত্রার প্রান্ত থেকে ইলেকট্রনগুলো কম তাপমাত্রার প্রান্তের দিকে স্থানান্তরিত হয়। ফলে ধাতুতে একপ্রান্ত থেকে অপরপ্রান্তে তাপের পরিবহন ঘটে।
কোনো মৌলের ইলেকট্রন বিন্যাসে সর্বশেষ কক্ষপথে যে ইলেকট্রন বা ইলেকট্রনসমূহ থাকে তার সংখ্যাকে যোজ্যতা ইলেকট্রন বলে।
কোনো মৌলের সর্বোচ্চ যোজনী ও সক্রিয় যোজনীর পার্থক্যকে সুপ্ত যোজনী বলে।
অণু গঠনকালে কোনো মৌলের একটি পরমাণুর সাথে অপর একটি মৌলের পরমাণু যুক্ত হওয়ার ক্ষমতাকে যোজনী বা যোজ্যতা বলা হয়।
একাধিক মৌলের কতিপয় পরমাণু বা আয়ন পরস্পরের সাথে মিলিত হয়ে ধনাত্মক বা ঋণাত্মক আধানবিশিষ্ট একটি পরমাণুগুচ্ছ তৈরি করে এবং এটি একটি মৌলের আয়নের ন্যায় আচরণ করে; এ ধরনের পরমাণুগুচ্ছকে যৌগমূলক বলে।
ম্যাগনেশিয়ার সংকেত MgO এবং অ্যালুমিনার সংকেত Al2O3 ।
তুঁতের সংকেত হলো CuSO4.5H2O ।
ফসফরাস (P) অণুতে চারটি (P4 ) পরমাণু বিদ্যমান।
অণু গঠনকালে কোনো মৌল ইলেকট্রন গ্রহণ, বর্জন অথবা শেয়ারের মাধ্যমে তার সর্বশেষ শক্তিস্তরে ৪টি (৮) করে e- ধারণের মাধ্যমে নিকটস্থ নিষ্ক্রিয় গ্যাসের ইলেকট্রন বিন্যাস লাভ করাকে অষ্টক নিয়ম বলা হয়।
অণু গঠনে কোনো পরমাণুর সর্বশেষ শক্তিস্তরে এক বা একাধিক জোড়া. ইলেকট্রন বিদ্যমান থাকবে এটি হচ্ছে 'দুই' এর নিয়ম।
অণুতে পরমাণুসমূহ যে আকর্ষণের মাধ্যমে একে অপরের সাথে যুক্ত থাকে তাকেই রাসায়নিক বন্ধন বলে।
অণুতে পরমাণুসমূহ যে আকর্ষণের মাধ্যমে একে অপরের সাথে যুক্ত থাকে তাকেই রাসায়নিক বন্ধন বলে।
খঋণাড়াক চার্জযুক্ত পরমাণুকে অ্যানায়ন বলে।
ধনাত্মক চার্জযুক্ত পরমাণুকে ক্যাটায়ন বলে।
রাসায়নিক বিক্রিয়ার সময় যেসব পরমাণু বা পরমাণুগুচ্ছ (মূলক) এক বা একাধিক ইলেকট্রন গ্রহণ বা বর্জনের মাধ্যমে ঋণাত্মক বা ধনাত্মক চার্জগ্রস্ত হয়, তাদেরকে আয়ন বলা হয়।
ইলেকট্রন আদান-প্রদানের মাধ্যমে গঠিত ক্যাটায়ন ও
অ্যানায়নসমূহ যে আকর্ষণ বল দ্বারা যৌগের অণুতে আবদ্ধ থাকে তাকে আয়নিক বন্ধন বলে
NaCl যৌগ আয়নিক বন্ধন গঠন করে।
ধাতু-অধাতু মিলে সাধারণত আয়নিক বন্ধন গঠন করে।
বহিঃস্থ স্তরে ইলেকট্রনের শেয়ারের মাধ্যমে যে বন্ধন গঠিত হয় তাকে সমযোজী বন্ধন বলে।
কোনো পরমাণুর যোজ্যতা স্তরের যে ইলেকট্রনগুলো বন্ধন গঠনে অংশগ্রহণ করে না তাদেরকে মুক্ত জোড় ইলেকট্রন বলে।
H2O অণুর আকৃতি কৌণিক।
দুটি সমযোজী অণু যখন খুবই নিকটবর্তী হয় তখন তাদের মধ্যে এক ধরনের দুর্বল আকর্ষণ বল কাজ করে; এই আকর্ষণ বলকেই ড্যানডার ওয়ালস আকর্ষণ বল বলে।
ইলেকট্রন শেয়ারের মাধ্যমে সমযোজী বন্ধন গঠিত হয়।
CO2 অণুর আকৃতি সরল রৈখিক।
মিথেন (CH4) অণুর আকৃতি চতুস্তলকীয়।
পানির অণুতে ২ (দুই) টি মুক্ত জোড় ইলেকট্রন আছে।
অ্যামোনিয়ার অণুর আকৃতি ত্রিকোণীয় পিরামিড।
যেসব যৌগে ইলেকট্রন শেয়ারের মাধ্যমে কন্ধন তথা সমযোজী কখন গঠিত হয়, সেই যৌগকে সমযোজী যৌগ বলে।
সমযোজী যৌগের অণুতে বন্ধনে আবদ্ধ পরমাণুগুলোর তড়িৎ ঋণাত্মকতার পার্থক্যের কারণে অণুতে আংশিক ধনাত্মক ও আংশিক ঋণাত্মক চার্জবিশিস্ট প্রান্তের সৃষ্টি হয়। এই ঘটনাকে বলা হয় পোলারিটি।
যেসব যৌগ দ্রাবকে দ্রবীভূত অবস্থায় ধনাত্মক ও ঋণাত্মক আয়নে বিযোজিত হয়, তারা পোলার যৌগ।
ধনাত্মক ও ঋণাত্মক আয়ন পরস্পর আকর্ষণের ফলে যে বঃধনের সৃষ্টি হয়, তাকে আয়নিক বন্ধন বলে এবং আয়নিক বন্ধন দ্বারা গঠিত যৌগসমূহকে আয়নিক যৌগ বলে.।
যেসব কঠিন পদার্থে অণু, পরমাণু বা আয়নগুলো নিয়মিত সুশৃঙ্খল উপায়ে ত্রিমাত্রিক গঠনে বিন্যস্ত থেকে জ্যামিতিক আকৃতি গঠন করে তাদেরকে কেলাসাকার পদার্থ বলে।
একখণ্ড ধাতুর মধ্যে পরমাণুসমূহ যে আকর্ষণের মাধ্যমে যুক্ত থাকে তাকেই ধাতব বন্ধন বলে।
ধাতব পরমাণু কর্তৃক ত্যাগকৃত ইলেকট্রনগুলো পারমাণবিক শাঁসের মধ্যবর্তী স্থানে মুক্তভাবে ঘোরাফেরা করলে সেই ইলেকট্রনকে সঞ্চরণশীল ইলেকট্রন বলে।
ধাতুতে পরমাণুসমূহ তার সর্বশেষ শক্তিস্তরের এক বা একাধিক ইলেকট্রনকে ত্যাগ করে ধনাত্মক আয়নে পরিণত হয়; এই ধনাত্মক আয়নকে পারমাণবিক শাঁস বলা হয়।
ধাতব খণ্ডে তড়িৎ পরিবাহিতার জন্য দায়ী হচ্ছে সঞ্চরণশীল ইলেকট্রন।
কোনো মৌলের সর্বশেষ প্রধান শক্তিস্তরের মোট ইলেকট্রন সংখ্যাকে সেই মৌলের যোজ্যতা ইলেকট্রন বলে। যেমন- Na (11) = 1s2 2s2 2p2 3s1। সর্বশেষ প্রধান শক্তিস্তরে ইলেকট্রন সংখ্যা ।টি। সুতরাং এর যোজ্যতা ইলেকট্রন এক। আবার, কোনো মৌলের ইলেকট্রন বিন্যাসে সর্বশেষ কক্ষপথে যত সংখ্যক ইলেকট্রন থাকে অথবা যত সংখ্যক বিজোড় ইলেকট্রন থাকে তাকে যোজনী বলে। যেমন- Mg (12) = 1s22s2 2p6 3s2। সর্বশেষ স্তরে 2টি ইলেকট্রন থাকায় Mg এর যোজনী 2 ।
জানা আছে, ধাতব মৌলের সর্ববহিঃস্থ শেলে অরবিটালে যে কয়টা e- থাকে, সেটা হচ্ছে যোজনী। 12Mg এর ইলেকট্রন বিন্যাস নিয়ে পাই- Mg(12) 1s2 2s2 2p6 3s2 উক্ত ইলেকট্রন বিন্যাস থেকে দেখা যায়, Mg এর. সর্ববহিঃস্থ শেলে 2টা e- আছে। তাই Mg এর যোজনী 2। অন্যভাবে বলা যায়, নিকটস্থ নিষ্ক্রিয় গ্যাসের ইলেকট্রনীয় কাঠামো অর্জন করতে প্রয়োজনীয় e- সংখ্যাই হচ্ছে যোজনী। এক্ষেত্রে Mg এর নিকটস্থ নিষ্ক্রিয় মৌল Ne এর নিষ্ক্রিয় চরিত্র অর্জন করতে ২টা e- ত্যাগ করতে হয়। তাই Mg এর যোজনী 2 ।
কোনো পরমাণু তার যোজ্যতী স্তর থেকে যতটি ইলেকট্রন দান করে অথবা যতটি ইলেকট্রন গ্রহণ করে অষ্টক পূর্ণ করে সেটি হলো ঐ মৌলের যোজনী। Na(11) ও CI(17) এর ইলেকট্রন বিন্যাস:
Na(11) = 1s22s22p63s1
Cl(17) 1s22s22p63s23p5
দেখা যাচ্ছে, Na পরমাণুর যোজ্যতা স্তরে 1টি মাত্র ইলেকট্রন থাকায় এটি। টি ইলেকট্রন দান করে অষ্টক পূর্ণতা অর্জন করে এবং Na আয়নে পরিণত হয়। এজন্য Na এর যোজনী।। অপরদিকে CI পরমাণুর যোজ্যতা স্তরে 7টি ইলেকট্রন আছে। অর্থাৎ অস্টক পূর্ণ অপেক্ষা। টি ইলেকট্রন কম আছে। তাই এটি। টি ইলেকট্রন গ্রহণ করে CI আয়নে পরিণত হয়। এজন্য CI এর যোজনী। অর্থাৎ 11Na ও 17Cl এর যোজনী একই।
ফ্লোরিনের যোজনী ও যৌজনী ইলেকট্রন ভিন্ন। কারণ আমরা জানি কোনো অধাতব মৌলের যোজ্যতা স্তরের বিজোড় ইলেকট্রনকে তার যোজনী বলে এবং সর্বশেষ শক্তিস্তরের ইলেকট্রনকে যোজনী ইলেকট্রন বলে। F এর ইলেকট্রন বিন্যাস- F(9)= 1s² 2s22px 2p2 y2px1
ইলেকট্রন বিন্যাস থেকে দেখা যায়, মৌলটির যোজ্যতাস্তরে বিজোড় ইলেকট্রন সংখ্যা। হওয়ায় যোজনী । এবং যোজ্যতা স্তরে মোট ইলেকট্রন সংখ্যা ? হওয়ায় যোজনী ইলেকট্রন 7 হয়।
কোনো অধাতব মৌলের সর্বশেষ কক্ষপথে বিজোড় ইলেকট্রন সংখ্যাকে ঐ মৌলের যোজনী বলে। অক্সিজেনের ইলেকট্রন বিন্যাস নিয়ে পাই-

অক্সিজেন হলো একটি অধাতু এবং এর শেষ কক্ষপথে বিজোড় ইলেকট্রন সংখ্যা 2। সুতরাং অক্সিজেনের যোজনী 2। আবার, কোনো মৌলের সর্বশেষ প্রধান শক্তিস্তরের মোট ইলেকট্রন সংখ্যাকে সেই মৌলের যোজ্যতা ইলেকট্রন বলে। ইলেকট্রন বিন্যাস, হতে দেখা যায় যে, অক্সিজেনের সর্বশেষ প্রধান শক্তিস্তরে ইলেকট্রন সংখ্যা হলো (2+4) = 6টি। অর্থাৎ যোজ্যতা ইলেকট্রন 6।
সুতরাং অক্সিজেনের যোজনী ও যোজনী ইলেকট্রন যথাক্রমে 2 ও 6, যা সমান নয়।
N এর ইলেকট্রন বিন্যাস হচ্ছে,
N(7): 1s2 2s2 2px1, 2py1, 2pz1
N এর বহিঃস্থ স্তরে ৩টি অযুগ্ম ইলেকট্রন রয়েছে।
ফলে নাইট্রোজেন মৌলটি একযোজী কোনো মৌলের তিনটি পরমাণুর সাথে যুক্ত হওয়ার ক্ষমতা রাখে। সংজ্ঞানুসারে, নাইট্রোজেনের যোজনী তিন। অপরদিকে নাইট্রোজেনের সর্বশেষ শক্তিস্তরে মোট ১টি ইলেকট্রন থাকায় এর যোজ্যতা ইলেকট্রন 5। সুতরাং, দেখা যাচ্ছে, N এর যোজনী ও এবং যোজ্যতা ইলেকট্রন 5, যা ভিন্ন।
ফসফরাসের ইলেকট্রন বিন্যাস-
P(15) = 1s2 2s2 2p6 3s2 3px1 3py1, 3px1
ফসফরাস একটি অধাতু এবং এর শেষ কক্ষপথে বিজোড় ইলেকট্রন সংখ্যা ও। সুতরাং P এর যোজ্যতা 3। আবার কোনো মৌলের সর্বশেষ প্রধান শক্তিস্তরে মোট ইলেকট্রন সংখ্যাকে সেই মৌলের যোজ্যতা ইলেকট্রন বলে। P এর ইলেকট্রন বিন্যাস থেকে দেখা যায়, এর সর্বশেষ প্রধান শক্তিস্তরে ৩টি ইলেকট্রন আছে। তাই P এর যোজ্যতা ইলেকট্রন 5। সুতরাং দেখা যাচ্ছে, ফসফরাসের যোজ্যতা ও যোজ্যতা ইলেকট্রন একই নয়।
কার্বনের যোজ্যতা ও যোজ্যতা ইলেকট্রন একই। কারণ কোনো মৌলের যোজ্যতা স্তরের মোট ইলেকট্রন সংখ্যাকে তার যোজ্যতা ইলেকট্রন বলে। যেমন-
কার্বনের ইলেকট্রন বিন্যাস: C(6) = 1s2 2s2 2p6
দেখা যাচ্ছে, C এর যোজ্যতাস্তরে 4টি ইলেকট্রন আছে। তাই কার্বনের যোজ্যতা ইলেকট্রন 4। আবার, কার্বন অধাতু হওয়ায় কার্বনের যোজ্যতা স্তরের বিজোড় e- কে যোজ্যতা বলে।
C(6) = 1s2 2s2 2px1, 2py1, 2pz1
কার্বনের যোজ্যতান্তরে 4 টি বিজোড় ইলেকট্রন থাকায় কার্বনের যোজ্যতাও 4।। এ কারণে কার্বনের যোজ্যতা ও যোজ্যতা ইলেকট্রন 4-তথা একই।
Mg এর e- বিন্যাস নিয়ে পাই,
Mg(12) 1s2 2s2 2p6 3s2
দেখা যাচ্ছে, Mg এর সর্ববহিঃস্থ শক্তিস্তরে মাত্র ২টি e- রয়েছে। জানা আছে, কোনো মৌলের ইলেকট্রন বিন্যাস সর্বশেষ কক্ষপথে য়ে ইলেকট্রন বা ইলেকট্রনসমূহ থাকে তার সংখ্যাকে যোজ্যতা ইলেকট্রন বলে। যেহেতু Mg এর e- বিন্যাসে সর্ববহিঃস্থ শক্তিস্তরে ২টি e- আছে। তাই এর যোজ্যতা ইলেকট্রন 2। আবার Mg এর বহিঃস্থ স্তরের e- ২টি ত্যাগ করে নিকটস্থ নিষ্ক্রিয় চরিত্র অর্জন করে ক্যাটায়নে পরিণত হয়ে যৌগ গঠন করে। তাই Mg এর যোজনীও 2।
সুতরাং বলা যায়, Mg এর যোজ্যা ইলেকট্রন ও যোজনী উভয়ই 2 অর্থাৎ একই।
কোনো অধাতব মৌলের যোজ্যতা স্তরের বিজোড় ইলেকট্রনকে তার যোজ্যতা বা যোজনী বলে। কার্বনের ইলেকট্রন বিন্যাস:
C(6) = 1s2 2s2 2px1, 2py1, 2pz0
যোজ্যতা স্তরে 2টি বিজোড় ইলেকট্রন থাকায় যোজ্যতা 2। কিন্তু উত্তেজিত অবস্থায় এর ইলেকট্রন বিন্যাস:
C(6) = 1s2 2s2 2px1, 2py1, 2pz1
যোজ্যতা স্তরে 4টি বিজোড় ইলেকট্রন থাকায় যোজ্যতা 4। অর্থাৎ কার্বন একাধিক যোজ্যতা প্রদর্শন করে।
অধাতব মৌলের যোজ্যতা স্তরের বিজোড় ইলেকট্রন সংখ্যাকে ঐ মৌলের যোজনী বলে। সালফার পরিবর্তনশীল' যোজনী প্রদর্শন করে। সালফার এর স্বাভাবিক ও উত্তেজিত অবস্থায় ইলেকট্রন বিন্যাস নিম্নরূপ-
S(16) = 1s2 2s2 2p6 3s2 3px1 3py1, 3px1 যোজনী 2
*S(16)= 1s2 2s2 2p6 3s2 3px1 3py1, 3px 3dxy1 যোজনী 4
*S(16) = 1s2 2s2 2p6 3s2 3px1 3py1, 3px 3dxy1 3dyz 1 যোজনী 6
স্বাভাবিক অবস্থায় সালফারের যোজনী-2 হলেও উত্তেজিত অবস্থায় যোজনী 4, 6 হয়। যে মৌলের একাধিক যোজনী বিদ্যমান সে মৌল পরিবর্তনশীল যোজনী প্রদর্শন করে। এজন্য সালফার পরিবর্তনশীল যোজনী আছে।
কোনো মৌলের সর্বোচ্চ যোজনী ও সক্রিয় যোজনীর পার্থক্যকে ঐ মৌলের সুপ্ত যোজনী বলে। CO যৌগে কার্বন (C) এর সক্রিয় যোজনী 2। কিন্তু C এর সর্বোচ্চ যোজনী 4 ।
সুতরাং, CO যৌগে কার্বনের সুপ্ত যোজনী = 4-2=2 ।
যোজনী ও জারণ সংখ্যা এক নয়, এর কারণ নিচে ব্যাখ্যা করা হলো:
(i) কোনো মৌলের যোজনী হলো অপর মৌলের সাথে যুক্ত হওয়ার ক্ষমতা। যোজনীর কোনো ধনাত্মকতা বা ঋণাত্মকতা নেই। অপরদিকে কোনো যৌগে কোনো মৌলের জারণ সংখ্যা বলতে এমন একটি সংখ্যাকে বোঝায়, যা দ্বারা সংশ্লিষ্ট পরমাণুতে সৃষ্ট চার্জের প্রকৃতি ও সংখ্যামান উভয়ই প্রকাশ পায়। জারণ সংখ্যা ধনাত্মক ও ঋণাত্মক বা শূন্য হতে পারে।
ii) মৌলের যোজনী সব সময় পূর্ণসংখ্যা। কিন্তু জারণ সংখ্যা ভগ্নাংশ হতে পারে।
সুতরাং, বলা যায়, জারণ সংখ্যা ও যোজনী একই বিষয় নয়।
দস্তার (Zn) যোজনী ও যোজ্যতা ইলেকট্রন সমান হবে। কারণ Zn এর ইলেকট্রন বিন্যাস-
Zn(30) = 1s2 2s2 2p6 3s2 3p6 3d10 4s2
Zn এর যোজ্যতা স্তরে ২টি ইলেকট্রন আছে। এজন্য Zin এর যোজ্যতা ইলেকট্রন 2। আবার Zin ধাতু হওয়ায় এর যোজ্যতা স্তরের মোট ইলেকট্রনই হচ্ছে এর যোজনী। এজন্য Zn এর যোজনী ও যোজ্যতা ইলেকট্রন সমান।
আয়নের ইলেকট্রন বিন্যাস:
F(26) = 1s2 2s2 2p6 3s2 3p6 3d6 4s2
যোজ্যতা স্তরে 2টি ইলেকট্রন থাকায় এটি ২টি ইলেকট্রন ত্যাগ করে Fe2+ আয়নে পরিণত পরিণত হতে পারে। এজন্য Fe এর যোজনী 2 হয়।
Fe2+(26) = 1s2 2s2 2p6 3s2 3p6 3d6 4s2
আবার, Fe2+ আয়নের 3d অরবিটালে 6টি ইলেকট্রন থাকায় সুস্থিতির জন্য। টি ইলেকট্রন ত্যাগ করে Fe3+ আয়নে পরিণত হতে পারে। এজন্য Fe এর যোজনী 3।
Fe3+(26) = 1s2 2s2 2p6 3s2 3p6 3d54s0
সুতরাং, আয়রন (Fe) 2 ও ও যোজনী অর্থাৎ পরিবর্তনশীল যোজনী প্রদর্শন করে।
একটি যৌগমূলক। কারণ আয়নটি একাধিক পরমাণু (P ও H) সমন্বয়ে গঠিত মূলক, যা রাসায়নিক বিক্রিয়ায় একটি মাত্র পরমাণুর ন্যায় আচরণ করে এবং বিক্রিয়া শেষে অপরিবর্তিত থাকে। যেমন-

নাইট্রেট (N(),) একটি যৌগমূলক। কারণ NO, আয়নটি ঋণাত্মক আধানবিশিষ্ট, যা একাধিক পরমাণু সমন্বয়ে গঠিত। রাসায়নিক বিক্রিয়ায় এটি একটি মাত্র পরমাণুর ন্যায় আচরণ করে এবং বিক্রিয়া শেষে অপরিবর্তিত থাকে। যেমন Zn+2HNO3 → Zn(NO3)2 + H2(g)
কে যৌগমূলক বলা হয়। কারণ মূলকটি ।টি C পরমাণু ও 3টি () পরমাণুর সমন্বয়ে গঠিত, যা একটি মাত্র পরমাণুর ন্যায় আচরণ করে এবং বিক্রিয়া শেষে অপরিবর্তিত থাকে।
কে যৌগমূলক বলা হয়। কারণ মূলকটি একাধিক পরমাণুর সমন্বয়ে গঠিত, রাসায়নিক বিক্রিয়ায় একটিমাত্র পরমাণুর ন্যায় আচরণ করে এবং বিক্রিয়া শেষে অপরিবর্তিত থাকে। যেমন-
Zn + H2SO4→ ZnSO4 + H2(g)
বিক্রিয়া থেকে দেখা যায়, বিক্রিয়ক ও উৎপাদে এর কোনো পরিবর্তন হয়নি। সুতরাং একটি যৌগমূলক।
আর্গন (Ar) নিষ্ক্রিয় গ্যাস। কারণ 18Ar এর (1s2 2s2 2p6 3s2 3p6) সর্ববহিঃস্থ স্তরে ইলেকট্রন দ্বারা অষ্টকপূর্ণ থাকে যা অত্যন্ত সুস্থিত। এ সুস্থিত ইলেকট্রন বিন্যাস ভাঙতে অনেক শক্তির প্রয়োজন। তাই Ar স্বাভাবিক অবস্থায় কোনো মৌলের সাথে যুক্ত হয় না। অর্থাৎ বহিঃস্থ স্তরের সুবিন্যস্ত ইলেকট্রন বিন্যাসের কারণে Ar নিষ্ক্রিয় হয়।
Mg2+ হলো ম্যাগনেসিয়ামের দ্বিধনাত্মক আয়ন'।
Mg এর ইলেকট্রন বিন্যাস নিম্নরূপ: Mg(12) =Is22s2 2p63s2
ম্যাগনেসিয়াম (Mg) পরমাণুর শেষ শক্তিস্তরে 2টি ইলেকট্রন বিদ্যমান থাকায় এটি সহজেই উক্ত ইলেকট্রন দুটি ত্যাগ করে নিষ্ক্রিয় গ্যাস Ne এর ইলেকট্রন বিন্যাস অর্জন করে এবং Mg2+ তড়িৎ ধনাত্মক আয়ন গঠন করে। যেমন- Mg-2e -→ Mg2+
সাধারণত Na2+ আয়ন গঠন অসম্ভব। কারণ Na+আয়নের ইলেকট্রন বিন্যাস, Na+(11) = 1s2 2s22p6
ইলেকট্রন বিন্যাস অনুসারে, Na+আয়নের যোজ্যতা স্তরে 8 টি - ইলেকট্রন থাকায় এটি সুস্থিত। এখান থেকে ।টি ইলেকট্রন ত্যাগ - করতে অনেক শক্তির প্রয়োজন বলে Na2+ গঠন অসম্ভব।
ক্যাটায়ন ও অ্যানায়নের মধ্যে পার্থক্য নিম্নরূপ-
| ক্যাটায়ন | অ্যানায়ন |
| ১. ধনাত্মক চার্জযুক্ত পরমাণুসমূহকে ক্যাটায়ন বলে। | ১. ঋণাত্মক চার্জযুক্ত পরমাণুসমূহকে অ্যানায়ন বলে। |
| ২. ক্যাটায়নে ইলেকট্রনের চেয়ে প্রোটনের সংখ্যা বেশি থাকে। | ২. অ্যানায়নে প্রোটনের চেয়ে ইলেকট্রনের সংখ্যা বেশি থাকে। |
| ৩. ক্যাটায়নের উদাহরণ: Ca2+, Mg2+, NH4' ইত্যাদি। | ৩. অ্যানায়নের উদাহরণ: O2- OH-, CI-, F- ইত্যাদি। |
পটাশিয়াম (K) ইলেকট্রন বিন্যাস হলো-
K(19) → 1s2 2s2 2p6 3s2 3p6 4s1
K পরমাণুর সর্ববহিঃস্থ কক্ষপথে । টি ইলেকট্রন থাকায় ইলেকট্রন শেয়ার বা গ্রহণের মাধ্যমে অষ্টকপূর্ণ করতে পারে না। কিন্তু Mg পরমাণুর সর্ববহিঃস্থ কক্ষপথের 1টি ইলেকট্রন সহজেই ত্যাগ করে অষ্টক পূর্ণ করতে পারে। তাই K কেবল আয়নিক বন্ধনের মাধ্যমে আয়নিক যৌগ গঠন করতে পারে।
Mg পরমাণুর ইলেকট্রন বিন্যাস-
Mg(12) 1s2 2s2 2p6 3s2
Mg পরমাণুর সর্বশেষ শক্তিস্তরে 2টি মাত্র ইলেকট্রন থাকায় এটি সহজেই ২টি ইলেকট্রন দান করে নিকটতম নিষ্ক্রিয় গ্যাস নিয়নের কাঠামো অর্জন করে। যেহেতু ২টি ইলেকট্রন দান করে সেহেতু এটি অধাতুর সাথে যুক্ত হয়ে আয়নিক বন্ধন গঠন করে। ইলেকট্রন শেয়ারের মাধ্যমে সমযোজী বন্ধন গঠন করতে পারে না।
CO2 এর গঠন নিম্নরূপ-
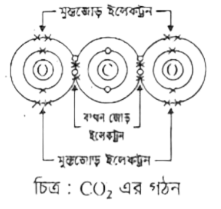
দেখা যাচ্ছে যে, CO2অণুতে 4টি বন্ধন জোড় এবং 4টি মুক্তজোড় ইলেকট্রন বিদ্যমান। কারণ 4 জোড়া ইলেকট্রন C ও O শেয়ারের মাধ্যমে CO2 গঠন করে, যা বন্ধন জোড় ইলেকট্রন। এছাড়া দুটি () এ আরও 4 জোড়া ইলেকট্রন রয়েছে যা বন্ধনে অংশগ্রহণ করে নি, যা মুক্ত জোড় ইলেকট্রন।
গ্লুকোজ (C6H12O6) এর জলীয় দ্রবণ বিদ্যুৎ পরিবহন করে না। কারণ জলীয় দ্রবণে গ্লুকোজ আয়নিত হয়ে ক্যাটায়ন বা অ্যানায়ন সৃষ্টি করতে পারে না। ফলে ইলেকট্রন পরিবহন ঘটে না বলে গ্লুকোজের জলীয় দ্রবণ বিদ্যুৎ পরিবহন করে না।
হাইড্রোজেন ও ক্লোরিন এর মধ্যে সমযোজী বন্ধনের মাধ্যমে হাইড্রোজেন ক্লোরাইড (HCI) গঠিত হয়। সাধারণত সমযোজী যৌগ অপোলার হয়। কিন্তু হাইড্রোজেন (2.1) ও ক্লোরিনের (3.0) তড়িৎ ঋণাত্মকতার পার্থক্য বেশি হওয়ায় ক্লোরিন বন্ধনজোড় ইলেকট্রনকে নিজের দিকে টেনে নেয়। ফলে হাইড্রোজেন আংশিক ধনাত্মক ও ক্লোরিন আংশিক ঋণাত্মক চার্জে চার্জিত হয়। এভাবে সৃষ্ট আংশিক ধনাত্মক ও আংশিক ঋণাত্মক চার্জযুক্ত যৌগ পোলার যৌগ। এ কারণে HCI যৌগটি পোলার।
যে সমযোজী যৌগে পোলারিটির সৃষ্টি হয় তাকে পোলার যৌগ বলে। ফ্লুরিনের তড়িৎঋণাত্মকতা হাইড্রোজেন অপেক্ষা বেশি। তাই H-F এ শেয়ারকৃত ইলেকট্রনযুগল F পরমাণুর দিকে বেশি আকৃষ্ট হয়। ফলে পরমাণুতে আংশিক ঋণাত্মক প্রাপ্ত এবং H পরমাণুতে আংশিক ধনাত্মক প্রান্তের সৃষ্টি হয়। এ কারণে HF পোলার যৌগ।
বিশুদ্ধ হাইড্রোক্লোরিক এসিড তড়িৎ পরিবাহী নয়। কারণ কোনো যৌগকে তড়িৎ পরিবাহী হতে হলে অবশ্যই ক্যাটায়ন ও অ্যানায়ন উৎপন্ন করতে হবে। কিন্তু বিশুদ্ধ অবস্থায় HCI আণবিক অবস্থায় থাকে। HCI এর হাইড্রোজেন পরমাণু বিয়োজিত হয়ে H' আয়ন উৎপন্ন করতে পারে না. বলে বিশুদ্ধ হাইড্রোক্লোরিক এসিড তড়িৎ পরিবাহী নয়।
KF কঠিন অবস্থায় বিদ্যুৎ পরিবহন করে না। কারণ কঠিন অবস্থায় KF অণু ত্রিমাত্রিকভাবে সুবিন্যস্ত হয়ে একটি স্ফটিক তৈরি করে। এ অবস্থায় ধনাত্মক (K') ও ঋণাত্মক (1) আয়নে পরিণত হতে পারে না। আমরা জানি, বিদ্যুৎ পরিবহনের জন্য ইলেকট্রনের আদান-প্রদান প্রয়োজন হয়। কিন্তু কঠিন KF ইলেকট্রন স্থানান্তর করতে পারে না বলে বিদ্যুৎ পরিবহন করে না।
C12H22O11 যৌগটি জলীয় দ্রবণে বিদ্যুৎ পরিবহন করে না। কারণC12H22O11যৌগটি সমযোজী যৌগ। সমযোজী যৌগ কোনো বিচ্ছিন্ন আয়ন তৈরি করে না। আর দ্রবণে আয়ন না থাকলে তা কখনই বিদ্যুৎ পরিবহন করতে পারে না। দ্রবণেC12H22O11আয়ন আকারে বিভক্ত হয় না। কাজেইC12H22O11 জলীয় দ্রবণে বিদ্যুৎ পরিবহন করে না।
ধাতব কেলাসে ধাতু পরমাণুসমূহ একত্রে পাশাপাশি অবস্থান করে। সকল ধাতুরই শেষ কক্ষপথে কমসংখ্যক ইলেকট্রন থাকে। তাই ধাতব কেলাসে এই ইলেকট্রনগুলো পরমাণুর কক্ষপথ থেকে বের হয়ে সমগ্র ধাতব খণ্ডে মুক্তভাবে চলাচল করে। ফলে বৈদ্যুতিক ক্ষেত্রের প্রভাবে বা ধাতব খন্ডকে ব্যাটারির সাথে যুক্ত করে বর্তনীপূর্ণ-করলে সহজেই বর্তনীর ঋণাত্মক প্রান্ত থেকে মুক্ত ইলেকট্রনসমূহ ধনাত্মক প্রান্তের দিকে চলাচল করে এবং এভাবেই বিদ্যুৎ পরিবহন করে।
Related Question
View All১ ক্লিকে প্রশ্ন, শীট, সাজেশন ও
অনলাইন পরীক্ষা তৈরির সফটওয়্যার!
শুধু প্রশ্ন সিলেক্ট করুন — প্রশ্নপত্র অটোমেটিক তৈরি!



